Сокращение березы
| Сокращение березы | |
|---|---|
| Назван в честь | Артур Берч |
| Тип реакции | Органическая окислительно-восстановительная реакция |
| Идентификаторы | |
| Портал органической химии | береза-редукция |
| RSC Идентификатор онтологии | RXNO: 0000042 |
Восстановление Берча — это органическая реакция, которая используется для преобразования аренов в 1,4-циклогексадиены . Реакция названа в честь австралийского химика Артура Берча и включает органическое восстановление ароматических колец в аминовом растворителе (традиционно жидкий аммиак ) с помощью щелочного металла (традиционно натрий) и источника протонов (традиционно спирт ). В отличие от каталитического гидрирования , восстановление по Берчу не восстанавливает ароматическое кольцо полностью до циклогексана .

Примером может служить восстановление нафталина в аммиаке и этаноле:

Механизм реакции и региоселективность
[ редактировать ]Раствор натрия в жидком аммиаке состоит из соли -электрида ярко-синего цвета [Na(NH 3 ) x ] + и − . присоединяются Сольватированные электроны к ароматическому кольцу, образуя анион-радикал , который затем отрывает протон от спирта. Затем процесс повторяется либо в орто-, либо в пара -положении (в зависимости от заместителей), образуя конечный диен. [1] Остаточные двойные связи не стабилизируют дальнейшие радикальные присоединения. [2] [3]

Известно, что реакция имеет третий порядок : первый порядок по ароматическим соединениям, первый порядок по щелочному металлу и первый порядок по спирту. [4] Для этого необходимо, чтобы лимитирующей стадией было превращение анион-радикала B в циклогексадиенильный радикал C.

Этот шаг также определяет структуру продукта. Хотя Артур Берч первоначально утверждал, что протонирование происходит в мета -положении, [5] последующее исследование показало, что протонирование происходит либо в орто-, либо в пара -положении. Доноры электронов имеют тенденцию индуцировать орто- протонирование, как показано при восстановлении анизола (1). Электроноакцепторные заместители имеют тенденцию индуцировать пара -протонирование, как показано при восстановлении бензойной кислоты (2). [6]


Сольватированные электроны преимущественно восстанавливают достаточно электроотрицательные функциональные группы, такие как кетоны или нитрогруппы , но не атакуют спирты , карбоновые кислоты или простые эфиры . [6]
Вторичная региоселективность протонирования
[ редактировать ]Второе восстановление и протонирование также ставит механистические вопросы. Таким образом, карбанион имеет три резонансные структуры (на рисунке обозначены B, C и D).

Простые вычисления Хюккеля приводят к равным электронным плотностям на трех атомах 1, 3 и 5, но к асимметричному порядку связей. Изменение обменных интегралов для учета изменения межатомных расстояний дает максимальную электронную плотность в центральном атоме 1, [7] [8] [9] результат подтвержден более современными расчетами RHF . [10]
| Приближение | Атом плотности 3 | Атом плотности 2 | Атом плотности 1 | Заказ на залог 2–3 | Ордер на залог 1–2 |
|---|---|---|---|---|---|
| Хюккель (1-й прибл.) | 0.333 | 0.00 | 0.333 | 0.788 | 0.578 |
| 2-й приблизительно | 0.317 | 0.00 | 0.365 | 0.802 | 0.564 |
| 3-й приблизительно | 0.316 | 0.00 | 0.368 | 0.802 | 0.562 |
Результат аналогичен конъюгированным енолятам. Когда эти анионы (но не енольный таутомер ) кинетически протонируют, они делают это в центре, образуя β,γ-ненасыщенный карбонил. [7] [11]
Модификации
[ редактировать ]Традиционное восстановление Берча требует криогенных температур для сжижения аммиака и пирофорных доноров электронов щелочных металлов. Были разработаны варианты, позволяющие уменьшить неудобства.
Альтернативными растворителями служат многие амины: например, ТГФ. [12] [13] или смесь н -пропиламина и этилендиамина . [14]
Чтобы избежать прямой щелочи, существуют химические альтернативы, такие как восстановитель M-SG . Восстановление также может осуществляться с помощью внешнего потенциала или жертвенного анода (магния или алюминия), но тогда для совместного размещения реагентов посредством комплексообразования необходимы соли щелочных металлов. [15]
Березовое алкилирование
[ редактировать ]При алкилировании по Берчу анион , образующийся при восстановлении по Берчу, улавливается подходящим электрофилом, таким как галогеналкан , например: [16]
В замещенных ароматических соединениях электроноакцепторный заместитель , такой как карбоновая кислота , стабилизирует карбанион с образованием наименее замещенного олефина ; [17] электронодонорный заместитель оказывает противоположный эффект. [18]
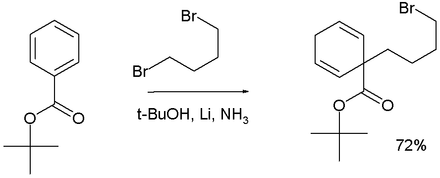
При добавлении 1,4-дибромбутана к восстановлению трет -бутилбензоата по Берчу образуется 1,1-циклогексадиеновый продукт. [19]
Уменьшение скамейки
[ редактировать ]представляет Восстановление Бенкезера собой гидрирование полициклических ароматических углеводородов , особенно нафталинов, с использованием лития или кальция металлического в растворителях на основе алкиламинов с низкой молекулярной массой . В отличие от традиционного восстановления Берча, реакцию можно проводить при температурах выше точки кипения аммиака (-33 ° C). [20] [21]
При восстановлении нафталина литием в смешанном растворе этиламин - диметиламин основными продуктами являются бицикло[3.3.0]дец-(1,9)-ен, бицикло[3.3.0]дец-(1,2)-ен. и бицикло[3.3.0]декан. [22] [23]

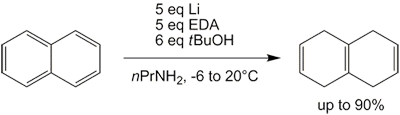
Направляющие эффекты нафталиновых заместителей остаются теоретически малоизученными. Заместители, расположенные рядом с мостиком, по-видимому, непосредственно восстанавливаются до незамещенного кольца; β-заместители (на одну связь дальше) имеют тенденцию к прямому восстановлению до замещенного кольца. [6]
История
[ редактировать ]Артур Берч , основываясь на более ранних работах Вустера и Годфри, [24] разработал реакцию во время работы в лаборатории Дайсона Перринса в Оксфордском университете . [25] В оригинальной процедуре Берча использовались натрий и этанол ; [5] [26] [27] Позже Альфред Л. Уайлдс обнаружил, что литий дает более высокий выход. [28] [29]
Реакцию было трудно понять механически, и споры продолжались до 1990-х годов.
Случай с электроноакцепторными группами очевиден, поскольку алкилирование по Берчу служит ловушкой для предпоследнего дианиона D. Этот дианион появляется даже в бесспиртовых реакциях. Таким образом, первоначальное протонирование является пара , а не ipso , как видно из превращения BC. [30] [31] [32]

Для электронодонорных заместителей Берч первоначально предложил метаатаку , соответствующую местонахождению наибольшей электронной плотности в нейтральном бензольном кольце , и эту позицию поддержали Крапчо и Ботнер-Бай. [4] [33] Эти выводы были оспорены Циммерманом в 1961 году, который рассчитал электронную плотность радикальных и диеновых анионов, обнаружив, что орто- сайт был наиболее отрицательным и, следовательно, с наибольшей вероятностью протонировал. [7] [9] Но ситуация оставалась неопределенной, поскольку вычисления оставались очень чувствительными к геометрии перехода. Хуже того, орбитальные вычисления Хюкеля и неограниченные вычисления Хартри-Фока дали противоречивые ответы. Бёрнем в 1969 году пришел к выводу, что самые надежные вычисления поддерживают метаатаку ; [34] Бёрч и Радом в 1980 году пришли к выводу, что как орто-, так и мета- замены будут происходить с небольшим предпочтением орто-замен . [35]
В начале 1990-х годов Циммерман и Ван разработали методику эксперимента, позволяющую различать орто- и мета- протонирование. Метод начался с предпосылки, что карбанионы гораздо более основные, чем соответствующие анионы-радикалы, и поэтому протонируют менее избирательно. Соответственно, два протонирования при восстановлении Берча должны проявлять изотопный эффект : в протиево-дейтериевой среде анион-радикал должен преимущественно протонировать, а карбанион дейтерировать. Действительно, различные метоксилированные ароматические соединения содержали меньше орто- дейтерия, чем мета (соотношение 1:7). Более того, современные расчеты электронной плотности теперь твердо указывают на орто- протонирование; пограничные орбитальные плотности, наиболее аналогичные традиционным вычислениям, использованным в прошлых исследованиях, этого не сделали. [10]
не хотел признавать, что орто- протонирование является предпочтительным, Хотя Бёрч еще в 1996 году [36] Циммерман и Ван одержали победу: современные учебники однозначно согласны с тем, что электронодонорные заместители способствуют орто- атаке. [6]
Дополнительное чтение
[ редактировать ]- Кейн, Д. (1976). «Восстановление и родственные реакции α,β-ненасыщенных карбонильных соединений с металлами в жидком аммиаке». Орг. Реагировать. (обзор). 23 : 1–258. дои : 10.1002/0471264180.или023.01 . ISBN 0471264180 .
См. также
[ редактировать ]- Сольватированный электрон — восстановитель
- Восстановление Буво – Блана - еще одна реакция с использованием сольватированных электронов.
- Синтез метамфетамина — применение
Ссылки
[ редактировать ]- ^ Марч, Джерри (1985), Продвинутая органическая химия: реакции, механизмы и структура, 3-е издание , Нью-Йорк: Wiley, ISBN 9780471854722 , OCLC 642506595
- ^ Рабидо, П.В.; Марсинов, З. (1992). «Березовое восстановление ароматических соединений». Орг. Реагировать. (обзор). 42 : 1–334. дои : 10.1002/0471264180.или042.01 . ISBN 0471264180 .
- ^ Мандер, Л.Н. (1991). «Частичное восстановление ароматических колец растворением металлов и другими методами». Компр. Орг. Синтез. (обзор). 8 : 489–521. дои : 10.1016/B978-0-08-052349-1.00237-7 . ISBN 978-0-08-052349-1 .
- ^ Jump up to: а б Крапчо, АП; Ботнер-Бай, А.А. (1959). «Кинетика металл-аммиачно-спиртового восстановления бензола и замещенных бензолов1». Дж. Ам. хим. Соц . 81 (14): 3658–3666. дои : 10.1021/ja01523a042 .
- ^ Jump up to: а б Березка 1944 года .
- ^ Jump up to: а б с д Кэри, Фрэнсис А.; Сундберг, Ричард Дж. (2007). Продвинутая органическая химия . Том. B: Реакции и синтез (5-е изд.). Нью-Йорк: Спрингер. стр. 437–439. ISBN 978-0-387-44899-2 .
- ^ Jump up to: а б с Циммерман, HE (1961). «Ориентация на снижение металлического аммиака». Тетраэдр . 16 (1–4): 169–176. дои : 10.1016/0040-4020(61)80067-7 .
- ^ Циммерман, Ховард Э. (1975). Квантовая механика для химиков-органиков . Нью-Йорк: Академическая пресса. стр. 154–5 . ISBN 0-12-781650-Х .
- ^ Jump up to: а б Циммерман, HE (1963). «Перегруппировки, катализируемые основаниями». В Де Майо, П. (ред.). Молекулярные перегруппировки . Нью-Йорк: Межнаучный. стр. 350–352.
- ^ Jump up to: а б
- Циммерман, HE; Ван, Пенсильвания (1990). «Региоселективность редукции березы». Дж. Ам. хим. Соц . 112 (3): 1280–1281. дои : 10.1021/ja00159a078 .
- Циммерман, HE; Ван, Пенсильвания (1993). «Региоселективность редукции березы». Дж. Ам. хим. Соц . 115 (6): 2205–2216. дои : 10.1021/ja00059a015 .
- ^ Пауфлер, Р.М. (1960) доктор философии. Диссертация, Северо-Западный университет, Эванстон, Иллинойс.
- ^ Эчери, Золтан и Мюллер, Миклош (1961). «Восстановление витамина D2 щелочными металлами». Венгерский химический журнал . 67 : 330–332.
- ^ Донохо, Тимоти Дж. и Хаус, Дэвид (2002). «Частичное безаммиачное восстановление ароматических соединений с использованием ди- трет -бутилбифенила лития (LiDBB)». Журнал органической химии . 67 (14): 5015–5018. дои : 10.1021/jo0257593 . ПМИД 12098328 .
- ^ Гарст, Майкл Э.; Ллойд Дж.; Шервин; Н. Андрей; Натали С.; Альфред А.; и др. (2000). «Восстановление литием в низкомолекулярных аминах и этилендиамине». Журнал органической химии . 65 (21): 7098–7104. дои : 10.1021/jo0008136 . ПМИД 11031034 .
- ^ Питерс, Байрон К.; Родригес, Кевин X.; Рейсберг, Соломон Х.; Бейл, Себастьян Б.; Хики, Дэвид П.; Кавамата, Ю; Коллинз, Майкл; Старр, Джереми; Чен, Лонгруй; Удьявара, Сагар; Кландер, Кевин; Гори, Тимоти Дж.; Андерсон, Скотт Л.; Нейрок, Мэтью; Минтир, Шелли Д.; Бэран, Фил С. (21 февраля 2019 г.). «Масштабируемое и безопасное синтетическое органическое электровосстановление, вдохновленное химией литий-ионных аккумуляторов» . Наука . 363 (6429): 838–845. Бибкод : 2019Sci...363..838P . дои : 10.1126/science.aav5606 . ПМК 7001862 . ПМИД 30792297 .
- ^ Табер, DF; Ганн, BP; Чинг Чиу, И. (1983). «Алкилирование аниона в результате восстановления о-анисовой кислоты по Берчу: 2-гептил-2-циклогексенон» . Органические синтезы ; Сборник томов , т. 7, с. 249 .
- ^ Кюне, Мэн; Ламберт, Б.Ф. (1963). «1,4-Дигидробензойная кислота» . Органические синтезы ; Сборник томов , т. 5, с. 400 .
- ^ Пакетт, Луизиана; Барретт, Дж. Х. (1969). «2,7-Диметилоксепин» . Органические синтезы ; Сборник томов , т. 5, с. 467 .
- ^ Клайв, Деррик Л.Дж. и Сунаси, Раджеш (2007). «Образование бензоконденсированных карбоциклов путем формальной радикальной циклизации на ароматическом кольце». Органические письма . 9 (14): 2677–2680. дои : 10.1021/ol070849l . ПМИД 17559217 .
- ^ Березовые сокращения , Институт химии, Скопье , Македония.
- ^ Фогель, Э.; Клюг, В.; Брейер, А. (1974). «1,6-Метано[10]аннулен» . Органические синтезы ; Сборник томов , т. 6 .
- ^ Эдвин М. Кайзер и Роберт А. Бенкезер "Δ 9,10 -Окталин" Org. Synth. 1970, т. 50, стр. 88 и далее. doi : 10.15227/orgsyn.050.0088
- ^ Индекс Merck , 13-е изд.
- ^ Вустер, CB; Годфри, КЛ (1937). «Механизм восстановления ненасыщенных соединений щелочными металлами и водой». Журнал Американского химического общества . 59 (3): 596. doi : 10.1021/ja01282a504 .
- ^
- Берч, Эй Джей (1944). «Восстановление растворением металлов. Часть I». Дж. Хим. Соц. : 430. дои : 10.1039/JR9440000430 .
- Берч, AJ (1945). «Восстановление растворением металлов. Часть II». Дж. Хим. Соц. : 809. дои : 10.1039/jr9450000809 .
- Берч, AJ (1946). «Восстановление растворением металлов. Часть III». Дж. Хим. Соц. : 593. дои : 10.1039/jr9460000593 .
- Берч, Эй Джей (1947). «Восстановление растворением металлов. Часть IV». Дж. Хим. Соц. : 102. дои : 10.1039/jr9470000102 .
- Берч, Артур Дж. (1947). «Восстановление растворением металлов. Часть V». Дж. Хим. Соц. : 1642. дои : 10.1039/jr9470001642 .
- Берч, Эй Джей; Мухерджи, С.М. (1949). «Восстановление растворением металлов. Часть VI. Некоторые приложения в синтезе». Дж. Хим. Соц. : 2531. дои : 10.1039/jr9490002531 .
- ^ Береза 1945 .
- ^ Береза 1946 .
- ^ Уайлдс, Алабама; Нельсон, Н.А. (1953). «Превосходный метод восстановления эфиров фенолов до дигидропроизводных и ненасыщенных кетонов». Дж. Ам. хим. Соц . 75 (21): 5360–5365. дои : 10.1021/ja01117a064 .
- ^ Берч, Эй Джей; Смит, Х. (1958). «Восстановление растворами металлов и аминов: применение в синтезе и определении структуры». Кварта. Преподобный (обзор). 12 (1): 17. дои : 10.1039/qr9581200017 .
- ^ Бачи, JW; Эпштейн, Ю.; Герцберг-Минцли, Х.; Левенталь, Дж. Э. (1969). «Синтез соединений, родственных гиббереллиновой кислоте. III. Аналоги кольца А гиббереллинов». Дж. Орг. Хим . 34 : 126–135. дои : 10.1021/jo00838a030 .
- ^ Табер, DF; Ганн, BP; Чинг Чиу, я (1983). «Алкилирование аниона в результате восстановления о-анисовой кислоты по Берчу: 2-гептил-2-циклогексенон» . Органические синтезы . 61:59 ; Сборник томов , т. 7, с. 249 .
- ^ Го, З.; Шульц, АГ (2001). «Методология органического синтеза. Получение и диастереоселективное восстановление-алкилирование 3-замещенных 2-метил-2,3-дигидроизоиндол-1-онов». Дж. Орг. Хим . 66 (6): 2154–2157. дои : 10.1021/jo005693g . ПМИД 11300915 .
- ^ Берч, Эй Джей; Насипури, Д. (1959). «Механизмы реакций восстановления металлоаммиачными растворами». Тетраэдр . 6 (2): 148–153. дои : 10.1016/0040-4020(59)85008-0 .
- ^ Бернхэм, ДР (1969). «Ориентации в механизме восстановления анизола по Берчу». Тетраэдр . 25 (4): 897–904. дои : 10.1016/0040-4020(69)85023-4 .
- ^
- Берч, Эй Джей; Хинде, Алабама; Радом, Л. (1980). «Теоретический подход к восстановлению Берча. Структура и стабильность анион-радикалов замещенных бензолов». Дж. Ам. хим. Соц . 102 (10): 3370–3376. дои : 10.1021/ja00530a012 .
- Берч, Эй Джей; Радом, Л. (1980). «Теоретический подход к восстановлению Берча. Структура и стабильность циклогексадиенильных радикалов». Дж. Ам. хим. Соц . 102 (12): 4074–4080. дои : 10.1021/ja00532a016 .
- ^ См. диаграммы в:
- Берч, Эй Джей (1992). «Стероидные гормоны и Люфтваффе. Предприятие фундаментальных стратегических исследований и некоторые его последствия: сокращение Берча становится сокращением рождаемости». Стероиды . 57 (8): 363–377. дои : 10.1016/0039-128X(92)90080-S . ПМИД 1519267 . S2CID 24827957 .
- Берч, Эй Джей (1996). «Редукция Берча в органическом синтезе» . Чистое приложение. Хим . 68 (3): 553–556. дои : 10.1351/pac199668030553 . S2CID 41494178 .

