Нафталин
| |||
 | |||
 | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Нафталин [2] | |||
| Другие имена белая смола, камфорная смола, камфорная смола, нафталин, нафталин, антиклещ, альбокарбон, гексален, нафталиновые шарики, хлопья моли [1] | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| 1421310 | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.001.863 | ||
| Номер ЕС |
| ||
| 3347 | |||
| КЕГГ | |||
ПабХим CID | |||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 10 Ч 8 | |||
| Молярная масса | 128.174 g·mol −1 | ||
| Появление | Белые твердые кристаллы/хлопья | ||
| Запах | Сильный запах каменноугольной смолы или нафталина | ||
| Плотность | 1,145 г/см 3 (15,5 °С) [3] 1,0253 г/см 3 (20 °С) [4] 0,9625 г/см 3 (100 °С) [3] | ||
| Температура плавления | 78,2 ° С (172,8 ° F; 351,3 К) 80,26 ° С (176,47 ° F; 353,41 К) при 760 мм рт.ст. [4] | ||
| Точка кипения | 217,97 ° С (424,35 ° F; 491,12 К) при 760 мм рт.ст. [3] [4] | ||
| 19 мг/л (10 °С) 31,6 мг/л (25 °С) 43,9 мг/л (34,5 °С) 80,9 мг/л (50 °С) [4] 238,1 мг/л (73,4 °С) [5] | |||
| Растворимость | Растворим в спиртах , нашатырном спирте , Карбоновых кислотах , C 6 H 6 , SO 2 , [5] CCl 4 , CS 2 , толуол , анилин [6] | ||
| Растворимость в этаноле | 5 г/100 г (0 °С) 11,3 г/100 г (25 °С) 19,5 г/100 г (40 °С) 179 г/100 г (70 °С) [6] | ||
| Растворимость в уксусной кислоте | 6,8 г/100 г (6,75 °С) 13,1 г/100 г (21,5 °С) 31,1 г/100 г (42,5 °С) 111 г/100 г (60 °С) [6] | ||
| Растворимость в хлороформе | 19,5 г/100 г (0 °С) 35,5 г/100 г (25 °С) 49,5 г/100 г (40 °С) 87,2 г/100 г (70 °С) [6] | ||
| Растворимость в гексане | 5,5 г/100 г (0 °С) 17,5 г/100 г (25 °С) 30,8 г/100 г (40 °С) 78,8 г/100 г (70 °С) [6] | ||
| Растворимость в масляной кислоте | 13,6 г/100 г (6,75 °С) 22,1 г/100 г (21,5 °С) 131,6 г/100 г (60 °С) [6] | ||
| войти P | 3.34 [4] | ||
| Давление пара | 8,64 Па (20 °С) 23,6 Па (30 °С) 0,93 кПа (80 °С) [5] 2,5 кПа (100 °С) [7] | ||
Закон Генри постоянная ( k H ) | 0,42438 л·атм/моль [4] | ||
| -91.9·10 −6 см 3 /моль | |||
| Теплопроводность | 98 кПа: 0,1219 Вт/м·К (372,22 К) 0,1174 Вт/м·К (400,22 К) 0,1152 Вт/м·К (418,37 К) 0,1052 Вт/м·К (479,72 К) [8] | ||
Показатель преломления ( n D ) | 1.5898 [4] | ||
| Вязкость | 0,964 сП (80 °С) 0,761 сП (100 ° С) 0,217 сП (150 °С) [9] | ||
| Структура | |||
| Моноклиника [10] | |||
| Р2 1 /б [10] | |||
| С 5 2 часа [10] | |||
а = 8,235 Å, b = 6,003 Å, c = 8,658 Å [10] α = 90°, β = 122,92°, γ = 90° | |||
| Термохимия | |||
Теплоемкость ( С ) | 165,72 Дж/моль·К [4] | ||
Стандартный моляр энтропия ( S ⦵ 298 ) | 167,39 Дж/моль·К [4] [7] | ||
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | 78,53 кДж/моль [4] | ||
Свободная энергия Гиббса (Δ f G ⦵ ) | 201,585 кДж/моль [4] | ||
Стандартная энтальпия горение (Δ c H ⦵ 298 ) | -5156,3 кДж/моль [4] | ||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | Огнеопасно , сенсибилизатор , возможный канцероген . [12] Пыль может образовывать взрывоопасные смеси с воздухом. | ||
| СГС Маркировка : | |||
    [11] [11] | |||
| Опасность | |||
| Х228 , Х302 , Х351 , Х410 [11] | |||
| П210 , П273 , П281 , П501 [11] | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 80 ° С (176 ° F; 353 К) [11] | ||
| 525 ° C (977 ° F; 798 К) [11] | |||
| Взрывоопасные пределы | 5.9% [11] | ||
| 10 частей на миллион [4] (СВВ), 15 частей на миллион [4] (НАБОР) | |||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза ) | 1800 мг/кг (крыса, перорально) 490 мг/кг (крыса, внутривенно) 1200 мг/кг (морская свинка, перорально) 533 мг/кг (мыши, перорально) [14] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
МЕХ (Допускается) | TWA 10 частей на миллион (50 мг/м 3 ) [13] | ||
РЕЛ (рекомендуется) | TWA 10 частей на миллион (50 мг/м 3 ) ST 15 частей на миллион (75 мг/м 3 ) [13] | ||
IDLH (Непосредственная опасность) | 250 частей на миллион [13] | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Нафталин — органическое соединение формулы С.
10 ч.
8 . Это простейший полициклический ароматический углеводород , представляющий собой белое кристаллическое твердое вещество с характерным запахом, который можно обнаружить уже при концентрациях всего 0,08 частей на миллион по массе . [15] углеводорода Структура ароматического нафталина состоит из конденсированной пары бензольных колец. Это основной ингредиент традиционных нафталиновых шариков .
История [ править ]
В начале 1820-х годов в двух отдельных отчетах описывалось белое твердое вещество с резким запахом, полученное в результате перегонки каменноугольной смолы . В 1821 году Джон Кидд процитировал эти два открытия, а затем описал многие свойства этого вещества и способы его производства. Он предложил название «нафталин» , поскольку оно произошло от разновидности нафты (широкий термин, охватывающий любую летучую, легковоспламеняющуюся жидкую углеводородную смесь, включая каменноугольную смолу). [16] Химическая формула нафталина была определена Майклом Фарадеем в 1826 году. Структура двух конденсированных бензольных колец была предложена Эмилем Эрленмейером в 1866 году. [17] и подтверждено Карлом Гребе три года спустя. [18]
Физические свойства [ править ]
Молекулу нафталина можно рассматривать как слияние пары бензольных колец. (В органической химии кольца сливаются, если они имеют два или более общих атома.) Таким образом, нафталин классифицируется как бензоидный полициклический ароматический углеводород (ПАУ). [19]
Восемь атомов углерода, которые не являются общими для двух колец, несут по одному атому водорода каждый. В стандартной номенклатуре производных соединений ИЮПАК эти восемь атомов пронумерованы последовательно от 1 до 8 по периметру молекулы, начиная с атома углерода, соседнего с общим. Общие атомы углерода обозначены 4а (между 4 и 5) и 8а (между 8 и 1). [20]
Молекулярная геометрия [ править ]
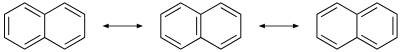
Молекула плоская, как у бензола. В отличие от бензола связи углерод-углерод в нафталине имеют разную длину. Связи C1-C2, C3-C4, C5-C6 и C7-C8 имеют длину около 1,37 Å (137 пм), тогда как длина других связей углерод-углерод составляет около 1,42 Å (142 пм). Эта разница, установленная методом рентгеновской дифракции , [21] согласуется с моделью валентной связи в нафталине и, в частности, с теоремой о перекрестном сопряжении . Эта теорема описывает нафталин как ароматическое бензольное звено, связанное с диеном , но не сопряженное с ним в значительной степени (по крайней мере, в основном состоянии ), что согласуется с двумя из трех его резонансных структур.
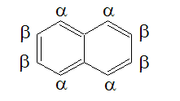
Благодаря этому резонансу молекула имеет двустороннюю симметрию в плоскости общей пары углерода, а также в плоскости, разделяющей пополам связи C2-C3 и C6-C7, и в плоскости атомов углерода. Таким образом, существует два набора эквивалентных атомов водорода: альфа- положения, пронумерованные 1, 4, 5 и 8, и бета- положения, 2, 3, 6 и 7. Тогда возможны два изомера монозамещенных нафталинов, соответствующие к замене в альфа- или бета-позиции.

Структурные изомеры нафталина, имеющие два конденсированных ароматических кольца, включают азулен , который имеет конденсированную систему колец 5–7, и бицикло[6.2.0]декапентаен , который имеет конденсированную систему колец 4–8. [22]
Точечная группа симметрии нафталина D 2h .
Электропроводность [ править ]
Чистый кристаллический нафталин является умеренным изолятором при комнатной температуре с удельным сопротивлением около 10 12 Ом м . При плавлении удельное сопротивление падает более чем в тысячу раз, примерно до 4 × 10. 8 Ом м. Как в жидкости, так и в твердом теле удельное сопротивление зависит от температуры по закону ρ = ρ 0 exp( E /( k T )), где ρ 0 (Ом м) и E (эВ) — постоянные параметры, k — постоянная Больцмана ( 8,617×10 −5 эВ/ К ), а Т — абсолютная температура (К). Параметр Е равен 0,73 в твердом теле. Однако твердое тело проявляет полупроводниковый характер ниже 100 К. [23] [24]
Химические свойства [ править ]
Реакции с электрофилами [ править ]
В реакциях электрофильного ароматического замещения нафталин реагирует легче, чем бензол. Например, хлорирование и бромирование нафталина протекает без катализатора с образованием 1-хлорнафталина и 1-бромнафталина соответственно. Аналогичным образом, хотя и бензол, и нафталин можно алкилировать с использованием условий реакции Фриделя-Крафтса , нафталин также можно легко алкилировать путем реакции с алкенами или спиртами с использованием серной или фосфорной кислоты . катализаторов [25]
С точки зрения региохимии , электрофилы атакуют альфа-положение. Селективность альфа-замещения по сравнению с бета-заменой можно объяснить с точки зрения резонансных структур промежуточного соединения: для промежуточного альфа-замещения можно выделить семь резонансных структур, четыре из которых сохраняют ароматическое кольцо. При бета-замещении промежуточное соединение имеет только шесть резонансных структур, и только две из них являются ароматическими. Сульфирование дает «альфа»-продукт нафталин-1-сульфоновую кислоту в качестве кинетического продукта, но нафталин-2-сульфоновую кислоту в качестве термодинамического продукта. Изомер 1 образуется преимущественно при 25 °C, а изомер 2 — при 160 °C. Сульфирование с образованием 1- и 2-сульфоновой кислоты происходит легко:
- H 2 SO 4 + C 10 H 8 → C 10 H 7 SO 3 H + H 2 O
Дальнейшее сульфирование дает ди-, три- и тетрасульфоновые кислоты.
Литиация [ править ]
Аналогично синтезу фениллития происходит превращение 1-бромнафталина в 1-литионафталин путем литий-галогенного обмена :
- C 10 H 7 Br + BuLi → C 10 H 7 Li + BuBr
Образующийся литионафталин подвергается вторичному литиированию, в отличие от поведения фениллития. Эти 1,8-дилитиопроизводные являются предшественниками множества производных перинафталина . [26]
Восстановление и окисление [ править ]
С щелочными металлами нафталин образует темно-сине-зеленые анионные соли-радикалы, такие как нафталин натрия , Na. + С 10 Ч −
8 . Анионы нафталина являются сильными восстановителями.
Нафталин можно гидрировать под высоким давлением в присутствии металлических катализаторов с образованием 1,2,3,4-тетрагидронафталина ( C
10 ч.
12 ), также известный как тетралин . Дальнейшее гидрирование дает декагидронафталин или декалин ( C
10 ч.
18 ).
Окисление O
2 в присутствии пятиокиси ванадия в качестве катализатора дает фталевый ангидрид :
- С 10 Н 8 + 4,5 О 2 → С 6 Н 4 (СО) 2 О + 2 СО 2 + 2 Н 2 О
Эта реакция лежит в основе основного применения нафталина. Окисление также можно осуществлять с использованием обычных стехиометрических хроматных или перманганатных реагентов.
Производство [ править ]

Большую часть нафталина получают из каменноугольной смолы . С 1960-х по 1990-е годы значительные объемы нафталина производились также из тяжелых нефтяных фракций при переработке нефти , но в настоящее время производство осуществляется в основном из каменноугольной смолы. Ежегодно производится около 1,3 млн тонн.
Нафталин является наиболее распространенным компонентом каменноугольной смолы. Состав каменноугольной смолы варьируется в зависимости от типа угля и обработки, но типичная каменноугольная смола содержит около 10% нафталина по весу. В промышленной практике перегонка каменноугольной смолы дает масло, содержащее около 50% нафталина, а также двенадцать других ароматических соединений . Это масло после промывки водным раствором едкого натра для удаления кислых компонентов (главным образом различных фенолов ) и серной кислотой для удаления основных компонентов подвергают фракционной перегонке для выделения нафталина. Сырой нафталин, полученный в результате этого процесса, содержит около 95% нафталина по весу. Основными примесями являются серосодержащее ароматическое соединение бензотиофен (<2%), индан (0,2%), инден (<2%) и метилнафталин (<2%). Нафталин, полученный из нефти, обычно чище, чем нафталин, полученный из каменноугольной смолы. При необходимости сырой нафталин можно дополнительно очистить путем перекристаллизации из любого из множества растворителей, в результате чего будет получено 99% нафталина по массе, что соответствует температуре 80 °C (точка плавления). [25]
В Северной Америке производителями каменноугольной смолы являются Koppers Inc., Ruetgers Canada Inc. и Recochem Inc., а основным производителем нефти — Monument Chemical Inc.. В Западной Европе известными производителями являются Koppers, Ruetgers и Deza. В Восточной Европе нафталин производят различные металлургические комбинаты (Северсталь, Евраз, Мечел, ММК) в России , специализированные производители нафталина и фенола ИНКОР, Енакиевский металлургический завод в Украине и АрселорМиттал Темиртау в Казахстане .
Другие источники и явления [ править ]
Нафталин и его алкильные гомологи являются основными компонентами креозота .
Следовые количества нафталина производятся магнолиями и некоторыми видами оленей , а также формозскими подземными термитами , которые, возможно, производятся термитами в качестве репеллента против «муравьев, ядовитых грибов и нематод ». [27] Некоторые штаммы эндофитного гриба Muscodor albus производят нафталин среди ряда летучих органических соединений, тогда как Muscodor vitigenus производит почти исключительно нафталин. [28]
Использует [ править ]
Нафталин используется главным образом в качестве предшественника производных химических веществ. Самым крупным применением нафталина является промышленное производство фталевого ангидрида , хотя больше фталевого ангидрида производится из о -ксилола .
Фумигант [ править ]
Нафталин использовался в качестве фумиганта . Когда-то он был основным ингредиентом нафталиновых шариков , хотя сейчас его использование в значительной степени заменено альтернативами, такими как 1,4-дихлорбензол . В герметичном контейнере, содержащем гранулы нафталина, пары нафталина достигают уровня, токсичного как для взрослых, так и для личинок многих бабочек , поражающих текстиль. Другие фумигантные применения нафталина включают использование в почве в качестве фумиганта- пестицида , на чердаках для отпугивания насекомых и животных, таких как опоссумы , [29] а также в музейных ящиках и шкафах для защиты содержимого от нападения насекомых-вредителей.
Растворитель [ править ]
Расплавленный нафталин представляет собой превосходную среду, солюбилизирующую плохо растворимые ароматические соединения. Во многих случаях он более эффективен, чем другие высококипящие растворители, такие как дихлорбензол , бензонитрил , нитробензол и дурол . Реакцию C 60 с антраценом удобно проводить при кипячении нафталина с образованием аддукта Дильса-Альдера 1:1 . [30] Ароматизация гидропорфиринов достигнута с использованием раствора ДДХ в нафталине. [31]
Производное использование [ править ]
производство фталевого ангидрида , который является промежуточным продуктом, используемым для производства пластификаторов поливинилхлорида Самым крупным применением нафталина является , а также для производства полимеров алкидных смол, используемых в красках и лаках.
Сульфоновые кислоты и сульфонаты [ править ]
многие нафталинсульфоновые кислоты Полезны и сульфонаты. Нафталинсульфоновые кислоты используются в синтезе 1-нафтола и 2-нафтола , прекурсоров различных красителей, пигментов, химикатов для переработки резины и других химикатов и фармацевтических препаратов. [25] Они также используются в качестве диспергаторов в синтетических и натуральных каучуках, сельскохозяйственных пестицидах , красителях и пластинах свинцово-кислотных аккумуляторов . Нафталиндисульфоновые кислоты, такие как кислота Армстронга, используются в качестве предшественников и для образования фармацевтических солей, таких как CFT .
Аминонафталинсульфокислоты являются предшественниками синтеза многих синтетических красителей .
Алкилнафталинсульфонаты (смачивающих агентов) , (АНС) используются во многих отраслях промышленности в качестве немоющих поверхностно-активных веществ которые эффективно диспергируют коллоидные системы в водных средах. Основное коммерческое применение находится в сельскохозяйственной химической промышленности, где АНС используется для смачивающихся порошков и смачиваемых гранулированных (сухосыпучих) составов, а также в текстильной и тканевой промышленности, где смачивающие и пеногасящие свойства АНС используются для операций отбеливания и крашения.
Некоторые нафталинсульфонатные полимеры являются суперпластификаторами, используемыми для производства высокопрочных бетонов . Их получают путем обработки нафталинсульфокислоты формальдегидом с последующей нейтрализацией гидроксидом натрия или гидроксидом кальция .
Другое использование производное

Многие азокрасители производятся из нафталина. Полезные агрохимикаты включают нафтоксиуксусные кислоты. [25]
При гидрировании нафталина получают тетрагидронафталин ( тетралин ) и декагидронафталин ( декалин ), которые используются в качестве малолетучих растворителей . Тетралин используется в качестве растворителя-донора водорода. [25]
Алкилирование нафталина пропиленом дает смесь диизопропилнафталинов , которые используются в качестве нелетучих жидкостей для чернил. [25]
Замещенные нафталины служат фармацевтическими препаратами, такими как пропранолол ( бета-блокатор ) и набуметон ( нестероидный противовоспалительный препарат ).
Другое использование [ править ]
Несколько применений обусловлены высокой летучестью нафталина: он используется для создания искусственных пор при производстве шлифовальных кругов с высокой пористостью ; используется в инженерных исследованиях теплопередачи с использованием сублимации массы ; и он был исследован в качестве сублимируемого топлива для двигателей спутников на холодном газе. [32] [33]
Влияние на здоровье [ править ]
Воздействие большого количества нафталина может повредить или разрушить эритроциты , чаще всего у людей с наследственным заболеванием, известным как дефицит глюкозо-6-фосфатдегидрогеназы (G6PD) . [34] от которого страдают более 400 миллионов человек. У людей, особенно детей, развилось состояние, известное как гемолитическая анемия , после проглатывания нафталиновых шариков или дезодорантов, содержащих нафталин. Симптомы включают усталость , отсутствие аппетита, беспокойство и бледность кожи. Воздействие большого количества нафталина может вызвать спутанность сознания , тошноту , рвоту , диарею , кровь в моче и желтуху (желтое окрашивание кожи из-за дисфункции печени ) . [35]
США Национальная токсикологическая программа (NTP) провела эксперимент, в ходе которого самцы и самки крыс и мышей подвергались воздействию паров нафталина в будние дни в течение двух лет. [36] Как у самцов, так и у самок крыс были обнаружены признаки канцерогенеза с увеличением случаев аденомы и нейробластомы носа. У самок мышей были обнаружены некоторые признаки канцерогенеза, основанные на увеличении случаев , тогда как у самцов альвеолярных и бронхиолярных аденом легких мышей не было обнаружено никаких признаков канцерогенеза.
Международное агентство по исследованию рака (IARC) [37] классифицирует нафталин как потенциально канцерогенный для человека и животных ( Группа 2B ). МАИР также указывает, что острое воздействие вызывает катаракту у людей, крыс , кроликов и мышей ; и что гемолитическая анемия (описанная выше) может возникнуть у детей и младенцев после перорального или ингаляционного воздействия или после воздействия на мать во время беременности. Калифорнии Согласно Положению 65 , нафталин внесен в список «известных в штате как вызывающих рак». [38] Выявлен вероятный механизм канцерогенного действия нафталиновых шариков и некоторых видов освежителей воздуха, содержащих нафталин. [39] [40]
Регламент [ править ]
Правительственные учреждения США установили пределы профессионального воздействия нафталина. Управление по охране труда установило допустимый предел воздействия на уровне 10 частей на миллион (50 мг/м2). 3 ) в течение восьмичасового средневзвешенного значения. Национальный институт охраны труда и здоровья установил рекомендуемый предел воздействия на уровне 10 частей на миллион (50 мг/м2). 3 ) более восьмичасового средневзвешенного значения, а также предел кратковременного воздействия на уровне 15 частей на миллион (75 мг/м 3 ). [41] Минимальный порог запаха нафталина для человека составляет 0,084 ppm. [42]
Нафталины и другие продукты, содержащие нафталин, запрещены на территории ЕС с 2008 года. [43] [44]
В Китае запрещено использование нафталина в нафталиновых шариках. [45] опасность для здоровья человека и повсеместное использование натуральной камфоры В качестве причин запрета называют .
Производные нафталина [ править ]
Неполный список производных нафталина включает следующие соединения:
| Имя | Химическая формула | Молярная масса [g/mol] | Температура плавления [°C] | Точка кипения [°С] | Плотность [г/см 3 ] | Показатель преломления |
|---|---|---|---|---|---|---|
| 1-нафтойная кислота | С 11 Н 8 О 2 | 172.18 | 157 | 300 | – | |
| 2-нафтойная кислота | С 11 Н 8 О 2 | 172.18 | 185.5 | – | ||
| 1-нафтоилхлорид | С 11 Н 7 ClO | 190.63 | 16–19 | 190 (35 Торр ) | 1.265 | 1.6552 |
| 1-Нафтол | С 10 Н 8 О | 144,17 | 94–96 | 278 | 1.224 | – |
| 1-Нафтальдегид | С 11 Н 8 О | 156,18 | 1–2 | 160 (15 Торр) | ||
| 1-нитронафталин | С 10 Ч 7 НЕТ 2 | 173.17 | 53–57 | 340 | 1.22 | – |
| 1-фторонафталин | С 10 Ч 7 Ж | 146.16 | −19 | 215 | 1.323 | 1.593 |
| 1-хлоронафталин | С 10 Н 7 Cl | 162.62 | −6 | 259 | 1.194 | 1.632 |
| 2-хлоронафталин | С 10 Н 7 Cl | 162.62 | 59.5 | 256 | 1.138 | 1.643 |
| 1-бромнафталин | С 10 Ч 7 Бр | 207.07 | −2 | 279 | 1.489 | 1.670 |
| 1,2,7-Триметилнафталин (Сапоталин) | С 13 Ч 14 | 170.25 | 143 | 128 | 0.987 | |
| Нафталин-2-сульфоновая кислота |
См. также [ править ]
- Камфора
- Диалин , Тетралин , Декалин
- Список межзвездных и околозвездных молекул
- Нафталиновые шарики
- 1-Нафтол , 2-Нафтол
- Реакция Вагнера-Яурега (классический синтез нафталина)
Ссылки [ править ]
- ^ Нафталин: торговые названия
- ^ Номенклатура органической химии: рекомендации ИЮПАК и предпочтительные названия 2013 г. (Синяя книга) . Кембридж: Королевское химическое общество . 2014. стр. 13, 35, 204, 207, 221–222, 302, 457, 461, 469, 601, 650. doi : 10.1039/9781849733069-FP001 (неактивно 22 июня 2024 г.). ISBN 978-0-85404-182-4 .
{{cite book}}: CS1 maint: DOI неактивен по состоянию на июнь 2024 г. ( ссылка ) - ^ Jump up to: Перейти обратно: а б с «Критерии качества окружающей воды для нафталина» (PDF) . Агентство по охране окружающей среды США. 23 апреля 2014 г. Проверено 21 июня 2014 г.
- ^ Jump up to: Перейти обратно: а б с д и ж г час я дж к л м н Лиде, Дэвид Р., изд. (2009). Справочник CRC по химии и физике (90-е изд.). Бока-Ратон, Флорида : CRC Press . ISBN 978-1-4200-9084-0 .
- ^ Jump up to: Перейти обратно: а б с Анатольевич, Кипер Руслан. «нафталин» . chemister.ru . Проверено 21 июня 2014 г.
- ^ Jump up to: Перейти обратно: а б с д и ж Зейделл, Атертон; Линке, Уильям Ф. (1919). Растворимость неорганических и органических соединений (2-е изд.). Нью-Йорк: Компания Д. Ван Ностранда. стр. 443–446 .
- ^ Jump up to: Перейти обратно: а б Нафталин в Линстреме, Питере Дж.; Маллард, Уильям Г. (ред.); Интернет-книга NIST по химии , справочная база данных стандартов NIST № 69 , Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд) (получено 24 мая 2014 г.)
- ^ «Теплопроводность нафталина» . ДДБСТ ГмбХ . Архивировано из оригинала 4 марта 2016 г. Проверено 21 июня 2014 г.
- ^ «Динамическая вязкость нафталина» . ДДБСТ ГмбХ . Архивировано из оригинала 4 марта 2016 г. Проверено 21 июня 2014 г.
- ^ Jump up to: Перейти обратно: а б с д Дуглас, Боди Э.; Хо, Ши-Минг (2007). Строение и химия кристаллических твердых тел . Нью-Йорк: Springer Science+Business Media, Inc., с. 288. ИСБН 978-0-387-26147-8 .
- ^ Jump up to: Перейти обратно: а б с д и ж Sigma-Aldrich Co. , Нафталин .
- ^ Канцерогенность нафталина
- ^ Jump up to: Перейти обратно: а б с Карманный справочник NIOSH по химическим опасностям. «#0439» . Национальный институт безопасности и гигиены труда (NIOSH).
- ^ «Нафталин» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт безопасности и гигиены труда (NIOSH).
- ^ Амур Дж. Э., Хаутала Э (1983). «Запах как средство обеспечения химической безопасности: пороговые значения запаха по сравнению с пороговыми значениями и летучими веществами для 214 промышленных химикатов при разбавлении воздуха и воды». J Appl Токсикол . 3 (6): 272–290. дои : 10.1002/jat.2550030603 . ПМИД 6376602 . S2CID 36525625 .
- ^ Джон Кидд (1821 г.). «Наблюдения за нафталином, своеобразным веществом, напоминающим конкретное эфирное масло, которое образуется при разложении каменноугольной смолы под воздействием красного каления». Философские труды . 111 : 209–221. дои : 10.1098/rstl.1821.0017 . S2CID 97798085 .
- ^ Эмиль Эрленмейер (1866 г.). «Исследования о так называемых ароматических кислотах» . Анналы химии и фармации . 137 (3): 327–359. дои : 10.1002/jlac.18661370309 .
- ^ К. Гребе (1869) «Ueber die Constitution des Naphthalene» (О структуре нафталина), Annals of Chemistry and Pharmacie , 149 : 20–28.
- ^ «Полициклические ароматические углеводороды (ПАУ)» (PDF) . Архивировано (PDF) из оригинала 30 ноября 2014 г.
Нафталин — это ПАУ, который коммерчески производится в США.
- ^ Синяя книга , P-14.4 НУМЕРАЦИЯ
- ^ Круикшанк, DWJ; Спаркс, РА (18 октября 1960 г.). «Экспериментальное и теоретическое определение длин связей в нафталине, антрацене и других углеводородах». Труды Королевского общества A: Математические, физические и технические науки . 258 (1293): 270–285. Бибкод : 1960RSPSA.258..270C . дои : 10.1098/rspa.1960.0187 . S2CID 96765335 .
- ^ Дитер Кремер; Томас Шмидт; Чарльз В. Бок (1985). «Теоретическое определение молекулярной структуры и конформации. 14. Бицикло[6.2.0]декапентаен ароматический или антиароматический?». Дж. Орг. Хим . 50 (15): 2684–2688. дои : 10.1021/jo00215a018 .
- ^ Борнманн, Джон А. (1962). «Полупроводимость нафталина» . Журнал химической физики . 36 (6): 1691–1692. Бибкод : 1962ЖЧФ..36.1691Б . дои : 10.1063/1.1732805 . ISSN 0021-9606 .
- ^ Шейн, Л.Б.; Дюк, CB; МакГи, Арканзас (1978). «Наблюдение прыжкового перехода электронов в нафталине» . Письма о физических отзывах . 40 (3): 197–200. Бибкод : 1978PhRvL..40..197S . doi : 10.1103/PhysRevLett.40.197 . ISSN 0031-9007 .
- ^ Jump up to: Перейти обратно: а б с д и ж Герд Коллин; Хартмут Хёке; Хельмут Грейм (2003). «Нафталин и гидронафталин». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. ISBN 978-3527306732 . .
- ^ ван Соолинген Дж., де Ланг Р.Дж., ден Бестен Р. и др. (1995). «Простая процедура получения 1,8-бис(дифенилфосфино)нафталина». Синтетические коммуникации . 25 (11): 1741–1744. дои : 10.1080/00397919508015858 .
- ^ «Нафталиновый шарик от термитов отпугивает насекомых» . Наука/Техника . Новости Би-би-си. 8 апреля 1998 года.
- ^ Дейзи Б.Х., Стробель Г.А., Кастильо У. и др. (ноябрь 2002 г.). «Нафталин, средство от насекомых, производится Muscodor vitigenus , новым эндофитным грибом» . Микробиология . 148 (Часть 11): 3737–41. дои : 10.1099/00221287-148-11-3737 . ПМИД 12427963 .
- ^ «Краткий обзор исследования репеллента опоссумов» . Архивировано из оригинала 28 сентября 2013 года.
- ^ К. Харт; Ю. Мурата; Н. Сугита; и др. (1993). «Использование нафталина в качестве растворителя для селективного образования аддукта Дильса-Альдера C 60 с антраценом в соотношении 1: 1». тетраэдра Буквы 34 (52): 8473–8476. дои : 10.1016/S0040-4039(00)61362-X .
- ^ М.А. Филатов; А.В. Чепраков (2011). «Синтез новых тетрабензо- и тетранафтопорфиринов реакциями присоединения 4,7-дигидроизоиндола». Тетраэдр . 67 (19): 3559–3566. дои : 10.1016/j.tet.2011.01.052 .
- ^ Цифакис, Димитриос; Чарльз, Кристина; Босуэлл, Род (23 сентября 2020 г.). «Нафталин как топливо для холодных газовых двигателей Cubesat» . Границы в физике . 8 : 389. Бибкод : 2020FrP.....8..389T . дои : 10.3389/fphy.2020.00389 . hdl : 1885/229663 .
- ^ «Новая двигательная установка, использующая ключевой ингредиент нафталиновых шариков, может запускать спутники в космос» . Австралийская радиовещательная корпорация . 8 декабря 2021 г. Проверено 11 декабря 2021 г.
- ^ Сантуччи К., Шах Б. (январь 2000 г.). «Связь нафталина с острой гемолитической анемией» . Академия неотложной медицинской помощи . 7 (1): 42–7. дои : 10.1111/j.1553-2712.2000.tb01889.x . ПМИД 10894241 .
- ^ Энциклопедия MedlinePlus : Отравление нафталином.
- ^ «Технические отчеты NTP 410 и 500» . Технические отчеты NTP 410 и 500 доступны на сайте NTP: Long-Term Abstracts & Reports . Архивировано из оригинала 24 октября 2004 года . Проверено 6 марта 2005 г.
- ^ Монографии МАИР по оценке канцерогенных рисков для человека . ISBN 978-92-832-1282-9 . Проверено 25 декабря 2008 г.
{{cite book}}:|work=игнорируется ( помогите ) - ^ Предложение 65. Архивировано 29 июля 2019 г. в Wayback Machine , Управление оценки опасностей для здоровья окружающей среды.
- ^ «Ученые, возможно, разгадали тайну канцерогенных нафталиновых шариков» , Physorg.com , 20 июня 2006 г.
- ^ «Нафталины, освежители воздуха и рак» . Ассоциация гигиены окружающей среды Новой Шотландии . Проверено 24 мая 2013 г.
- ^ «CDC - Карманный справочник NIOSH по химическим опасностям - нафталин» . Cdc.gov . Проверено 6 марта 2022 г.
- ^ «Нафталин» (PDF) . Epa.gov . Архивировано (PDF) из оригинала 14 октября 2016 г. Проверено 6 марта 2022 г.
- ^ Олдерсон, Эндрю (15 ноября 2008 г.). «Святые бананы! Теперь еврократы запрещают нафталин» . Телеграф . Архивировано из оригинала 12 января 2022 г. Проверено 23 ноября 2013 г.
- ^ Грей, Керрина (17 ноября 2013 г.). «Совет предостерег от использования ядовитых нафталиновых шариков» . Ваш местный опекун . Ньюсквест (Лондон) Лтд . Проверено 23 ноября 2012 г.
- ^ Уведомление Управления экономики и торговли Госсовета и Министерства здравоохранения о прекращении производства и продажи нафталиновых таблеток и пропаганде использования камфорной продукции (Гоцзинмаодиао (1993) № 64)
Внешние ссылки [ править ]
- Нафталин — Национальный информационный центр по пестицидам
- Нафталин — Веб-сайт Агентства по охране окружающей среды США по токсичности воздуха
- Нафталин (PIM 363) - в основном из-за токсичности нафталина.
- Нафталин — CDC — Карманный справочник NIOSH по химическим опасностям
- Нафталин в базе данных свойств пестицидов (PPDB)
- . энциклопедия Британская Том. 19 (11-е изд.). 1911. стр. 100-1. 167–168.