Карбодиимид

В органической химии карбодиимид . (систематическое название IUPAC: метандиимин) [1] ) представляет собой функциональную группу с формулой RN=C=NR. На Земле они исключительно синтетические, но в межзвездном пространстве излучению обнаружено родительское соединение HN=C=NH по его мазерному . [2]
Хорошо известным карбодиимидом является дициклогексилкарбодиимид , который используется в синтезе пептидов . [3] Диалкилкарбодиимиды стабильны. Некоторые производные диарила имеют тенденцию превращаться в димеры и полимеры при хранении при комнатной температуре, хотя в основном это происходит с карбодиимидами с низкой температурой плавления, которые при комнатной температуре являются жидкостями. [4] Твердые диарилкарбодиимиды более стабильны, но со временем могут медленно гидролизоваться в присутствии воды.
Структура и связь
[ редактировать ]
С точки зрения связывания карбодиимиды изоэлектронны диоксиду углерода . Три основные резонансные структуры описывают карбодиимиды:
- РН=Ц=НР ↔ РН + ≡CN − Р ↔ РН − -C≡N + Р
Ядро N=C=N относительно линейно, а углы CN=C приближаются к 120°. В случае C(NCHPh 2 ) 2 центральный угол N=C=N составляет 170°, а углы CN=C находятся в пределах 1° от 126°. [5] Расстояния C=N короткие, около 120 пм, что характерно для двойных связей. Карбодиимиды хиральны , обладают C 2 -симметрией и, следовательно, аксиальной хиральностью . [6] Однако из-за низкого энергетического барьера, препятствующего вращению молекулы и, следовательно, быстрому превращению ее изомеров, фактическое выделение одного оптического изомера карбодиимида чрезвычайно затруднено. Это было продемонстрировано по крайней мере один раз в случае конформационно ограниченных циклических карбодиимидов; хотя есть и другие сообщения об одноручных аксиально-хиральных карбодиимидах, их достоверность с тех пор была поставлена под сомнение на экспериментальных и вычислительных основаниях. [7] [8]
Исходное соединение, метандиимин (HN=C=NH), представляет таутомер цианамида собой .
Синтез
[ редактировать ]Из тиомочевины и мочевины
[ редактировать ]Классический путь получения карбодиимидов включает дегидросульфуризацию тиомочевины . Типичным реагентом для этого процесса является оксид ртути : [9]
- (R(H)N) 2 CS + HgO → (RN) 2 C + HgS + H 2 O
Эту реакцию часто можно провести, как указано, даже если карбодиимиды реагируют с водой. В некоторых случаях к реакционной смеси добавляют дегидратирующий агент.
Дегидратация N,N'-диалкилмочевины дает карбодиимиды:
- (R(H)N) 2 CO → (RN) 2 C + H 2 O
Пятиокись фосфора [10] и п- толуолсульфонилхлорид использовались в качестве дегидратирующих агентов. [11] [12]
Из изоцианатов
[ редактировать ]Изоцианаты можно превратить в карбодиимиды с потерей углекислого газа: [13] [4]
- 2 РН=С=О → (РН) 2 С + СО 2
Реакция катализируется оксидами фосфина . Эта реакция обратима. [9]
Реакции
[ редактировать ]По сравнению с другими гетероалленами карбодиимиды являются очень слабыми электрофилами и реагируют с нуклеофилами только в присутствии катализаторов, таких как кислоты. [14] Таким способом гуанидины . можно получить [3] Являясь слабыми основаниями, карбодиимиды связываются с кислотами Льюиса, образуя аддукты . [9]
Окисление Моффатта
[ редактировать ]Карбодиимиды — это реагенты для окисления Моффатта — протокола превращения спирта в карбонил (кетон или альдегид) с использованием диметилсульфоксида в качестве окислителя: [15]
- (CH 3 ) 2 SO + (CyN) 2 C + R 2 CHOH → (CH 3 ) 2 S + (CyNH) 2 CO + R 2 C=O
Обычно сульфоксид и диимид используются в избытке. [16] В результате реакции образуются диметилсульфид и мочевина в качестве побочных продуктов.
Связующие агенты
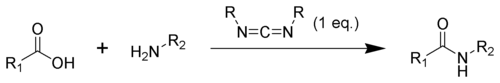
[ редактировать ]В органическом синтезе в качестве дегидратирующих агентов используются соединения, содержащие карбодиимидную функциональность. В частности, их часто используют для преобразования карбоновых кислот в амиды или сложные эфиры . Добавки, такие как N-гидроксибензотриазол или N-гидроксисукцинимид , часто добавляют для увеличения выхода и уменьшения побочных реакций.
Поликарбодиимиды также можно использовать в качестве сшивающих агентов для водных смол, таких как полиуретановые дисперсии или акриловые дисперсии. Здесь поликарбодиимид реагирует с карбоновыми кислотами, функциональные группы которых часто присутствуют в таких водных смолах, с образованием N-ацилмочевины. В результате между полимерными цепями образуются ковалентные связи, благодаря которым они сшиваются. [17] [18]
Путь образования амида
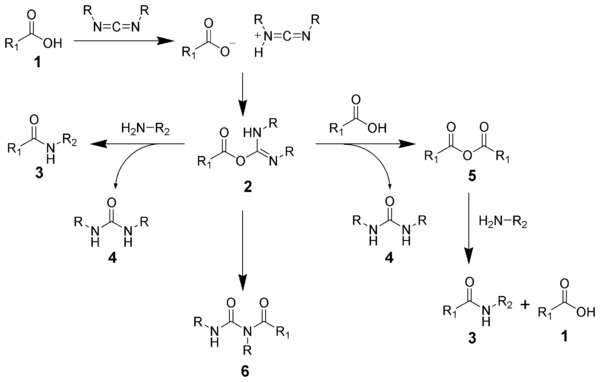
[ редактировать ]Образование амида с использованием карбодиимида является распространенной реакцией, но сопряжено с риском возникновения нескольких побочных реакций. Кислота 1 вступит в реакцию с карбодиимидом с образованием ключевого промежуточного соединения: O-ацилизомочевины 2 , которую можно рассматривать как сложный эфир карбоновой кислоты с активированной уходящей группой. O-ацилизомочевина будет реагировать с аминами с образованием желаемого амида 3 и мочевины 4 .
Возможные реакции O-ацилизомочевины 2 приводят как к желаемым, так и к нежелательным продуктам. O-ацилизомочевина 2 может реагировать с дополнительной карбоновой кислотой 1 с образованием ангидрида кислоты 5 , который может далее реагировать с образованием амида 3 . Основной путь нежелательной реакции включает перегруппировку O-ацилизомочевины 2 в стабильную N - ацилмочевину 6 . Использование растворителей с низкой диэлектрической постоянной, таких как дихлорметан или хлороформ, может свести к минимуму эту побочную реакцию. [19]
Примеры
[ редактировать ]ДКК
[ редактировать ]
DCC (аббревиатура от N , N' - дициклогексилкарбодиимида ) был одним из первых карбодиимидов, разработанных в качестве реагента. Он широко используется для образования амидов и сложных эфиров, особенно для синтеза пептидов твердофазного . DCC приобрел популярность главным образом благодаря своим высокопродуктивным реакциям амидного сочетания и тому факту, что он довольно недорогой.
Однако у DCC есть серьезные недостатки, и его использования часто избегают по нескольким причинам:
- Побочный продукт N , N ' - дициклогексилмочевина в основном удаляется фильтрованием, но следовые примеси удалить бывает трудно. Он несовместим с традиционным твердофазным синтезом пептидов.
- DCC является сильным аллергеном , и повторный контакт с кожей увеличивает вероятность сенсибилизации к этому соединению. Сообщалось о клинических сообщениях о людях, которые не могли войти в помещения, где используются пептидные связующие агенты.
ДВС
[ редактировать ]
В отличие от ДКК, ДИК ( N , N' - диизопропилкарбодиимид ) представляет собой жидкость. Продукт его гидролиза, N,N'-диизопропилмочевина, растворим в органических растворителях.
ЭДГ
[ редактировать ]EDC представляет собой водорастворимый карбодиимидный реагент, используемый для широкого спектра целей. Помимо использования, аналогичного использованию DCC и DIC, он также используется в различных биохимических целях в качестве сшивающего агента или химического зонда .
CMCT или CMC
[ редактировать ]1-циклогексил-(2-морфолиноэтил)карбодиимид метоп- п- толуолсульфонат представляет собой карбодиимид, разработанный для химического исследования структуры РНК в биохимии.
См. также
[ редактировать ]- Диимид серы - аналог серы.
Ссылки
[ редактировать ]- ^ Номенклатура органической химии: рекомендации ИЮПАК и предпочтительные названия 2013 г. (Синяя книга) . Кембридж: Королевское химическое общество . 2014. с. 375. дои : 10.1039/9781849733069-00372 . ISBN 978-0-85404-182-4 .
Название карбодиимид для HN=C=NH сохраняется, но только для общей номенклатуры; никакая замена не допускается. Систематическое название метандиимин является предпочтительным названием ИЮПАК.
- ^ Макгуайр, Бретт А.; Лумис, Райан А.; Чарнесс, Кэмерон М.; Корби, Джоанна Ф.; Блейк, Джеффри А.; Холлис, Ян М.; Ловас, Фрэнк Дж.; Джуэлл, Филип Р.; Ремижан, Энтони Дж. (20 октября 2012 г.). «Межзвездный карбодиимид (HNCNH): новое астрономическое обнаружение в результате исследования GBT Primos с помощью особенностей мазерного излучения» . Астрофизический журнал . 758 (2): L33. arXiv : 1209.1590 . Бибкод : 2012ApJ...758L..33M . дои : 10.1088/2041-8205/758/2/L33 . ISSN 2041-8205 . S2CID 26146516 .
- ^ Jump up to: а б Эндрю Уильямс; Ибрагим Т. Ибрагим (1981). «Карбодиимидная химия: последние достижения». хим. Преподобный . 81 (6): 589–636. дои : 10.1021/cr00046a004 .
- ^ Jump up to: а б Т.В. Кэмпбелл; Джей Джей Монагл (1963). «Дифенилкарбодиимид». Орг. Синтез . 43:31 . дои : 10.15227/orgsyn.043.0031 .
- ^ Jump up to: а б Ирнгартингер, Х.; Йегер, Х.-У. (1978). «Кристаллическая и молекулярная структура двух карбодиимидов: бис (дифенилметил) карбодиимида и бис (п-метоксифенил) карбодиимида». Acta Crystallographica Раздел B: Структурная кристаллография и кристаллохимия . 34 (11): 3262–3265. дои : 10.1107/S0567740878010626 .
- ^ Винсент, AT; Уитли, Пи Джей (1972). «Кристаллическая структура бис -п -нитрофенилкарбодиимида, O 2 N·C 6 H 4 ·N:C:N·C 6 H 4 ·NO 2 ». Журнал Химического общества, Perkin Transactions 2 (11): 1567–1571. дои : 10.1039/P29720001567 .
- ^ Танигучи, Тору; Сузуки, Такахиро; Сато, Харука; Ситибу, Юкацу; Кониси, Кацуаки; Монд, Кенджи (2018). «Получение карбодиимидов с одноручной осевой хиральностью» . Журнал Американского химического общества . 140 (46): 15577–15581. дои : 10.1021/jacs.8b08969 . ПМИД 30398863 . S2CID 53231838 . Проверено 18 августа 2020 г.
- ^ Дамрауэр, Роберт; Лин, Хай; Дамрауэр, Нильс Х. (2014). «Вычислительные исследования карбодиимидных колец» . Журнал органической химии . 79 (9): 3781–3788. дои : 10.1021/jo4026435 . ПМИД 24716711 . Проверено 18 августа 2020 г.
- ^ Jump up to: а б с Фредерик Курцер; К. Дураги-Заде (1967). «Достижения химии карбодиимидов». хим. Преподобный . 67 (2): ee107–152. дои : 10.1021/cr60246a001 . ПМИД 4859920 .
- ^ Анри Ульрих (2008). Химия и технология карбодиимидов . Вайли-ВЧ. ISBN 978-0-470-06510-5 .
- ^ Джон С. Шиэн; Филип А. Круикшанк (1968). «1-Этил-3-(3-диметиламино)пропилкарбодиимид гидрохлорид и метиодид». Орг. Синтез . 48 : 83. дои : 10.15227/orgsyn.048.0083 .
- ^ Арнаб К. Майти; Скай Фортье; Леонель Григо; Алехандро Х. Метта-Маганья (2014). «Синтез «сверхобъемного» гуанидината, обладающего расширяемым координационным карманом». Неорг. Хим . 53 (15): 8155–8164. дои : 10.1021/ic501219q . ПМИД 25029088 .
- ^ Монагл, Джей-Джей (1962). «Карбодиимиды. III. Превращение изоцианатов в карбодиимиды. Каталитические исследования». Дж. Орг. хим. 27 (11): 3851–3855. дои : 10.1021/jo01058a022 .
- ^ Ли, Чжэнь; Майер, Роберт Дж.; Офиал, Армин Р.; Майр, Герберт (27 апреля 2020 г.). «От карбодиимидов к диоксиду углерода: количественная оценка электрофильной активности гетероалленов». Журнал Американского химического общества . 142 (18): 8383–8402. дои : 10.1021/jacs.0c01960 . ПМИД 32338511 . S2CID 216557447 .
- ^ Тидвелл, Т.Т. (1990). «Окисление спиртов активированным диметилсульфоксидом и родственные реакции: обновленная информация». Синтез . 1990 (10): 857–870. дои : 10.1055/s-1990-27036 .
- ^ Джон Г. Моффат (1967). «Холан-24-ал». Орг. Синтез . 47:25 . дои : 10.15227/orgsyn.047.0025 .
- ^ Хессельманс, LCJ; Дерксен, Эй Джей; ван ден Гурберг, JAM (2006). «Поликарбодиимидные сшиватели». Прогресс в области органических покрытий . 55 (2): 142–148. doi : 10.1016/j.porgcoat.2005.08.011 . ISSN 0300-9440 .
- ^ Постумус, В.; Дерксен, Эй Джей; ван ден Гурберг, JAM; Хессельманс, LCJ (2007). «Сшивание поликарбодиимидами». Прогресс в области органических покрытий . 58 (2–3): 231–236. doi : 10.1016/j.porgcoat.2006.09.031 . ISSN 0300-9440 .
- ^ Хотан Мохарради (2010). Соединение веществ, содержащих первичный амин, с гиалуроновой кислотой посредством карбодиимид-опосредованного амидирования (Диссертация). Уппсальский университет. ISSN 1650-8297 .
