Гуанидин
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Гуанидин [1] | |||
| Другие имена Иминометандиамин | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| 506044 | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Лекарственный Банк | |||
| Информационная карта ECHA | 100.003.656 | ||
| Номер ЕС |
| ||
| 100679 | |||
| МеШ | Гуанидин | ||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| Ч 5 Н 3 | |||
| Молярная масса | 59.072 g·mol −1 | ||
| Температура плавления | 50 ° С (122 ° F; 323 К) | ||
| войти P | −1.251 | ||
| Конъюгатная кислота | Гуанидиний | ||
| Термохимия | |||
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | −57 – −55 кДж моль −1 | ||
Стандартная энтальпия горение (Δ c H ⦵ 298 ) | −1,0511 – −1,0531 МДж моль −1 | ||
| Фармакология | |||
| Фармакокинетика : | |||
| 7–8 часов | |||
| Опасности | |||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза ) | 475 мг/кг (перорально, крыса) [2] | ||
| Родственные соединения | |||
Родственные соединения | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
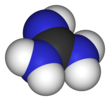
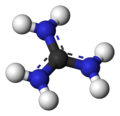
Гуанидин представляет собой соединение формулы HNC(NH 2 ) 2 . Это бесцветное твердое вещество, растворяющееся в полярных растворителях. Это прочная основа , которая используется при производстве пластмасс и взрывчатых веществ . Он обнаруживается в моче преимущественно у пациентов с почечной недостаточностью. [3] Гуанидиновый фрагмент также появляется в более крупных органических молекулах, в том числе в боковой цепи аргинина .
Структура
[ редактировать ]Гуанидин можно рассматривать как азотистый аналог угольной кислоты . То есть группа C=O в угольной кислоте заменяется группой C=NH, а каждый OH заменяется группой NH.
2 группа. [4] Во многом таким же образом изобутен можно рассматривать как аналог углерода. Подробный кристаллографический анализ гуанидина был выяснен через 148 лет после его первого синтеза, несмотря на простоту молекулы. [5] В 2013 году с помощью монокристаллической нейтронографии были точно определены положения атомов водорода и параметры их смещения. [6]
Производство
[ редактировать ]Гуанидин можно получить из природных источников. Впервые он был выделен в 1861 году Адольфом Штрекером путем окислительной деградации ароматического природного продукта, гуанина , выделенного из перуанского гуано . [7] [8]
Лабораторный метод получения гуанидина заключается в щадящем (180-190 °С) термическом разложении сухого роданида аммония в безводных условиях:
- 3 NH 4 SCN → 2 CH 5 N 3 + H 2 S + CS 2
Коммерческий путь включает двухэтапный процесс, начинающийся с реакции дициандиамида с аммония солями . Благодаря посредничеству бигуанидина на этой стадии аммонолиза образуются соли катиона гуанидиния (см. Ниже). На втором этапе соль обрабатывают основанием, например метоксидом натрия . [7]
Соли изотиурония (S-алкилированные тиомочевины ) реагируют с аминами с образованием солей гуанидиния : [9]
- РНХ 2 + [СН 3 СК(NH 2 ) 2 ] + Х − → [RN(H)C(NH 2 ) 2 ] + Х − + СН 3 Ш
Образующиеся ионы гуанидиния часто можно депротонировать с образованием гуанидина. Этот подход иногда называют синтезом Ратке в честь его первооткрывателя. после Бернхарда Ратке [10] [11]
Химия
[ редактировать ]Катион гуанидиния
[ редактировать ]Сопряженная кислота называется гуанидиния катионом ( C(NH
2 ) +
3 ). Этот плоский симметричный ион состоит из трех аминогрупп , каждая из которых связана с центральным атомом углерода ковалентной связью порядка 4/3. Это очень стабильный катион +1 в водном растворе благодаря эффективной резонансной стабилизации заряда и эффективной сольватации молекулами воды. В результате его p K aH составляет 13,6. [12] (p K b 0,4) означает, что гуанидин является очень сильным основанием в воде; в нейтральной воде он существует почти исключительно в виде гуанидиния. В связи с этим большинство производных гуанидина представляют собой соли, содержащие сопряженную кислоту.
- канонические формы
Тестирование на гуанидин
[ редактировать ]Гуанидин можно избирательно обнаружить с помощью натриевой 1,2-нафтохинон-4-сульфоновой кислоты ( реагент Фолина ) и подкисленной мочевины. [13]
Использование
[ редактировать ]Промышленность
[ редактировать ]Основной солью, представляющей коммерческий интерес, является нитрат [C( NH
2 ) 3 ] НЕТ
3 . Он используется в качестве топлива, например, в подушках безопасности .
Лекарство
[ редактировать ]Со времен Средневековья в Европе гуанидин использовался для лечения диабета в качестве активного антигипергликемического ингредиента французской сирени . Из-за его долгосрочной гепатотоксичности дальнейшие исследования по контролю уровня сахара в крови были приостановлены сначала после открытия инсулина. Более поздняя разработка нетоксичных, безопасных бигуанидов привела к появлению давно используемого препарата первой линии для контроля диабета метформина , представленного в Европе в 1950-х годах и в США в 1995 году и теперь назначаемого более чем 17 миллионам пациентов в год в США. [14] [15]
Гуанидиния хлорид [14] является спорным в настоящее время адъювантом в лечении ботулизма . Недавние исследования показали, что у некоторых значительных групп пациентов не наблюдается улучшения после приема этого препарата. [16]
Биохимия
[ редактировать ]Гуанидин существует в протонированном виде, как гуанидиний, в растворе при физиологическом pH.
Хлорид гуанидина (также известный как гидрохлорид гуанидина) обладает хаотропными свойствами и используется для денатурации белков. Известно, что хлорид гуанидиния денатурирует белки с линейной зависимостью между концентрацией и свободной энергией разворачивания. В водных растворах, содержащих 6 М хлорида гуанидиния, почти все белки теряют всю свою вторичную структуру и превращаются в беспорядочно свернутые пептидные цепи. Тиоцианат гуанидиния также используется из-за его денатурирующего действия на различные биологические образцы.
Недавние исследования показывают, что гуанидиний вырабатывается бактериями как токсичный побочный продукт. Чтобы облегчить токсичность гуанидиния, бактерии разработали класс транспортеров, известных как экспортеры гуанидиния или белки Gdx, которые вытесняют дополнительные количества этого иона за пределы клетки. [17] Белки Gdx обладают высокой селективностью в отношении гуанидиния и монозамещенных гуанидинильных соединений и имеют перекрывающийся набор неканонических субстратов с экспортером лекарственного средства EmrE. [18]
Другой
[ редактировать ]Гидроксид гуанидиния является активным ингредиентом некоторых релаксантов для волос , не содержащих щелочи .
Производные гуанидина
[ редактировать ]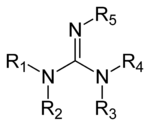
Гуанидины представляют собой группу органических соединений , имеющих общую функциональную группу и общую структуру (R
1 Р
2N )(Р
3 Р
4 Н)С=Н-Р
5 . Центральной связью в этой группе является имин , и группа структурно связана с амидинами и мочевинами. Примерами гуанидинов являются аргинин , триазабициклодецен , сакситоксин и креатин .
Галегин представляет собой изоамиленгуанидин . [19]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 . Королевское химическое общество . п. 883. дои : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ^ «Гуанидина гидрохлорид» . ХимИДплюс . Национальная медицинская библиотека . Архивировано из оригинала 12 августа 2014 г. Проверено 10 августа 2014 г.
- ^ Савинок Дж., Доборн Дж.К. (1975). «Концентрация в плазме и выведение с мочой производных гуанидина у здоровых людей и пациентов с почечной недостаточностью». Клиническая и экспериментальная фармакология и физиология . 2 (1): 1–15. дои : 10.1111/j.1440-1681.1975.tb02368.x . ПМИД 1126056 . S2CID 41794868 .
- ^ Гёбель М., Клапотке Т.М. (август 2007 г.). «Первая структурная характеристика гуанидина, HN=C(NH(2))(2)». Химические коммуникации . 43 (30): 3180–3182. дои : 10.1039/B705100J . ПМИД 17653381 .
- ^ Ямада Т., Лю Х, Энглерт У., Ямане Х., Дронсковски Р. (июнь 2009 г.). «Наконец-то достигнута твердотельная структура свободного основания гуанидина». Химия: Европейский журнал . 15 (23): 5651–5655. дои : 10.1002/chem.200900508 . ПМИД 19388036 .
- ^ Савински П.К., Мевен М., Энглерт У., Дронсковский Р. (2013). «Монокристаллическое нейтронографическое исследование на гуанидине, CN 3 H 5 » . Рост и дизайн кристаллов . 13 (4): 1730–5. дои : 10.1021/cg400054k .
- ^ Перейти обратно: а б Гютнер Т., Мерченк Б., Шульц Б. «Гуанидин и производные». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a12_545.pub2 . ISBN 978-3527306732 .
- ^ Носилки А (1861 г.). «Исследования химических взаимоотношений между гуанином, ксантином, теобромином, кофеином и креатинином» . Анна Либиха. Хим . 118 (2): 151–177. дои : 10.1002/jlac.18611180203 . Архивировано из оригинала 16 июля 2021 г. Проверено 02 июля 2019 г.
- ^ Палмер, Дэвид К. (2001). « S -Метилизотиомочевина». Энциклопедия реагентов для органического синтеза E-EROS . дои : 10.1002/047084289X.rm199s . ISBN 0471936235 .
- ^ «Генрих Бернхард Ратке. (1840-1923)» . Отчеты Немецкого химического общества (серии A и B) . 57 (9): А83–А92. 8 октября 1924 г. doi : 10.1002/cber.19240570929 .
- ^ Ратке, Б. (июль 1881 г.). «О производных и составе сернистого мочевины» . Отчеты Немецкого химического общества . 14 (2): 1774–1780. дои : 10.1002/cber.18810140247 .
- ^ Перрин Д.Д. (1972). Константы диссоциации органических оснований в водном растворе (Под ред.). Лондон: Баттервортс.
- ^ Салливан М.Х. (1 октября 1935 г.). «Колориметрический тест на гуанидин». Труды Общества экспериментальной биологии и медицины . 33 (1): 106–108. дои : 10.3181/00379727-33-8270C . ISSN 0037-9727 . S2CID 88290359 .
- ^ Перейти обратно: а б Бласлов К., Наранджа Ф.С., Круляц И., Ренар ИП (декабрь 2018 г.). «Подход к лечению диабета 2 типа: прошлое, настоящее и будущее» . Всемирный журнал диабета . 9 (12): 209–219. дои : 10.4239/wjd.v9.i12.209 . ПМК 6304295 . ПМИД 30588282 .
- ^ «Топ-300 2019 года» . clincalc.com . Архивировано из оригинала 12 февраля 2021 г. Проверено 17 февраля 2022 г.
- ^ Брук I (2001). Детские анаэробные инфекции: диагностика и лечение (3-е изд.). Тейлор и Фрэнсис. п. 529. ИСБН 0824741862 .
- ^ Кермани А.А., Макдональд CB, Гундепуди Р., Стокбридж РБ (март 2018 г.). «Экспорт гуанидиния — основная функция транспортеров семейства SMR» . Труды Национальной академии наук Соединенных Штатов Америки . 115 (12): 3060–3065. Бибкод : 2018PNAS..115.3060K . дои : 10.1073/pnas.1719187115 . ПМК 5866581 . ПМИД 29507227 .
- ^ Кермани А.А., Макдональд С.Б., Бурата О.Е., Бен Кофф Б., Коиде А., Денбаум Е. и др. (ноябрь 2020 г.). «Структурная основа беспорядочных связей у небольших переносчиков множественной лекарственной устойчивости» . Природные коммуникации . 11 (1): 6064. Бибкод : 2020NatCo..11.6064K . дои : 10.1038/s41467-020-19820-8 . ПМЦ 7695847 . ПМИД 33247110 .
- ^ Уиттерс, Лос-Анджелес (октябрь 2001 г.). «Цветение французской сирени» . Журнал клинических исследований . 108 (8): 1105–1107. дои : 10.1172/JCI14178 . ПМК 209536 . ПМИД 11602616 .