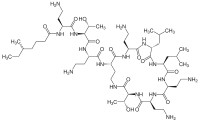
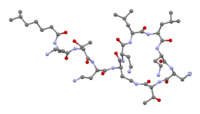
Колистин
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Ксилистин, Coly-Mycin M, Colobreathe и другие. |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а682860 |
| Данные лицензии |
|
| Маршруты администрация | Местно , внутрь , внутривенно , внутримышечно , ингаляционно. |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | 0% |
| Период полувыведения | 5 часов |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ |
|
| КЕГГ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.012.644 |
| Химические и физические данные | |
| Формула | С 52 Ч 98 Н 16 О 13 |
| Молярная масса | 1 155 .455 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Колистин , также известный как полимиксин Е , представляет собой антибиотик , используемый в качестве крайней меры лечения грамотрицательных инфекций с множественной лекарственной устойчивостью, включая пневмонию . [7] [8] Они могут включать такие бактерии, как Pseudomonas aeruginosa , Klebsiella pneumoniae или Acinetobacter . [9] Он выпускается в двух формах: колистиметат натрия можно вводить в вену , в мышцу или вдыхать, а сульфат колистина в основном наносят на кожу или принимают внутрь. [10] Колистиметат натрия [11] является пролекарством ; его получают реакцией колистина с формальдегидом и бисульфитом натрия, что приводит к присоединению сульфометильной группы к первичным аминам колистина. Колистиметат натрия менее токсичен, чем колистин, при парентеральном введении. В водных растворах подвергается гидролизу с образованием сложной смеси частично сульфометилированных производных, а также колистина. Резистентность к колистину начала проявляться с 2015 года. [12]
Общие побочные эффекты инъекционной формы включают проблемы с почками и неврологические проблемы . [8] Другие серьезные побочные эффекты могут включать анафилаксию , мышечную слабость и Clostridium difficile диарею, связанную с . [8] Ингаляционная форма может привести к сужению бронхиол . [8] Неясно, безопасно ли использование во время беременности для плода. [13] Колистин относится к полимиксинов . классу препаратов [8] Он действует путем разрушения цитоплазматической мембраны , что обычно приводит к гибели бактериальных клеток . [8]
Колистин был открыт в 1947 году, а колистиметат натрия был одобрен для медицинского применения в США в 1970 году. [9] [8] Он входит в Список основных лекарственных средств Всемирной организации здравоохранения . [14] Всемирная организация здравоохранения классифицирует колистин как критически важный для медицины человека препарат. [15] Он доступен в виде непатентованного лекарства . [16] Его получают из бактерий рода Paenibacillus . [10]
Медицинское использование
[ редактировать ]Антибактериальный спектр
[ редактировать ]Колистин эффективен при лечении инфекций, вызванных видами Pseudomonas, Escherichia и Klebsiella . Ниже представлены данные о чувствительности к минимальной ингибирующей концентрации (МИК) для нескольких значимых с медицинской точки зрения микроорганизмов: [17] [18]
- Escherichia coli : 0,12–128 мкг/мл.
- Klebsiella pneumoniae : 0,25–128 мкг/мл.
- Pseudomonas aeruginosa : ≤0,06–16 мкг/мл.
Например, колистин в сочетании с другими препаратами используется для борьбы с P. aeruginosa инфекцией биопленки в легких пациентов с муковисцидозом. [19] Биопленки имеют среду с низким содержанием кислорода под поверхностью, где бактерии метаболически неактивны, и колистин очень эффективен в этой среде. Однако P. aeruginosa обитают в верхних слоях биопленки, где остаются метаболически активными. [20] Это связано с тем, что выжившие толерантные клетки мигрируют к верхней части биопленки через пили и образуют новые агрегаты посредством ощущения кворума . [21]
Способ применения и дозировка
[ редактировать ]Формы
[ редактировать ]Коммерчески доступны две формы колистина: сульфат колистина и колистиметат натрия (метансульфонат натрия колистина, сульфометат натрия колистина). Сульфат колистина является катионным ; колистиметат натрия является анионным . Сульфат колистина стабилен, тогда как колистиметат натрия легко гидролизуется до различных метансульфированных производных. Сульфат колистина и колистиметат натрия выводятся из организма разными путями. В отношении Pseudomonas aeruginosa колистиметат является неактивным пролекарством колистина. Эти два препарата не являются взаимозаменяемыми.
- Колистиметат натрия можно использовать для лечения инфекций, вызванных Pseudomonas aeruginosa , у пациентов с муковисцидозом , а недавно он стал использоваться для лечения инфекции Acinetobacter с множественной лекарственной устойчивостью , хотя сообщалось о резистентных формах. [22] [23] Колистиметат натрия также вводили интратекально и внутрижелудочково при вызванном Acinetobacter baumannii и Pseudomonas aeruginosa. менингите и вентрикулите, [24] [25] [26] [27] Некоторые исследования показали, что колистин может быть полезен для лечения инфекций, вызванных устойчивыми к карбапенемам изолятами Acinetobacter baumannii . [23]
- Сульфат колистина можно использовать для лечения кишечных инфекций или для подавления толстой кишки флоры . Сульфат колистина также используется в кремах, порошках и ушных растворах для местного применения.
- Колистин А (полимиксин Е1) и колистин Б (полимиксин Е2) можно очищать индивидуально для исследования и изучения их эффектов и эффективности в виде отдельных соединений.
Дозировка
[ редактировать ]Колистина сульфат и колистиметат натрия можно вводить внутривенно, но дозировка сложна. Различную маркировку парентеральных препаратов метансульфоната колистина в разных частях мира отметили Li et al. [28] Колистиметат натрия производства Xellia (коломицин для инъекций) назначается в международных единицах, тогда как колистиметат натрия производства Parkdale Pharmaceuticals (Coly-Mycin M парентеральный) назначается в миллиграммах колистиновой основы:
- Коломицин 1 000 000 ЕД — колистиметат 80 мг; [29]
- Коли-мицин М 150 мг колистина в основе составляет 360 мг колистиметата или 4 500 000 единиц. [30]
Поскольку колистин был введен в клиническую практику более 50 лет назад, он никогда не подпадал под действие правил, которым подчиняются современные лекарства, и поэтому не существует стандартизированной дозировки колистина и детальных исследований фармакологии или фармакокинетики. Поэтому оптимальная дозировка колистина при большинстве инфекций неизвестна. Рекомендуемая внутривенная доза коломицина составляет от 1 до 2 миллионов единиц три раза в день для пациентов с массой тела 60 кг и более с нормальной функцией почек. Рекомендуемая доза Coly-Mycin составляет от 2,5 до 5 мг/кг основания колистина в день, что эквивалентно 6–12 мг/кг колистиметата натрия в день. Таким образом, для мужчины весом 60 кг рекомендуемая доза Коломицина составляет от 240 до 480 мг колистиметата натрия, тогда как рекомендуемая доза Коли-Мицина составляет от 360 до 720 мг колистиметата натрия. Аналогично, рекомендуемая «максимальная» доза для каждого препарата различна (480 мг для Коломицина и 720 мг для Коли-Мицина). В каждой стране существуют разные дженерики колистина, а рекомендуемая доза зависит от производителя. Полное отсутствие какого-либо регулирования или стандартизации дозы затрудняет внутривенное дозирование колистина для врача. [ нужна ссылка ]
Колистин использовался в сочетании с рифампицином ; существуют доказательства синергизма in vitro , [31] [32] и эта комбинация успешно использовалась у пациентов. [33] Имеются также данные in vitro о синергизме колистиметата натрия, применяемого в сочетании с другими антисинегнойными антибиотиками. [34]
Аэрозоль колистиметата натрия (Промиксин; Коломицин для инъекций) используется для лечения легочных инфекций, особенно при муковисцидозе. В Великобритании рекомендуемая доза для взрослых составляет 1–2 миллиона единиц (80–160 мг) колистиметата, распыляемого через распылитель, два раза в день. [35] [29] Распыленный колистин также использовался для уменьшения тяжелых обострений у пациентов с хронической обструктивной болезнью легких и инфекцией Pseudomonas aeruginosa . [36]
Сопротивление
[ редактировать ]Резистентность к колистину встречается редко, но была описана. По состоянию на 2017 год [update], не существует единого мнения о том, как определять устойчивость к колистину. Французское общество микробиологии использует пороговую величину МИК на уровне 2 мг/л, тогда как Британское общество антимикробной химиотерапии устанавливает пороговую величину МИК на уровне 4 мг/л или менее как чувствительную и 8 мг/л или более как резистентную. . В США не установлены стандарты описания чувствительности к колистину.
Первым известным геном устойчивости к колистину в плазмиде , который можно передавать между бактериальными штаммами, является mcr-1 . Он был обнаружен в 2011 году в Китае на свиноферме, где регулярно используется колистин, и стал широко известен в ноябре 2015 года. [37] [38] Наличие этого плазмидного гена было подтверждено с декабря 2015 года в Юго-Восточной Азии, ряде европейских стран, [39] и США. [40] Он обнаружен в некоторых штаммах бактерий Paenibacillus Polymyxa . [ нужна ссылка ]
Индия сообщила о первом подробном исследовании устойчивости к колистину, в ходе которого были выявлены 13 инфекций, устойчивых к колистину, зарегистрированных за 18 месяцев. Они пришли к выводу, что инфекции, устойчивые к лекарствам, особенно те, которые находятся в кровотоке, имеют более высокую смертность. Еще несколько случаев были зарегистрированы в других индийских больницах. [41] [42] Хотя устойчивость к полимиксинам обычно составляет менее 10%, она чаще встречается в странах Средиземноморья и Юго-Восточной Азии (Корея и Сингапур), где показатели устойчивости к колистину растут. [43] Устойчивая к колистину кишечная палочка была выявлена в США в мае 2016 года. [44]
Недавний обзор, проведенный с 2016 по 2021 год, показал, что E. coli является доминирующим видом, несущим гены mcr. Плазмидно-опосредованная устойчивость к колистину также присуща другим видам, несущим другие гены, устойчивые к антибиотикам. Появление гена mcr-9 весьма примечательно. [45]
Использование колистина для лечения инфекций Acinetobacter baumannii привело к развитию устойчивых штаммов бактерий. У них также развилась устойчивость к противомикробным соединениям LL-37 и лизоциму , вырабатываемым иммунной системой человека. Эта перекрестная устойчивость вызвана мутациями усиления функции гена pmrB , который контролирует экспрессию липида А-фосфоэтаноламинтрансфераз (аналогично mcr-1 ), расположенных на бактериальной хромосоме. [46] Аналогичные результаты были получены с mcr-1- положительной E. coli , которая стала лучше выживать в условиях смеси животных антимикробных пептидов in vitro и более эффективно убивать инфицированных гусениц. [47]
Не вся устойчивость к колистину и некоторым другим антибиотикам обусловлена наличием генов устойчивости. [48] Гетерорезистентность – явление, при котором очевидно генетически идентичные микробы проявляют определенный диапазон устойчивости к антибиотикам. [49] наблюдается у некоторых видов Enterobacter по крайней мере с 2016 г. [48] и наблюдался у некоторых штаммов Klebsiella pneumoniae в 2017–2018 гг. [50] В ряде случаев это явление имеет значительные клинические последствия. [50]
По своей сути устойчивый
[ редактировать ]- Бруцелла
- Буркхолдерия цепасия
- Хризеобактерия индологенес
- Эдвардсиэлла
- Элизабеткингия менингосептика
- Francesella tularensis spp.
- Грамотрицательные кокки
- Хеликобактер пилори
- Моракселла катаралис
- виды Морганеллы.
- Neisseria gonorrhoeae и Neisseria meningitidis
- Протей
- Провиденс
- Серратия
- Некоторые штаммы Stenotropomonasmaltophilia. [51]
Переменное сопротивление
[ редактировать ]Побочные реакции
[ редактировать ]Основными проявлениями токсичности, описанными при внутривенном лечении, являются нефротоксичность (поражение почек) и нейротоксичность (повреждение нервов). [52] [53] [54] [55] но это может отражать назначенные очень высокие дозы, которые намного превышают дозы, рекомендованные в настоящее время любым производителем, и для которых не было сделано никаких корректировок с учетом ранее существовавшего заболевания почек. Нейро- и нефротоксические эффекты носят преходящий характер и исчезают после прекращения терапии или снижения дозы. [56]
При дозе 160 мг колистиметата внутривенно каждые восемь часов наблюдается очень незначительная нефротоксичность. [57] [58] Действительно, колистин, по-видимому, обладает меньшей токсичностью, чем аминогликозиды , которые впоследствии заменили его, и его использовали в течение длительных периодов времени до шести месяцев без каких-либо побочных эффектов. [59] Нефротоксичность, вызванная колистином, особенно вероятна у пациентов с гипоальбуминемией. [60]
Основной токсичностью, описанной при лечении аэрозолями, является бронхоспазм . [61] которые можно лечить или предотвратить с помощью агонистов β2-адренергических рецепторов, таких как сальбутамол. [62] или следуя протоколу десенсибилизации. [63]
Механизм действия
[ редактировать ]Колистин представляет собой поликатионный пептид, имеющий как гидрофильные , так и липофильные фрагменты . [64] Эти катионные области взаимодействуют с внешней мембраной бактерий , вытесняя бактериальные противоионы магния и кальция в липополисахариде . [ нужна ссылка ] Гидрофобные и гидрофильные области взаимодействуют с цитоплазматической мембраной подобно детергенту, солюбилизируя мембрану в водной среде. [ нужна ссылка ] Этот эффект является бактерицидным даже в изомолярной среде. [ нужна ссылка ]
Колистин связывается с липополисахаридами и фосфолипидами внешней клеточной мембраны грамотрицательных бактерий. Он конкурентно вытесняет двухвалентные катионы (Ca 2+ и мг 2+ ) от фосфатных групп мембранных липидов, что приводит к разрушению наружной клеточной мембраны, вытеканию внутриклеточного содержимого и гибели бактерий.
Фармакокинетика
[ редактировать ]В желудочно-кишечном тракте не происходит клинически полезного всасывания колистина. Поэтому при системной инфекции колистин необходимо вводить инъекционно.Колистиметат выводится почками, а колистин выводится непочечными механизмами, которые еще не изучены. [65] [66]
История
[ редактировать ]Колистин был впервые выделен в Японии в 1949 г. Ю. Коямой из колбы с ферментирующейся Bacillus Polymyxa var. колистинус , [67] и стал доступен для клинического использования в 1959 году. [68]
Колистиметат натрия, менее токсичный пролекарство, стал доступен для инъекций в 1959 году. В 1980-х годах использование полимиксина было широко прекращено из-за нефро- и нейротоксичности. Поскольку в 1990-х годах бактерии с множественной лекарственной устойчивостью стали более распространенными, колистин начал рассматриваться как экстренное решение, несмотря на его токсичность. [69]
Колистин также использовался в сельском хозяйстве, особенно в Китае, с 1980-х годов. В 2015 году производство сельскохозяйственной продукции в Китае превысило 2700 тонн. В 2016 году Китай запретил использование колистина для стимулирования роста животноводства. [70]
Биосинтез
[ редактировать ]Биосинтез колистина требует использования трех аминокислот: треонина , лейцина и 2,4-диаминомасляной кислоты. Линейная форма колистина синтезируется до циклизации. Биосинтез нерибосомальных пептидов начинается с загрузки модуля и последующего добавления каждой последующей аминокислоты. Последующие аминокислоты добавляются с помощью домена аденилирования (А), домена белка-носителя пептидила (PCP), домена эпимеризации (Е) и домена конденсации (С). Циклизация осуществляется тиоэстеразой . [71] Первый шаг — связать загрузочный домен, 6-метилгептановую кислоту, с доменами A и PCP. Теперь с доменами C, A и PCP, связанными с 2,4-диаминомасляной кислотой. Это продолжается с каждой аминокислотой до тех пор, пока линейная пептидная цепь не будет завершена. Последний модуль будет иметь тиоэстеразу для завершения циклизации и образования продукта колистина.

Ссылки
[ редактировать ]- ^ «База данных лекарственных средств» . Здоровье Канады . 25 апреля 2012 года . Проверено 13 января 2022 г.
- ^ «Colobreathe 1 662 500 МЕ, порошок для ингаляций, твердые капсулы – краткая характеристика продукта (SmPC)» . (эмс) . Проверено 16 ноября 2020 г.
- ^ «Коломицин 1 миллион международных единиц (МЕ) Порошок для приготовления раствора для инъекций, инфузий или ингаляций – Краткое описание характеристик продукта (SmPC)» . (эмс) . 27 мая 2020 г. Проверено 16 ноября 2020 г.
- ^ «Промиксин, 1 миллион международных единиц (МЕ), порошок для раствора для небулайзера – краткие характеристики продукта (SmPC)» . (эмс) . 23 сентября 2020 г. Проверено 16 ноября 2020 г.
- ^ «Инъекция Coly-Mycin M-колистиметата» . ДейлиМед . 3 декабря 2018 года . Проверено 16 ноября 2020 г.
- ^ «Коло-дыхание ЭПАР» . Европейское агентство по лекарственным средствам . 17 сентября 2018 года . Проверено 16 ноября 2020 г.
- ^ Пог Дж. М., Ортвайн Дж. К., Кэй К. С. (апрель 2017 г.). «Клинические соображения по оптимальному использованию полимиксинов: акцент на выборе и дозировке агентов» . Клиническая микробиология и инфекции . 23 (4): 229–233. дои : 10.1016/j.cmi.2017.02.023 . ПМИД 28238870 .
- ^ Jump up to: а б с д и ж г «Монография по колистиметату натрия для специалистов» . Наркотики.com . Проверено 6 ноября 2019 г.
- ^ Jump up to: а б Фалагас М.Э., Грамматикос А.П., Михалопулос А. (октябрь 2008 г.). «Потенциал антибиотиков старого поколения для удовлетворения текущей потребности в новых антибиотиках». Экспертный обзор противоинфекционной терапии . 6 (5): 593–600. дои : 10.1586/14787210.6.5.593 . ПМИД 18847400 . S2CID 13158593 .
- ^ Jump up to: а б Беннетт Дж. Э., Долин Р., Блазер М. Дж., Манделл Г. Л. (2009). Электронная книга Манделла, Дугласа и Беннета «Принципы и практика инфекционных заболеваний» . Elsevier Науки о здоровье. п. 469. ИСБН 9781437720600 .
- ^ Берген П.Дж., Ли Дж., Рейнер С.Р., Nation RL (июнь 2006 г.). «Метансульфонат колистина является неактивным пролекарством колистина против Pseudomonas aeruginosa» . Антимикробные средства и химиотерапия . 50 (6): 1953–1958. дои : 10.1128/AAC.00035-06 . ПМК 1479097 . ПМИД 16723551 .
- ^ Хасман Х., Хаммерум А.М., Хансен Ф., Хендриксен Р.С., Олесен Б., Агерсё Ю. и др. (10 декабря 2015 г.). «Обнаружение mcr-1, кодирующего плазмидно-опосредованные устойчивые к колистину изоляты Escherichia coli из инфекции кровотока человека и импортированного куриного мяса, Дания, 2015 г.» . Евронаблюдение . 20 (49): 30085. doi : 10.2807/1560-7917.ES.2015.20.49.30085 . ПМИД 26676364 .
- ^ «Использование колистиметата (Coly Mycin M) во время беременности» . Наркотики.com . Проверено 11 ноября 2019 г.
- ^ Всемирная организация здравоохранения (2019). Модельный список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г. Женева: Всемирная организация здравоохранения. hdl : 10665/325771 . ВОЗ/MVP/EMP/IAU/2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ Всемирная организация здравоохранения (2019). Критически важные противомикробные препараты для медицины человека (6-е пересмотренное изд.). Женева: Всемирная организация здравоохранения. hdl : 10665/312266 . ISBN 9789241515528 .
- ^ Британский национальный формуляр: BNF 76 (76-е изд.). Фармацевтическая пресса. 2018. с. 547. ИСБН 9780857113382 .
- ^ «Полимиксин Е (колистин) – База знаний по антимикробному индексу – ТОКУ-Э» . Архивировано из оригинала 28 мая 2016 года . Проверено 28 мая 2016 г.
- ^ «Колистина сульфат, данные о чувствительности USP и минимальной ингибирующей концентрации (MIC)» (PDF) . 3 марта 2016 г. Архивировано (PDF) из оригинала 4 марта 2016 г. Проверено 10 февраля 2014 г.
- ^ Херрманн Г., Ян Л., Ву Х., Сонг З., Ван Х., Хойби Н. и др. (ноябрь 2010 г.). «Комбинации колистин-тобрамицин превосходят монотерапию в отношении уничтожения биопленки Pseudomonas aeruginosa» . Журнал инфекционных болезней . 202 (10): 1585–1592. дои : 10.1086/656788 . ПМИД 20942647 .
- ^ Памп С.Дж., Йермансен М., Йохансен Х.К., Толкер-Нильсен Т. (апрель 2008 г.). «Толерантность к антимикробному пептиду колистину в биопленках Pseudomonas aeruginosa связана с метаболически активными клетками и зависит от генов pmr и mexAB-oprM» . Молекулярная микробиология . 68 (1): 223–240. дои : 10.1111/j.1365-2958.2008.06152.x . ПМИД 18312276 . S2CID 44556845 .
- ^ Чуа С.Л., Ям Дж.К., Хао П., Адав С.С., Салидо М.М., Лю Ю. и др. (февраль 2016 г.). «Селективное мечение и уничтожение толерантных к антибиотикам популяций бактерий в биопленках Pseudomonas aeruginosa» . Природные коммуникации . 7 : 10750. Бибкод : 2016NatCo...710750C . дои : 10.1038/ncomms10750 . ПМЦ 4762895 . ПМИД 26892159 .
- ^ Рейс А.О., Луз Д.А., Тогним MC, Садер Х.С., Гейлс AC (август 2003 г.). «Изоляты Acinetobacter spp., устойчивые к полимиксину: что дальше?» . Новые инфекционные заболевания . 9 (8): 1025–1027. дои : 10.3201/eid0908.030052 . ПМК 3020604 . ПМИД 12971377 .
- ^ Jump up to: а б Таунер К.Дж. (2008). «Молекулярные основы устойчивости к антибиотикам у Acinetobacter spp.» . Молекулярная биология ацинетобактера . Кайстер Академик Пресс. ISBN 978-0-306-43902-5 . Архивировано из оригинала 7 февраля 2012 г.
- ^ Бенифла М., Цукер Г., Коэн А., Алкан М. (июль 2004 г.). «Успешное лечение Acinetobacter менингита интратекальным полимиксином Е» . Журнал антимикробной химиотерапии . 54 (1): 290–292. дои : 10.1093/jac/dkh289 . ПМИД 15190037 .
- ^ Ягмур Р., Эсен Ф (2006). «Интратекальный колистин для лечения вентрикулита, вызванного Pseudomonas aeruginosa: отчет о случае с успешным исходом» . Критическая помощь . 10 (6): 428. дои : 10.1186/cc5088 . ПМЦ 1794456 . ПМИД 17214907 .
- ^ Мотауаккил С., Чарра Б., Хачими А., Неджми Х., Бенслама А., Эльмдагри Н. и др. (октябрь 2006 г.). «Колистин и рифампицин в лечении внутрибольничных инфекций, вызванных мультирезистентными Acinetobacter baumannii». Журнал инфекции . 53 (4): 274–278. дои : 10.1016/j.jinf.2005.11.019 . ПМИД 16442632 .
- ^ Каракитсос Д., Парамитиоту Е., Самонис Г., Карабинис А. (ноябрь 2006 г.). «Является ли внутрижелудочковый колистин эффективным и безопасным средством лечения послеоперационного вентрикулита в отделении интенсивной терапии?». Acta Anaesthesiologica Scandinavica . 50 (10): 1309–1310. дои : 10.1111/j.1399-6576.2006.01126.x . ПМИД 17067336 . S2CID 25679033 .
- ^ Ли Дж., Нэйшн Р.Л., Тернидж Дж.Д., Милн Р.В., Култхард К., Рейнер С.Р., Патерсон Д.Л. (сентябрь 2006 г.). «Колистин: новый антибиотик для лечения грамотрицательных бактериальных инфекций с множественной лекарственной устойчивостью». «Ланцет». Инфекционные болезни . 6 (9): 589–601. дои : 10.1016/s1473-3099(06)70580-1 . ПМИД 16931410 .
- ^ Jump up to: а б «Коломицин для инъекций» . Краткое описание характеристик продукта . электронный справочник лекарственных средств (eMC). 18 мая 2016 года. Архивировано из оригинала 16 июля 2017 года . Проверено 3 июня 2017 г.
- ^ «КОМИТЕТ ПО ВЕТЕРИНАРНЫМ ЛЕКАРСТВЕННЫМ ПРОДУКТАМ: КОЛИСТИН: КРАТКИЙ ОТЧЕТ (2)» (PDF) . Европейское агентство лекарственных средств. Январь 2002 г. Архивировано из оригинала (PDF) 18 июля 2006 г. NB. База колистина имеет назначенную эффективность 30 000 МЕ/мг.
- ^ Ахмед Н., Уолгрен Н.Г. (2003). «Эффекты снижения артериального давления в острой фазе инфарктов тотального переднего кровообращения и других подтипов инсульта». Цереброваскулярные заболевания . 15 (4): 235–243. дои : 10.1159/000069498 . ПМИД 12686786 . S2CID 12205902 .
- ^ Хогг Г.М., Барр Дж.Г., Уэбб Ч.С. (апрель 1998 г.). «Активность комбинации колистина и рифампицина in vitro против штаммов Acinetobacter baumannii с множественной лекарственной устойчивостью» . Журнал антимикробной химиотерапии . 41 (4): 494–495. дои : 10.1093/jac/41.4.494 . ПМИД 9598783 .
- ^ Петросильо Н., Чинелло П., Пройетти М.Ф., Чеккини Л., Масала М., Франки С. и др. (август 2005 г.). «Комбинированная терапия колистином и рифампицином при инфекциях Acinetobacter baumannii, устойчивых к карбапенемам: клинический исход и побочные эффекты» . Клиническая микробиология и инфекции . 11 (8): 682–683. дои : 10.1111/j.1469-0691.2005.01198.x . ПМИД 16008625 .
- ^ Ринн С., Вуттон М., Боукер К.Е., Алан Холт Х., Ривз Д.С. (январь 1999 г.). «Оценка in vitro антипсевдомонадного противомикробного взаимодействия колистина с другими антибиотиками» . Клиническая микробиология и инфекции . 5 (1): 32–36. дои : 10.1111/j.1469-0691.1999.tb00095.x . ПМИД 11856210 .
- ^ «Промиксин, 1 миллион международных единиц (МЕ), порошок для раствора для небулайзера» . Информационная брошюра для пациентов . электронный справочник лекарственных средств (eMC). 12 января 2016 г. Архивировано из оригинала 16 июля 2017 г.
- ^ Бругера-Авила Н., Марин А., Гарсия-Олив И., Радуа Дж., Прат С., Хиль М., Руис-Мансано Дж. (2017). «Эффективность лечения небулайзерным колистином у больных ХОБЛ» . Международный журнал хронической обструктивной болезни легких . 12 : 2909–2915. дои : 10.2147/COPD.S138428 . ПМЦ 5634377 . ПМИД 29042767 .
- ^ Лю Ю., Ван Ю., Уолш Т.Р., Йи Л.С., Чжан Р., Спенсер Дж. и др. (февраль 2016 г.). «Появление плазмидно-опосредованного механизма устойчивости к колистину MCR-1 у животных и людей в Китае: микробиологическое и молекулярно-биологическое исследование». «Ланцет». Инфекционные болезни . 16 (2): 161–168. дои : 10.1016/S1473-3099(15)00424-7 . ПМИД 26603172 .
- ^ Чжан С. «Сопротивление антибиотикам последней инстанции незаметно распространяется» . Атлантика . Архивировано из оригинала 13 января 2017 г. Проверено 12 января 2017 г.
- ^ Маккенна М (03 декабря 2015 г.). «Apocalypse Pig Redux: Сопротивление последней инстанции в Европе» . Феномены . Архивировано из оригинала 28 мая 2016 года . Проверено 28 мая 2016 г.
- ^ «Первое открытие в Соединенных Штатах устойчивости к колистину при инфекции человека, вызванной кишечной палочкой» . www.sciencedaily.com . Архивировано из оригинала 27 мая 2016 г. Проверено 27 мая 2016 г.
- ^ «Появление устойчивости к лекарствам Pan среди грамотрицательных бактерий! Первая серия случаев из Индии» . Декабрь 2014.
- ^ «Новое беспокойство: в Индии появляется устойчивость к «последнему антибиотику» . Таймс оф Индия . 28 декабря 2014 г. Архивировано из оригинала 31 декабря 2014 г.
- ^ Бялваи АЗ, Самади Кафил Х (апрель 2015 г.). «Колистин, механизмы и распространенность резистентности» . Текущие медицинские исследования и мнения . 31 (4): 707–721. дои : 10.1185/03007995.2015.1018989 . ПМИД 25697677 . S2CID 33476061 .
- ^ «Обнаружение первого гена mcr-1 у бактерий E. coli, обнаруженного у человека в США» . cdc.gov . Министерство здравоохранения и социальных служб США. 31 мая 2016 г. Архивировано из оригинала 11 июля 2016 г. Проверено 6 июля 2016 г.
- ^ Хацидимитриу М, Каввада А, Каввадас Д, Кириазиди М.А., Мелетис Г, Хацопулу Ф, Хацидимитриу Д (декабрь 2021 г.). «Гены mcr, обеспечивающие устойчивость энтеробактерий к колистину? Пятилетний обзор» . Акта Медика Академика . 50 (3): 365–371. дои : 10.5644/ama2006-124.355 . ПМИД 35164512 . S2CID 246826086 .
- ^ Нэпьер Б.А., Берд Э.М., Сатола С.В., Кейгл С.М., Рэй С.М., МакГанн П. и др. (май 2013 г.). «Клиническое использование колистина вызывает перекрестную устойчивость к противомикробным препаратам у Acinetobacter baumannii» . мБио . 4 (3): e00021–e00013. дои : 10.1128/mBio.00021-13 . ПМЦ 3663567 . ПМИД 23695834 .
- ^ Джангир П.К., Огунлана Л., Сили П., Чиккели М., Шоу Л.П., Стивенс Э.Дж. и др. (апрель 2023 г.). «Эволюция устойчивости к колистину увеличивает устойчивость бактерий к антимикробным пептидам хозяина и вирулентность» . электронная жизнь . 12 : е84395. doi : 10.7554/eLife.84395 . ПМЦ 10129329 . ПМИД 37094804 .
- ^ Jump up to: а б Маккей Б. (6 марта 2018 г.). «Обнаружена распространенная «супербактерия», маскирующая устойчивость к сильнодействующему антибиотику» . wsj.com . Уолл Стрит Джорнал. Архивировано из оригинала 3 апреля 2018 г. Проверено 1 ноября 2018 г.
- ^ Эль-Халфави О.М., Вальвано М.А. (январь 2015 г.). «Антимикробная гетерорезистентность: новая область, нуждающаяся в ясности» . Обзоры клинической микробиологии . 28 (1): 191–207. дои : 10.1128/CMR.00058-14 . ПМЦ 4284305 . ПМИД 25567227 .
- ^ Jump up to: а б Группа VI, Сатола С.В., Берд Э.М., Фарли М.М., Джейкоб Дж.Т., Вайс Д.С. (март 2018 г.). «Устойчивая к карбапенемам Klebsiella pneumoniae , проявляющая клинически необнаруженную гетерорезистентность к колистину, приводит к неудаче лечения на мышиной модели инфекции» . мБио . 9 (2): e02448–17. дои : 10.1128/mBio.02448-17 . ПМЦ 5844991 . ПМИД 29511071 .
- ^ Марку Н., Апостолакос Х., Кумудиу С., Афанасиу М., Куцуку А., Аламанос И., Грегоракос Л. (октябрь 2003 г.). «Внутривенный колистин в лечении сепсиса, вызванного мультирезистентными грамотрицательными палочками, у пациентов в критическом состоянии» . Критическая помощь . 7 (5): С78–Р83. дои : 10.1186/cc2358 . ПМК 270720 . ПМИД 12974973 .
- ^ Волински Э., Хайнс JD (апрель 1962 г.). «Нейротоксическое и нефротоксическое действие колистина у пациентов с заболеваниями почек». Медицинский журнал Новой Англии . 266 (15): 759–762. дои : 10.1056/NEJM196204122661505 . ПМИД 14008070 .
- ^ Кох-Везер Дж., Сидель В.В., Федерман Э.Б., Канарек П., Файнер Д.С., Итон А.Е. (июнь 1970 г.). «Побочные эффекты колистиметата натрия. Проявления и скорость специфических реакций на протяжении 317 курсов терапии». Анналы внутренней медицины . 72 (6): 857–868. дои : 10.7326/0003-4819-72-6-857 . ПМИД 5448745 .
- ^ Ледсон М.Дж., Галлахер М.Дж., Каупертуэйт С., Конвери Р.П., Уолшоу М.Дж. (сентябрь 1998 г.). «Четырехлетний опыт внутривенного введения коломицина во взрослом отделении муковисцидоза» . Европейский респираторный журнал . 12 (3): 592–594. дои : 10.1183/09031936.98.12030592 . ПМИД 9762785 .
- ^ Ли Дж., Нэйшн Р.Л., Милн Р.В., Тернидж Дж.Д., Култхард К. (январь 2005 г.). «Оценка колистина как средства против полирезистентных грамотрицательных бактерий». Международный журнал противомикробных средств . 25 (1): 11–25. дои : 10.1016/j.ijantimicag.2004.10.001 . ПМИД 15620821 .
- ^ Берингер П. (ноябрь 2001 г.). «Клиническое применение колистина у больных муковисцидозом». Современное мнение в области легочной медицины . 7 (6): 434–440. дои : 10.1097/00063198-200111000-00013 . ПМИД 11706322 . S2CID 38084953 .
- ^ Конвей С.П., Этерингтон С., Мандей Дж., Голдман М.Х., Стронг Дж.Дж., Вуттон М. (ноябрь 2000 г.). «Безопасность и переносимость болюсного внутривенного введения колистина при острых респираторных обострениях у взрослых с муковисцидозом». Анналы фармакотерапии . 34 (11): 1238–1242. дои : 10.1345/aph.19370 . ПМИД 11098334 . S2CID 42625124 .
- ^ Литтлвуд Дж.М., Кох С., Ламберт П.А., Хойби Н., Элборн Дж.С., Конвей С.П. и др. (июль 2000 г.). «Десятилетний обзор коломицина» . Респираторная медицина . 94 (7): 632–640. дои : 10.1053/rmed.2000.0834 . ПМИД 10926333 .
- ^ Штейн А., Рауль Д. (октябрь 2002 г.). «Колистин: противомикробное средство XXI века?» . Клинические инфекционные болезни . 35 (7): 901–902. дои : 10.1086/342570 . ПМИД 12228836 .
- ^ Джакоббе Д.Р., ди Маси А., Лебофф Л., Дель Боно В., Росси М., Каппиелло Д. и др. (август 2018 г.). «Гипоальбуминемия как предиктор острого повреждения почек во время лечения колистином» . Научные отчеты . 8 (1): 11968. Бибкод : 2018NatSR...811968G . дои : 10.1038/s41598-018-30361-5 . ПМК 6086859 . ПМИД 30097635 .
- ^ Мэддисон Дж., Додд М., Уэбб А.К. (февраль 1994 г.). «Распыленный колистин вызывает чувство стеснения в груди у взрослых с муковисцидозом» . Респираторная медицина . 88 (2): 145–147. дои : 10.1016/0954-6111(94)90028-0 . ПМИД 8146414 .
- ^ Камин В., Швабе А., Кремер И. (декабрь 2006 г.). «Растворы для ингаляций: какие разрешено смешивать? Физико-химическая совместимость растворов лекарственных средств в небулайзерах» . Журнал муковисцидоза . 5 (4): 205–213. дои : 10.1016/j.jcf.2006.03.007 . ПМИД 16678502 .
- ^ Домингес-Ортега Дж., Мантейга Э., Абад-Шиллинг С., Юрецке М.А., Санчес-Рубио Дж., Кинделан С. (2007). «Индуцированная толерантность к распыляемому колистину после тяжелой реакции на препарат». Журнал исследовательской аллергологии и клинической иммунологии . 17 (1): 59–61. ПМИД 17323867 .
- ^ Ли Дж., Нэйшн Р.Л., Тернидж Дж.Д., Милн Р.В., Култхард К., Рейнер С.Р., Патерсон Д.Л. (сентябрь 2006 г.). «Колистин: новый антибиотик для лечения грамотрицательных бактериальных инфекций с множественной лекарственной устойчивостью». «Ланцет». Инфекционные болезни . 6 (9): 589–601. дои : 10.1016/S1473-3099(06)70580-1 . ПМИД 16931410 .
- ^ Ли Дж., Милн Р.В., Нэйшн Р.Л., Тернидж Дж.Д., Смитон Т.С., Култхард К. (май 2004 г.). «Фармакокинетика метансульфоната колистина и колистина у крыс после внутривенного введения метансульфоната колистина» . Журнал антимикробной химиотерапии . 53 (5): 837–840. дои : 10.1093/jac/dkh167 . ПМИД 15044428 .
- ^ Ли Дж., Милн Р.В., Нэйшн Р.Л., Тернидж Дж.Д., Смитон Т.С., Култхард К. (май 2003 г.). «Использование высокоэффективной жидкостной хроматографии для изучения фармакокинетики сульфата колистина у крыс после внутривенного введения» . Антимикробные средства и химиотерапия . 47 (5): 1766–1770. doi : 10.1128/AAC.47.5.1766-1770.2003 . ПМЦ 153303 . ПМИД 12709357 .
- ^ Кояма Ю., Куросаса А., Цучия А., Такакута К. (1950). «Новый антибиотик колистин, продуцируемый спорообразующими почвенными бактериями». Дж. Антибиот (Токио) . 3 .
- ^ Макларен Дж., Спелман Д. (22 ноября 2022 г.). Хоппер, округ Колумбия, Холл К.К. (ред.). «Колистин: Обзор» . До настоящего времени . Уолтерс Клювер. Архивировано из оригинала 31 мая 2016 г. Проверено 6 июня 2016 г.
- ^ Фалагас М.Э., Касиаку С.К. (май 2005 г.). «Колистин: возрождение полимиксинов для лечения грамотрицательных бактериальных инфекций с множественной лекарственной устойчивостью» . Клинические инфекционные болезни . 40 (9): 1333–1341. дои : 10.1086/429323 . ПМИД 15825037 . S2CID 21679015 .
- ^ Шенмейкерс К. (21 октября 2020 г.). «Как Китай заставляет своих фермеров отказаться от привычки к антибиотикам» . Природа . Проверено 2 августа 2021 г.
- ^ Дьюик ПМ (2009). Лекарственные натуральные продукты (Третье изд.). Джон Уайли и сыновья.
Дальнейшее чтение
[ редактировать ]- Рирдон С. (декабрь 2015 г.). «Распространение гена устойчивости к антибиотикам еще не означает бактериального апокалипсиса — пока» . Природа . дои : 10.1038/nature.2015.19037 .
Внешние ссылки
[ редактировать ]- «Страница тем колистина (библиография)» . Science.gov.