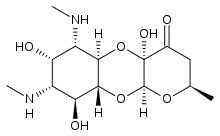
Спектиномицин
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Тробицин |
| Другие имена | (2 R ,4a R ,5a R ,6 S ,7 S ,8 R ,9 S ,9a R ,10a S )-4а,7,9-тригидрокси-2-метил-6,8- бис (метиламино)декагидро -4 H -пирано[2,3- b ][1,4]бензодиоксин-4-он , SPT/SPE/SC/SP [1] |
| AHFS / Drugs.com | Монография |
| Маршруты администрация | В |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.015.374 |
| Химические и физические данные | |
| Формула | С 14 Н 24 Н 2 О 7 |
| Молярная масса | 332.353 g·mol −1 |
| 3D model ( JSmol ) | |
| Температура плавления | От 184 до 194 ° C (от 363 до 381 ° F) |
| | |
Спектиномицин под торговой маркой Тробицин , продаваемый , среди прочего, , является антибиотиком, полезным для лечения инфекций, вызванных гонореей . [2] Его вводят путем инъекции в мышцу. [2]
Общие побочные эффекты включают боль в области инъекции, сыпь, тошноту, лихорадку и проблемы со сном. [2] тяжелые аллергические реакции . Иногда могут возникать [2] Как правило, его можно безопасно использовать во время беременности. [2] Его могут использовать те, у кого аллергия на пенициллин или цефалоспорины . [2] Он относится к классу препаратов аминоциклита и действует, останавливая выработку белка некоторыми бактериями. [2]
Спектиномицин был открыт в 1961 году. [3] Он входит в Список основных лекарственных средств Всемирной организации здравоохранения . [4] Он недоступен в Соединенных Штатах для использования человеком. [2] Он производится из бактерии Streptomyces spectabilis . [2]
Медицинское использование
[ редактировать ]Его вводят внутримышечными инъекциями для лечения гонореи , особенно у пациентов с аллергией на пенициллины .
Этот антибиотик больше не доступен в Соединенных Штатах для использования человеком, но все еще доступен для использования в ветеринарии.
Побочные эффекты
[ редактировать ]Побочные эффекты включают зуд , озноб , боль в животе и красную сыпь .
Механизм действия
[ редактировать ]Спектиномицин связывается с 30S- субъединицей бактериальной рибосомы и прерывает синтез белка.Одна из форм устойчивости возникла в 16S рибосомальной РНК Pasteurella multocida . [5]
Биосинтетический механизм
[ редактировать ]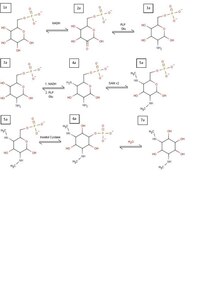
Биосинтез спектиномицина начинается аналогично всем аминогликозидам, с образования инозитолового кольца. Разница заключается в начальной модификации, которая образует инозитоловое кольцо спектиномицина. Процесс начинается с глюкозо-6-фосфата (1а), который окисляется НАД. + с образованием кетона по C2 (2a). Этот кетон затем превращается в первичную аминогруппу посредством пиридоксальфосфата (PLP) и трансаминирования глутамина (3a). Этот процесс снова повторяется у C4 с образованием второго первичного амина (4a). Как только эти два амина присутствуют, глюкозное кольцо готово к метилированию с помощью двух молекул S-аденозилметионина (5а). Благодаря этому метилированию глюкозное кольцо наконец готово к превращению в инозитоловое кольцо с помощью инозитолциклазы (6a). Затем его можно гидролизовать, чтобы избавиться от фосфатной группы, что делает инозитоловое кольцо необходимым для спектиномицина (7a).
Пока все это происходит, происходит альтернативный путь создания функциональной группы сахара из аналогичного исходного продукта. В этом пути глюкозо-1-фосфат в качестве исходного продукта используется (1b). Она преобразуется в TDP-глюкозу посредством TDP-синтазы (2b). Затем у глюкозы TDP гидроксил удаляется из C6 с помощью фермента гидратазы (3b), который затем восстанавливается через НАДН в C4, создавая новый продукт (4b). При наличии этого кетона PLP и глютамин могут преобразовать его в первичный амин (5b), который затем можно удалить с помощью деаминазы (6b). Это преобразование в 6b также сопровождается двойным восстановлением по C4 и C3 за счет еще двух молекул НАДН, давая конечный продукт, необходимый для образования аминогликозида. При этом продукты 7a и 6b могут соединяться, удаляя функциональную группу TDP и соединяясь с молекулой сахара с образованием аминогликозида спектиномицина. [6]
Природа
[ редактировать ]Он относится к классу аминоциклитов , тесно связанных с аминогликозидами . Спектиномицин промышленно производят путем ферментации бактерии Streptomyces spectabilis . Спектиномицин вырабатывается в природе многими организмами, включая цианобактерии и различные виды растений. [ нужна ссылка ] Он присутствует в геноме или пластоме многих пластид в виде оперона spc , длина которого обычно составляет от двух до десяти генов. Разница в размерах может быть связана с устранением устаревших генов или взятием на себя его функции ядерными генами. Спектиномицин в основном вырабатывается организмами в качестве защитного механизма от хищников.
История
[ редактировать ]Спектиномицин был открыт в 1961 году. [3] Перебои с поставками произошли в 2001 году. [7]
Ссылки
[ редактировать ]- ^ «Список сокращений антибиотиков» . Проверено 22 июня 2023 г.
- ^ Jump up to: а б с д и ж г час я «Спектиномицина гидрохлорид» . Американское общество фармацевтов системы здравоохранения. Архивировано из оригинала 24 сентября 2015 г. Проверено 6 сентября 2015 г.
- ^ Jump up to: а б Учебник по разработке и открытию лекарств, четвертое издание . ЦРК Пресс. 2009. с. 438. ИСБН 9781439882405 . Архивировано из оригинала 3 октября 2015 г.
- ^ Всемирная организация здравоохранения (2019). Модельный список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г. Женева: Всемирная организация здравоохранения. hdl : 10665/325771 . ВОЗ/MVP/EMP/IAU/2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ Керенберг С., Шварц С. (июнь 2007 г.). «Мутации в 16S рРНК и рибосомальном белке S5, связанные с высоким уровнем устойчивости к спектиномицину у Pasteurella multocida» . Антимикроб. Агенты Чематер . 51 (6): 2244–6. дои : 10.1128/AAC.00229-07 . ЧВК 1891365 . ПМИД 17371823 .
- ^ Дьюик, Пол М. (4 февраля 2009 г.). Лекарственные натуральные продукты: биосинтетический подход, 3-е издание . Интернет-библиотека Wiley: Wiley. стр. 485–508 . дои : 10.1002/9780470742761 . ISBN 9780470741689 .
- ^ «От Центров по контролю и профилактике заболеваний. Обновленная информация о доступности спектиномицина в США» . ДЖАМА . 286 (11): 1308–9. Сентябрь 2001 г. doi : 10.1001/jama.286.11.1308 . ПМИД 11575327 .