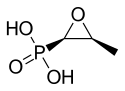
Фосфомицин
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Монурил, Монурол, Ивозфо и другие. |
| Другие имена | Фосфомицин, фосфономицин, фосфомицин трометамин |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а697008 |
| Данные лицензии |
|
| Маршруты администрация | Внутривенно , Через рот |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | 30–37% (внутрь, фосфомицин трометамин ); варьируется в зависимости от приема пищи |
| Связывание с белками | ноль |
| Метаболизм | ноль |
| Период полувыведения | 5,7 часов (в среднем) |
| Экскреция | Почка , без изменений |
| Идентификаторы | |
| Номер CAS |
|
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.041.315 |
| Химические и физические данные | |
| Формула | C3H7O4C3H7O4P |
| Молярная масса | 138.059 g·mol −1 |
| 3D model ( JSmol ) | |
| Температура плавления | 94 ° С (201 ° F) |
| (проверять) | |
Фосфомицин под торговой маркой Монурол , продаваемый , среди прочего, , представляет собой антибиотик, в основном используемый для лечения инфекций нижних мочевых путей . [7] Он не показан при инфекциях почек . [7] Иногда его применяют при инфекциях простаты . [7] Обычно его принимают внутрь. [7]
Общие побочные эффекты включают диарею, тошноту, головную боль и вагинальные дрожжевые инфекции . [7] Тяжелые побочные эффекты могут включать анафилаксию и Clostridioides difficile диарею, связанную с . [7] Хотя использование во время беременности не было признано вредным, такое использование не рекомендуется. [8] Однократная доза при грудном вскармливании кажется безопасной. [8] Фосфомицин действует, вмешиваясь в производство бактериальной клеточной стенки . [7]
Фосфомицин был открыт в 1969 году и одобрен для медицинского применения в США в 1996 году. [ глобализировать ] . [7] [9] Он входит в Список основных лекарственных средств Всемирной организации здравоохранения . [10] Всемирная организация здравоохранения классифицирует фосфомицин как критически важный для медицины человека. [11] Он доступен в виде непатентованного лекарства . [12] Первоначально он вырабатывался некоторыми видами Streptomyces , хотя сейчас его производят химическим путем. [9]
Медицинское использование
[ редактировать ]Фосфомицин используется для лечения инфекций мочевого пузыря , где его обычно назначают однократно перорально. [13]
Пероральный фосфомицин не рекомендуется детям до 12 лет. [14]
Были предложены дополнительные варианты использования. [15] Глобальная проблема развития устойчивости к противомикробным препаратам в последнее время привела к возобновлению интереса к их использованию. [16]
Фосфомицин можно использовать в качестве эффективного лечения как ИМП, так и осложненных ИМП, включая острый пиелонефрит. Стандартной схемой лечения осложненных ИМП является пероральный прием дозы 3 г один раз каждые 48 или 72 часа, всего 3 дозы, или доза 6 г каждые 8 часов в течение 7–14 дней при внутривенном введении фосфомицина. [17]
Внутривенный фосфомицин все чаще используется для лечения инфекций, вызванных бактериями с множественной лекарственной устойчивостью , в основном в качестве препарата-партнера, чтобы избежать возникновения резистентности и воспользоваться его синергетической активностью с некоторыми другими противомикробными препаратами. Суточная доза для взрослых обычно составляет от 12 до 24 граммов. [18] При введении непрерывной инфузии назначают ударную дозу фосфомицина 8 г с последующей суточной дозой 16 г или 24 г. Непрерывная инфузия рекомендуется пациентам с нормальной функцией почек. [19]
Бактериальная чувствительность
[ редактировать ]Молекула фосфомицина имеет эпоксидное или оксирановое кольцо, которое сильно натянуто и, следовательно, очень реакционноспособно. [ нужна ссылка ]
Фосфомицин обладает широкой антибактериальной активностью в отношении как грамположительных, так и грамотрицательных патогенов, а также полезной активностью в отношении E. faecalis , E. coli и различных грамотрицательных микроорганизмов, таких как Citrobacter и Proteus . Учитывая большую активность в среде с низким pH и преобладающую экскрецию в активной форме с мочой, фосфомицин нашел применение для профилактики и лечения ИМП, вызванных этими уропатогенами. Следует отметить, что активность против S. saprophyticus , Klebsiella и Enterobacter варьируется и должна подтверждаться тестированием минимальной ингибирующей концентрации . Активность в отношении патогенов, продуцирующих β-лактамазы расширенного спектра действия , продуцирующих ESBL , особенно E. coli , варьируется от хорошей до отличной, поскольку препарат не подвержен проблемам перекрестной резистентности.Существующие клинические данные подтверждают возможность использования препарата при неосложненных ИМП, вызванных чувствительными микроорганизмами. Однако порог чувствительности 64 мг/л не следует применять при системных инфекциях. [ нужна ссылка ]
Сопротивление
[ редактировать ]Развитие бактериальной резистентности на фоне терапии является частым явлением и делает фосфомицин непригодным для длительной терапии тяжелых инфекций. Мутации, которые инактивируют несущественный переносчик глицерофосфата, делают бактерии устойчивыми к фосфомицину. [20] [21] [22] Тем не менее, фосфомицин можно использовать для лечения бактериемии MRSA. [23]
Назначение фосфомицина вместе хотя бы с другим активным препаратом снижает риск развития бактериальной резистентности. Фосфомицин действует синергично со многими другими антибиотиками, включая аминогликозиды, карбапенемы, цефалоспорины, даптомицин и оритаванцин. [18] [24]
Ферменты, придающие устойчивость к фосфомицину, также были идентифицированы и кодируются как на хромосомах , так и на плазмидах . [25]
Три родственных фермента устойчивости к фосфомицину (названные FosA, FosB и FosX) являются членами суперсемейства глиоксалаз . Эти ферменты действуют путем нуклеофильной атаки углерода 1 фосфомицина, что открывает эпоксидное кольцо и делает препарат неэффективным. [ нужна ссылка ]
Ферменты различаются по идентичности нуклеофила, используемого в реакции: глутатион для FosA, бациллитиол для FosB, [26] [27] и вода для FosX. [25]
Как правило, ферменты FosA и FosX продуцируются грамотрицательными бактериями, тогда как FosB продуцируются грамположительными бактериями. [25]
FosC использует АТФ и добавляет фосфатную группу к фосфомицину, тем самым изменяя его свойства и делая препарат неэффективным. [28]
Побочные эффекты
[ редактировать ]Препарат хорошо переносится и имеет низкую частоту вредных побочных эффектов. [13]
Механизм действия
[ редактировать ]Несмотря на свое название (оканчивающееся на -омицин), фосфомицин не является макролидом , а принадлежит к новому классу фосфоновых антибиотиков. Фосфомицин обладает бактерицидным действием и ингибирует биогенез клеточной стенки бактерий, инактивируя фермент UDP -N -ацетилглюкозамин-3-енолпирувилтрансферазу , также известный как MurA. [29] Этот фермент катализирует обязательную стадию биосинтеза пептидогликана , а именно связывание фосфоенолпирувата (ФЕП) с 3'-гидроксильной группой УДФ -N -ацетилглюкозамина . Этот пируватный фрагмент обеспечивает линкер, который соединяет гликановую и пептидную части пептидогликана. Фосфомицин представляет собой аналог PEP, который ингибирует MurA путем алкилирования в активном центре остатка цистеина (Cys 115 в ферменте Escherichia coli ). [30] [31]
Фосфомицин проникает в бактериальную клетку через глицерофосфатный транспортер. [32]
История
[ редактировать ]Фосфомицин (первоначально известный как фосфономицин) был открыт совместными усилиями компании Merck and Co. и испанской Compañía Española de Penicilina y Antibióticos (CEPA). Впервые он был выделен путем скрининга бульонных культур Streptomyces fradiae, выделенных из образцов почвы, на способность вызывать образование сферопластов растущими бактериями. Открытие было описано в серии статей, опубликованных в 1969 году. [33] CEPA начала производство фосфомицина в промышленных масштабах в 1971 году на своем предприятии в Аранхуэсе . [34]
Производство
[ редактировать ]Полный кластер генов биосинтеза фосфомицина из Streptomyces fradiae был клонирован и секвенирован, а гетерологичное производство фосфомицина в S. lividans было достигнуто Райаном Вудиером из исследовательских групп Хуйминь Чжао и Уилфреда ван дер Донка . [35]
Крупномасштабное производство фосфомицина достигается путем получения эпоксида цис-пропенилфосфоновой кислоты с получением рацемической смеси фосфомицина. [36]
Ссылки
[ редактировать ]- ^ «Лекарства, отпускаемые по рецепту: регистрация новых химических веществ в Австралии, 2017» . Управление терапевтических товаров (TGA) . 21 июня 2022 года. Архивировано из оригинала 10 апреля 2023 года . Проверено 9 апреля 2023 г.
- ^ «Лекарственные средства, отпускаемые по рецепту, и биологические препараты: годовой обзор TGA за 2017 год» . Управление терапевтических товаров (TGA) . 21 июня 2022 г. Проверено 31 марта 2024 г.
- ^ «Краткое описание нормативного решения – Ивозфо» . Здоровье Канады . 23 октября 2014 г. Архивировано из оригинала 7 июня 2022 г. Проверено 7 июня 2022 г.
- ^ «Монурил 3г, гранулы для приготовления раствора для перорального применения. Краткое описание характеристик продукта (SmPC)» . (эмс) . 1 июня 2021 года. Архивировано из оригинала 8 марта 2022 года . Проверено 7 июня 2022 г.
- ^ «Фомицит 40 мг/мл, порошок для приготовления раствора для инфузий. Краткое описание характеристик продукта (SmPC)» . (эмс) . 11 февраля 2021 года. Архивировано из оригинала 7 июня 2022 года . Проверено 7 июня 2022 г.
- ^ «Монурол-фосфомицин трометамин порошок» . ДейлиМед . 24 октября 2019 года. Архивировано из оригинала 7 июня 2022 года . Проверено 7 июня 2022 г.
- ^ Перейти обратно: а б с д и ж г час «Монография по фосфомицину трометамину для специалистов» . Наркотики.com . Архивировано из оригинала 29 октября 2019 года . Проверено 29 октября 2019 г.
- ^ Перейти обратно: а б «Использование фосфомицина (монурола) во время беременности» . Наркотики.com . Архивировано из оригинала 29 октября 2019 года . Проверено 29 октября 2019 г.
- ^ Перейти обратно: а б Финч Р.Г., Гринвуд Д., Уитли Р.Дж., Норрби С.Р. (2010). Электронная книга «Антибиотики и химиотерапия» . Elsevier Науки о здоровье. п. 259. ИСБН 9780702047657 .
- ^ Всемирная организация здравоохранения (2019). Модельный список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г. Женева: Всемирная организация здравоохранения. hdl : 10665/325771 . ВОЗ/MVP/EMP/IAU/2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ Всемирная организация здравоохранения (2019). Критически важные противомикробные препараты для медицины человека (6-е пересмотренное изд.). Женева: Всемирная организация здравоохранения. hdl : 10665/312266 . ISBN 9789241515528 .
- ^ Британский национальный формуляр: BNF 76 (76-е изд.). Фармацевтическая пресса. 2018. С. 560–561. ISBN 9780857113382 .
- ^ Перейти обратно: а б Патель С.С., Бальфур Дж.А., Брайсон Х.М. (апрель 1997 г.). «Фосфомицин трометамин. Обзор его антибактериальной активности, фармакокинетических свойств и терапевтической эффективности при пероральном применении однократной дозы при острых неосложненных инфекциях нижних мочевых путей». Наркотики . 53 (4): 637–656. дои : 10.2165/00003495-199753040-00007 . ПМИД 9098664 . S2CID 46972404 .
- ^ «МОНУРИЛ САШЕ 3G» . Архивировано из оригинала 28 мая 2014 года . Проверено 26 мая 2014 г.
- ^ Фалагас М.Э., Яннопулу К.П., Коколакис Г.Н., Рафаилидис П.И. (апрель 2008 г.). «Фосфомицин: применение не только при инфекциях мочевыводящих путей и желудочно-кишечного тракта» . Клинические инфекционные болезни . 46 (7): 1069–1077. дои : 10.1086/527442 . ПМИД 18444827 .
- ^ Фалагас М.Э., Грамматикос А.П., Михалопулос А. (октябрь 2008 г.). «Потенциал антибиотиков старого поколения для удовлетворения текущей потребности в новых антибиотиках». Экспертный обзор противоинфекционной терапии . 6 (5): 593–600. дои : 10.1586/14787210.6.5.593 . ПМИД 18847400 . S2CID 13158593 .
- ^ Жанель Г.Г., Жанель М.А., Карловский Ю.А. (28 марта 2020 г.). «Пероральный и внутривенный фосфомицин для лечения осложненных инфекций мочевыводящих путей» . Канадский журнал инфекционных заболеваний и медицинской микробиологии . 2020 . Hindawi Limited: 8513405. doi : 10.1155/2020/8513405 . ПМЦ 7142339 . ПМИД 32300381 .
- ^ Перейти обратно: а б Антонелло Р.М., Принсипи Л., Мараоло А.Е., Виаджи В., Пол Р., Фаббиани М. и др. (август 2020 г.). «Фосфомицин как лекарственный препарат-партнер для лечения системных инфекций. Систематический обзор его синергических свойств на основе исследований in vitro и in vivo» . Антибиотики . 9 (8): 500. doi : 10.3390/antibiotics9080500 . ПМК 7460049 . ПМИД 32785114 .
- ^ Антонелло Р.М., Ди Белла С., Мараоло А.Е., Луццати Р. (июнь 2021 г.). «Фосфомицин при постоянной или длительной инфузии при системных бактериальных инфекциях: систематический обзор предлагаемого режима дозирования на основе исследований in vitro, in vivo и клинических исследований» . Европейский журнал клинической микробиологии и инфекционных заболеваний . 40 (6): 1117–1126. дои : 10.1007/s10096-021-04181-x . ПМЦ 8139892 . ПМИД 33604721 .
- ^ Кахан Ф.М., Кахан Дж.С., Кэссиди П.Дж., Кропп Х. (май 1974 г.). «Механизм действия фосфомицина (фосфономицина)». Анналы Нью-Йоркской академии наук . 235 (1): 364–386. Бибкод : 1974NYASA.235..364K . дои : 10.1111/j.1749-6632.1974.tb43277.x . ПМИД 4605290 . S2CID 33013586 .
- ^ Кастаньеда-Гарсия А., Бласкес Х., Родригес-Рохас А. (апрель 2013 г.). «Молекулярные механизмы и клиническое влияние приобретенной и внутренней устойчивости к фосфомицину» . Антибиотики . 2 (2): 217–236. дои : 10.3390/антибиотики2020217 . ПМЦ 4790336 . ПМИД 27029300 .
- ^ Омори К., Китагава Х., Такада М., Маэда Р., Номура Т., Кубо Ю., Сигэмото Н., Оге Х. (апрель 2024 г.). «Фосфомицин как терапия спасения при персистирующей метициллин-резистентной бактериемии Staphylococcus aureus: серия случаев и обзор литературы». J Заразить химиотерапией . 30 (4): 352–356. дои : 10.1016/j.jiac.2023.10.024 . ПМИД 37922987 .
- ^ Лагатолла К., Мехат Дж.В., Ла Раджионе Р.М., Луццати Р., Ди Белла С. (сентябрь 2022 г.). «Исследование in vitro и in vivo синергизма оритаванцина и фосфомицина против ванкомицин-резистентного Enterococcus faecium » . Антибиотики . 11 (10): 1334. doi : 10.3390/antibiotics11101334 . ПМЦ 9598191 . ПМИД 36289992 .
- ^ Перейти обратно: а б с Ригсби Р.Э., Филлгроув К.Л., Бейхоффер Л.А., Армстронг Р.Н. (2005). «Белки, устойчивые к фосфомицину: связь глутатионтрансфераз и эпоксидгидролаз в суперсемействе металлоферментов» . Глутион [ sic ] трансферазы и гамма-глутамилтранспептидазы . Методы энзимологии. Том. 401. С. 367–379 . дои : 10.1016/S0076-6879(05)01023-2 . ISBN 9780121828066 . ПМИД 16399398 .
- ^ Шарма С.В., Джотивасан В.К., Ньютон Г.Л., Аптон Х., Вакабаяши Дж.И., Кейн М.Г. и др. (июль 2011 г.). «Химический и химиоферментативный синтез бациллитиола: уникального низкомолекулярного тиола среди грамположительных бактерий с низким содержанием G + C». Ангеванде Хеми . 50 (31): 7101–7104. дои : 10.1002/anie.201100196 . ПМИД 21751306 .
- ^ Робертс А.А., Шарма С.В., Странкман А.В., Дюран С.Р., Рават М., Гамильтон С.Дж. (апрель 2013 г.). «Механистические исследования FosB: двухвалентной металлозависимой бациллитиол-S-трансферазы, которая опосредует устойчивость к фосфомицину у Staphylococcus aureus» . Биохимический журнал . 451 (1): 69–79. дои : 10.1042/BJ20121541 . ПМЦ 3960972 . ПМИД 23256780 .
- ^ Гарсиа П., Арка П., Эваристо Суарес Х (июль 1995 г.). «Продукт fosC, гена Pseudomonas syringae, опосредует устойчивость к фосфомицину, используя АТФ в качестве косубстрата» . Антимикробные средства и химиотерапия . 39 (7): 1569–1573. дои : 10.1128/aac.39.7.1569 . ПМЦ 162783 . ПМИД 7492106 .
- ^ Браун Э.Д., Вивас Э.И., Уолш К.Т., Колтер Р. (июль 1995 г.). «MurA (MurZ), фермент, который катализирует первую стадию биосинтеза пептидогликана, необходим для Escherichia coli» . Журнал бактериологии . 177 (14): 4194–4197. дои : 10.1128/jb.177.14.4194-4197.1995 . ПМК 177162 . ПМИД 7608103 .
- ^ Чжу Ю., Ян Ю., Хан Х., Бетци С., Олесен Ш., Марсилио Ф., Шенбрунн Э. (апрель 2012 г.). «Функциональное следствие ковалентной реакции фосфоенолпирувата с УДФ-N-ацетилглюкозамин-1-карбоксивинилтрансферазой (MurA)» . Журнал биологической химии . 287 (16): 12657–12667. дои : 10.1074/jbc.M112.342725 . ПМК 3339971 . ПМИД 22378791 .
- ^ Крекель Ф., Самланд А.К., Машеру П., Амрайн Н., Эванс Дж.Н. (октябрь 2000 г.). «Определение значения pKa C115 в MurA (UDP-N-ацетилглюкозамин енолпирувилтрансфераза) из Enterobacter cloacae». Биохимия . 39 (41): 12671–12677. дои : 10.1021/bi001310x . ПМИД 11027147 .
- ^ Санторо А., Каппелло А.Р., Мадео М., Мартелло Е., Якопетта Д., Дольче В. (декабрь 2011 г.). «Взаимодействие фосфомицина с переносчиком глицерин-3-фосфата Escherichia coli». Biochimica et Biophysical Acta (BBA) – Общие предметы . 1810 (12): 1323–1329. дои : 10.1016/j.bbagen.2011.07.006 . ПМИД 21791237 .
- ^ Сильвер LL (2011). «Рациональные подходы к открытию антибактериальных средств: прегеномный направленный и фенотипический скрининг». В Догерти Т., Пуччи М.Дж. (ред.). Открытие и разработка антибиотиков . Спрингер. п. 46. дои : 10.1007/978-1-4614-1400-1_2 . ISBN 978-1-4614-1400-1 .
- ^ «О нас: Наша история» . Энкрос . Архивировано из оригинала 14 сентября 2011 года.
- ^ Вудиер Р.Д., Шао З., Томас П.М., Келлехер Н.Л., Блоджетт Дж.А., Меткалф В.В. и др. (ноябрь 2006 г.). «Гетерологичное производство фосфомицина и идентификация минимального кластера биосинтетических генов» . Химия и биология . 13 (11): 1171–1182. doi : 10.1016/j.chembiol.2006.09.007 . ПМИД 17113999 .
- ^ Марокко CP, Дэвис EV, Финнелл JE, Nguyen PH, Mateer SC, Ghiviriga I и др. (2011). «Асимметричный синтез (-)-фосфомицина и его транс-(1S,2S)-диастереомера с использованием биокаталитического восстановления в качестве ключевого этапа». Тетраэдр: Асимметрия . 22 (18–19). Эльзевир Б.В.: 1784–1789. дои : 10.1016/j.tetasy.2011.10.009 . ISSN 0957-4166 .