Тедизолид
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Сивекстро |
| Другие имена | ТР-700, торезолид [1] |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а614038 |
| Данные лицензии | |
| Маршруты администрация | Внутрь , внутривенно |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | 91% |
| Связывание с белками | 70–90% |
| Период полувыведения | 12 часов |
| Экскреция | Фекалии |
| Идентификаторы | |
| Номер CAS |
|
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ |
|
| КЕГГ | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.249.430 |
| Химические и физические данные | |
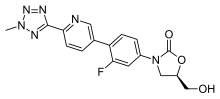
| Формула | С 17 Ч 15 Ф Н 6 О 3 |
| Молярная масса | 370.344 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
Тедизолид , продаваемый под торговой маркой Sivextro, представляет собой антибиотик класса оксазолидинонов . Тедизолид фосфат представляет собой пролекарство фосфатного эфира активного соединения тедизолида. Он был разработан Cubist Pharmaceuticals после приобретения Trius Therapeutics (производитель: Dong-A Pharmaceuticals) и продается для лечения острых бактериальных инфекций кожи и структур кожи (также известных как осложненные инфекции кожи и структур кожи (cSSSI)) . [5] [ нужна медицинская ссылка ]
Наиболее распространенные побочные эффекты включают тошноту (плохое самочувствие), головную боль, диарею и рвоту. [4] Эти побочные эффекты обычно имели легкую или умеренную степень тяжести. [4]
Тедизолид был одобрен для медицинского применения в США в июне 2014 года. [6] [7] и для медицинского использования в Европейском Союзе в марте 2015 года. [4]
Медицинское использование
[ редактировать ]США Тедизолид был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) 20 июня 2014 года с показанием для лечения острых бактериальных инфекций кожи и структур кожи (ABSSSI), вызванных некоторыми чувствительными бактериями, включая Staphylococcus aureus (в том числе устойчивыми к метициллину). штаммы, MRSA и штаммы, чувствительные к метициллину), различные виды Streptococcus ( S. pyogenes , S. agalactiae и группа S. anginosus, включая S. anginosus , S. intermedius и S. constellatus ) и Enterococcus faecalis . [6] [7] [8] [3] второго поколения Тедизолид — производное оксазолидинона , которое в 4–16 раз более эффективно против стафилококков и энтерококков по сравнению с линезолидом . [9] Рекомендуемая доза для лечения составляет 200 мг один раз в день в течение шести дней перорально (с пищей или без) или внутривенно (если пациент старше 18 лет). [3]
В Европейском Союзе тедизолид показан для лечения острых бактериальных инфекций кожи и структур кожи (ABSSSI) у взрослых. [4]
Механизм действия
[ редактировать ]Тедизолид фосфат (TR-701) представляет собой пролекарство, плазмы или кишечника которое активируется фосфатазами до тедизолида (TR-700) после перорального или внутривенного введения препарата. [3] [10] После активации тедизолид проявляет свою бактериостатическую микробную активность посредством ингибирования синтеза белка путем связывания с 50S рибосомальной субъединицей (на акцепторном сайте) бактерий. [3]

Фармакокинетические/фармакодинамические (ФК/ФД) свойства
[ редактировать ]Таблетки Тедизолид имеют пероральную биодоступность >90%. Тедизолид имеет более высокое связывание с белками плазмы (80%), более длительный период полувыведения и больший объем распределения по сравнению с линезолидом. Он главным образом метаболизируется в печени в виде неактивного сульфатного конъюгата (реакция фазы II), без метаболизма ферментами цитохрома Р-450. Менее 20% препарата выводится с мочой в неизмененном виде. Бактерицидная активность тедизолида в отношении VRE и MRSA зависит от времени. Наиболее тесная корреляция между fAUC24/MIC и индексом PK/PD тедизолида против MRSA и VRE. Для достижения 1 log10 уничтожения fAUC24/MIC тедизолида на моделях мышей с нейтропенией и инфекцией бедра, вызванной VRE и MRSA, должна составлять 14,2 и 138,5 соответственно. Постантибиотический эффект тедизолида против VRE и MRSA составляет 2,39 и 0,99 часа соответственно. [11]
Клинические испытания
[ редактировать ]Тедизолид доказал свою эффективность по сравнению с линезолидом в двух исследованиях III фазы, известных как исследования ESTABLISH. [12]
Тедизолид — второй препарат, одобренный FDA в соответствии с новым федеральным законом « Создание стимулов к использованию антибиотиков сейчас» (известным как Закон GAIN). [13] [14] Новые антибиотики, производимые в соответствии с этим новым законом, будут разрабатываться как сертифицированный продукт для лечения инфекционных заболеваний (QIDP), что позволит ускорить проверку FDA и получить дополнительные пять лет эксклюзивности на рынке. [14]
Побочные эффекты
[ редактировать ]Наиболее частыми побочными эффектами, обнаруженными в клинических исследованиях, были тошнота, головная боль, диарея, рвота и головокружение. [3] Также было обнаружено, что тедизолид оказывает гематологическое воздействие (кровь), как показано в исследованиях фазы I , в которых субъекты, получавшие дозы более 6 дней, показали возможное влияние дозы и продолжительности лечения на гематологические параметры. [3] Его безопасность у пациентов со сниженным уровнем лейкоцитов не установлена. [8] Пациенты, принимающие тедизолид, также имеют низкий риск периферической и оптической нейропатии , как и другие представители класса оксазолидинонов. [3]
Ссылки
[ редактировать ]- ^ «Триус растет по мере продвижения вперед антибиотиков» . 31 октября 2011 г.
- ^ «Разрешения на новые лекарства Министерства здравоохранения Канады: основные события 2015 г.» . Здоровье Канады . 4 мая 2016 года . Проверено 7 апреля 2024 г.
- ^ Jump up to: а б с д и ж г час «Сивекстро-тедизолид фосфат таблетка, покрытая пленочной оболочкой. Сивекстро-тедизолид фосфат для инъекций, порошок, лиофилизированный, для приготовления раствора» . ДейлиМед . 22 июня 2020 г. Проверено 24 октября 2020 г.
- ^ Jump up to: а б с д и «Сивэкстро ЭПАР» . Европейское агентство лекарственных средств (EMA) . 17 сентября 2018 года . Проверено 5 июля 2020 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ «Cubist Pharmaceuticals приобретает Trius Therapeutics» . Июль 2013 г. Архивировано из оригинала 2 апреля 2015 г. Проверено 17 марта 2015 г.
- ^ Jump up to: а б «Упаковка одобренного препарата: таблетки Сивекстро (тедизолид фосфат) NDA № 205435» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 24 декабря 1999 года . Проверено 5 июля 2020 г.
- ^ Jump up to: а б «Пакет одобрения препарата: Сивекстро (тедизолид фосфат) для инъекций NDA № 205436» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 24 декабря 1999 года . Проверено 5 июля 2020 г.
- ^ Jump up to: а б «FDA одобрило Sivextro для лечения кожных инфекций» (пресс-релиз). Июнь 2014 г. Архивировано из оригинала 21 января 2017 г. Проверено 16 декабря 2019 г.
- ^ «Тедизолид (TR-701): новый оксазолидинон с повышенной эффективностью» . По состоянию на 16 марта 2015 г.
- ^ Шаадт Р., Суини Д., Шинабаргер Д., Зуренко Г. (август 2009 г.). «Активность in vitro TR-700, активного ингредиента антибактериального пролекарства TR-701, нового оксазолидинонового антибактериального средства» . Антимикробные средства и химиотерапия . 53 (8): 3236–3239. дои : 10.1128/AAC.00228-09 . ПМЦ 2715649 . ПМИД 19528279 .
- ^ Карчионе Д., Интра Дж., Андриани Л., Кампаниле Ф., Гона Ф., Карлетти С. и др. (сентябрь 2023 г.). «Новые противомикробные препараты для лечения грамположительных устойчивых инфекций: комплексное руководство для врачей» . Фармацевтика . 16 (9): 1304. doi : 10.3390/ph16091304 . ПМЦ 10536666 . ПМИД 37765112 .
- ^ «Анализ фазы 3 УСТАНОВЛЕНИЯ испытаний тедизолида по сравнению с линезолидом при острых бактериальных инфекциях кожи и структур кожи» . По состоянию на 16 марта 2015 г.
- ^ «Новая рабочая группа FDA будет поддерживать инновации в разработке антибактериальных препаратов» . Сентябрь 2012.
- ^ Jump up to: а б «Три обнадеживающих шага на пути к новым антибиотикам» . Сентябрь 2014.
Внешние ссылки
[ редактировать ]- «Инъекции тедизолида: информация о лекарствах MedlinePlus» . МедлайнПлюс .