Амидин
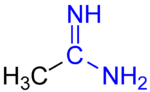
Амидины представляют собой органические соединения с функциональной группой RC(NR)NR 2 , где группы R могут быть одинаковыми или разными. Они представляют собой иминные производные амидов (RC(O)NR 2 ). Простейшим амидином является формамидин HC(=NH)NH 2 .
Примеры амидинов включают:
- ДБУ
- диминазен
- бензамидин
- Пентамидин
- Паранилин
Подготовка
[ редактировать ]Распространенным путем к первичным амидинам является реакция Пиннера . Реакция нитрила со спиртом в присутствии кислоты дает иминоэфир . Обработка полученного соединения аммиаком завершает превращение в амидин. [1] Вместо использования кислоты Бренстеда , кислоты Льюиса такие как трихлорид алюминия, прямому аминированию нитрилов способствуют . [2] Они также образуются путем аминирования имидоилхлорида . [3] Их получают также добавлением литийорганических реагентов к дииминам с последующим протонированием или алкилированием .
диметилформамида Ацеталь реагирует с первичными аминами с образованием амидинов: [4]
- Me 2 NC(H)(OMe) 2 + RNH 2 → Me 2 NC=NHR + 2 MeOH
Кислотно-щелочная химия
[ редактировать ]Амидины гораздо более основные, чем амиды, и являются одними из самых сильных незаряженных/неионизированных оснований. [5] [6]
Протонирование происходит по sp 2 -гибридизированный азот. Это происходит потому, что положительный заряд может делокализоваться на обоих атомах азота. Полученный катионный вид известен как амидиния. ион [7] и обладает одинаковой длиной связи CN.

Приложения
[ редактировать ]Некоторые лекарственные средства или кандидаты в лекарственные средства содержат амидиновые заместители. Примеры включают противопротозойный имидокарб , инсектицид амитраз , антигельминтное средство трибендимидин и ксиламидин , антагонист рецептора 5НТ2А. [8]
Формамидиний (см. ниже) может вступать в реакцию с галогенидом металла с образованием светопоглощающего полупроводникового материала в перовскитных солнечных элементах . Катионы или галогениды формамидиния (FA) могут частично или полностью заменять галогениды метиламмония при формировании поглотительных слоев перовскита в фотоэлектрических устройствах .
Номенклатура
[ редактировать ]Формально амидины представляют собой класс оксокислот . Оксокислота, из которой получают амидин, должна иметь форму R n E(=O)OH, где R представляет собой заместитель . Группа -OH заменяется группой 2 , -NH а группа =O заменяется на = , NR что дает амидинам общую структуру R n E(=NR)NR 2 . [9] [10] [11] Когда исходной оксокислотой является карбоновая кислота , образующийся амидин представляет собой карбоксамидин или карбоксимимидамид ( название ИЮПАК ). Карбоксамидины часто называют просто амидинами, поскольку они являются наиболее часто встречающимся типом амидинов в органической химии .
Производные
[ редактировать ]Катионы формамидиния
[ редактировать ]
Заметным подклассом ионов амидиния являются катионы формамидиния ; которую можно представить химической формулой [R
2N -CH=NR
2 ] +
. депротонирование Их дает стабильные карбены , которые можно представить химической формулой R
2N -C:-NR
2 . [12] [13]
Амидинатные соли
[ редактировать ]
Амидинатная соль имеет общую структуру M + [РНРКНР] − и его можно получить путем реакции карбодиимида с металлоорганическим соединением, таким как метиллитий . [15] Они широко используются в качестве лигандов в металлоорганических комплексах.
См. также
[ редактировать ]- Гуанидины — аналогичная группа соединений, в которой центральный атом углерода связан с тремя атомами азота.
- Имидазолины содержат циклический амидин.
Ссылки
[ редактировать ]- ^ А. В. Докс (1928). «Ацетамидина гидрохлорид». Органические синтезы . 8 : 1. дои : 10.15227/orgsyn.008.0001 .
- ^ « Н -Фенилбензамидин». Органические синтезы . 36 : 64. 1956. doi : 10.15227/orgsyn.036.0064 .
- ^ Артур К. Хонц, ЕС Вагнер (1951). «N,N-Дифенилбензамидин». Органические синтезы . 31 : 48. дои : 10.15227/orgsyn.031.0048 .
- ^ Дэниел А. Дикман; Майкл Боес; Альберт И. Мейерс (1989). «(S)-N,N-Диметил-N'-(1-трет-Бутокси-3-метил-2-бутил)формамидин». Органические синтезы . 67 : 52. дои : 10.15227/orgsyn.067.0052 .
- ^ Рош В.Ф. Улучшение понимания студентами-аптекарями и долгосрочное запоминание кислотно-щелочной химии. Американский журнал фармацевтического образования. 2007;71(6):122.
- ^ Клейден; Гривз; Уоррен (2001). Органическая химия . Издательство Оксфордского университета. п. 202 . ISBN 978-0-19-850346-0 .
- ^ Шредер, Томас; Гамильтон, Эндрю Д., ред. (2005). Функциональные синтетические рецепторы . Вайли-ВЧ. п. 132. ИСБН 3-527-30655-2 .
- ^ Гринхилл, Джон В.; Лю, Пинг (1993). 5 Амидины и гуанидины в медицинской химии . Прогресс медицинской химии. Том. 30. стр. 203–326. дои : 10.1016/S0079-6468(08)70378-3 . ISBN 9780444899897 . ПМИД 7905649 .
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « Амидины ». дои : 10.1351/goldbook.A00267
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « Карбоксамидины ». doi : 10.1351/goldbook.C00851
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « Сульфинамидины ». дои : 10.1351/goldbook.S06107
- ^ Олдер, Роджер В.; Блейк, Майкл Э.; Буфали, Симона; Баттс, Крейг П.; Орпен, А. Гай; Шютц, Ян; Уильямс, Стюарт Дж. (2001). «Получение солей тетраалкилформамидиния и родственных соединений в качестве предшественников стабильных карбенов». Журнал Химического общества, Perkin Transactions 1 (14): 1586–1593. дои : 10.1039/B104110J .
- ^ Эдвард К. Тейлор; Венделл А. Эрхарт; М. Каваниси (1966). «Формамидина ацетат». Органические синтезы . 46:39 . дои : 10.15227/orgsyn.046.0039 .
- ^ Китон, Ричард Дж.; Джаяратне, Кумудини К.; Хеннингсен, Дэвид А.; Котервас, Лиза А.; Сита, Лоуренс Р. (2001). «Резкое усиление активности живой полимеризации Циглера-Натта, опосредованной «экспонированными» инициаторами ацетамидината циркония: изоспецифическая живая полимеризация винилциклогексана». Журнал Американского химического общества . 123 (25): 6197–6198. дои : 10.1021/ja0057326 . ПМИД 11414862 .
- ^ Ульрих, Анри (2007). Химия и технология карбодиимидов . Чичестер, Англия: Джон Уайли и сыновья. ISBN 9780470065105 .