Оксокомплекс переходного металла

Оксокомплекс переходного металла представляет собой координационный комплекс, содержащий оксолиганд . Формально О 2- оксолиганд может быть связан с одним или несколькими металлоцентрами, т.е. он может существовать как концевой или (чаще всего) как мостиковый лиганд (рис. 1). Оксолиганды стабилизируют высокие степени окисления металла. [ 1 ] Они также обнаружены в некоторых металлопротеинах , например, в кофакторах молибдена и во многих железосодержащих ферментах. Одним из первых синтетических соединений, включающих оксо-лиганд, является феррат калия (K 2 FeO 4 ), который, вероятно, был получен Георгом Э. Сталем в 1702 году. [ 2 ]
Реактивность
[ редактировать ]Олирование и кислотно-основные реакции
[ редактировать ]
Распространенной реакцией, которую проявляют металл-оксосоединения, является олатирование , процесс конденсации, который превращает оксиды с низкой молекулярной массой в полимеры со связями MOM. Олирование часто начинается с депротонирования гидроксокомплекса металла. Он является основой минерализации и осаждения оксидов металлов. Для оксидов металлов d0 V V , Нб V , Она V , Мо МЫ , и Вт МЫ В процессе олатирования образуются полиоксометаллаты , большой класс молекулярных оксидов металлов.
Перенос атомов кислорода
[ редактировать ]Оксокомплексы металлов являются промежуточными продуктами во многих реакциях окисления, катализируемых металлами . Перенос атома кислорода — распространенная реакция, представляющая особый интерес в органической химии и биохимии . [ 3 ] Некоторые металл-оксо способны переносить свой оксо-лиганд на органические субстраты. Одним из таких примеров реактивности этого типа является фермент суперсемейства молибденовой оксотрансферазы .
В катализе окисления воды оксокомплексы металлов являются промежуточными продуктами превращения воды в O 2 .
Абстракция атома водорода
[ редактировать ]Переходные металлы-оксо также способны отрывать сильные связи C–H, N–H и O–H. Цитохром P450 содержит высоковалентное оксо-железо, способное отрывать атомы водорода от прочных связей C–H. [ 4 ]
Молекулярные оксиды
[ редактировать ]Некоторые из самых давно известных и наиболее широко используемых оксосоединений представляют собой окислители, такие как перманганат калия (KMnO 4 ) и тетраоксид осмия (OsO 4 ). [ 5 ] Подобные соединения широко используются для превращения алкенов в вицинальные диолы и спиртов в кетоны или карбоновые кислоты. [ 1 ] Более селективные или более мягкие окислительные реагенты включают хлорхромат пиридиния (PCC) и дихромат пиридиния (PDC). [ 1 ] Оксо-формы металлов способны к каталитическому, в том числе асимметричному окислению различных типов. Некоторые металл-оксокомплексы способствуют активации связи CH , превращая углеводороды в спирты. [ 6 ]

Выбор молекулярных оксидов металлов. Слева: ванадилхлорид (d 0 ), оксокарбонил вольфрама (d 2 ), перманганат (д 0 ), [ReO 2 (пиридин) 4 ] + (д 2 ), упрощенный вид соединения I (состояние цитохрома Р450 , d 4 ), и Ir(O)(мезитил) 3 (d 4 ). [ 7 ]
Металлоферменты
[ редактировать ]Железо(IV)-оксо-разновидности
[ редактировать ]
Оксосоединения железа(IV) являются промежуточными продуктами многих биологических окислений:
- Альфа-кетоглутарат-зависимые гидроксилазы активируют O 2 путем окислительного декарбоксилирования кетоглутарата , генерируя центры Fe(IV)=O, т.е. феррил , который гидроксилирует множество углеводородных субстратов. [ 9 ]
- цитохрома P450 Ферменты гема используют кофактор , вставляют феррильный кислород в насыщенные связи C–H, [ 10 ] эпоксидировать олефины, [ 11 ] [ 12 ] и окисляют ароматические группы. [ 13 ]
- Метанмонооксигеназа (ММО) окисляет метан в метанол посредством переноса атома кислорода от промежуточного соединения железа-оксо в его негем-дижелезном центре. [ 14 ] Много усилий направлено на воспроизведение реакций с использованием синтетических катализаторов. [ 6 ]
Молибден/вольфрам оксо-разновидности
[ редактировать ]
Оксо-лиганд (или аналогичный сульфидный лиганд) почти повсеместно встречается в химии молибдена и вольфрама, появляясь в рудах, содержащих эти элементы, во всей их синтетической химии, а также в их биологической роли (помимо нитрогеназы). Биологически транспортируемыми соединениями и отправной точкой биосинтеза принято считать оксометаллаты MoO 4 −2 или ВО 4 −2 . Все ферменты Mo/W, кроме нитрогеназы , связаны с одной или несколькими простетическими группами молибдоптерина . Центры Mo/W обычно циклически переключаются между шестивалентным (M(VI)) и четырехвалентным (M(IV)) состояниями. Хотя между этими ферментами существуют некоторые различия, члены всех трех семейств участвуют в переносе атома кислорода между центром Mo/W и субстратом. [ 15 ] Репрезентативными реакциями каждого из трех структурных классов являются:
- Сульфитоксидаза : SO 3 −2 + Н 2 О → SO 4 −2 + 2 ч. + + 2 и −
- ДМСО-редуктаза : H 3 CS(O)CH 3 ( ДМСО ) + 2 H + + 2 и − → H 3 CSCH 3 ( ДМС ) + H 2 O
- Альдегидферредоксиноксидоредуктаза : RCHO + H 2 O → RCO 2 H + 2 H + + 2 и −
Три различных класса кофакторов молибдена показаны на рисунке. Биологическое использование вольфрама зеркально отражает использование молибдена. [ 16 ]
Кислородвыделяющий комплекс
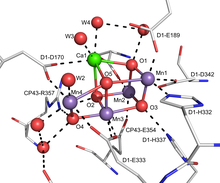
[ редактировать ]Активным центром кислородвыделяющего комплекса (ОКЭ) фотосистемы II (ФСII) является Са-центр Mn 4 O 5 с несколькими мостиковыми оксо-лигандами, которые участвуют в окислении воды до молекулярного кислорода. [ 17 ] В OEC предлагается использовать концевой оксо-промежуточный продукт в реакции окисления воды. Этот комплекс отвечает за производство почти всего молекулярного кислорода Земли. Это ключевое звено в кислородном цикле необходимо для большей части биоразнообразия , существующего на Земле.
«Оксо-стена»
[ редактировать ]
Термин «оксостенка» — это теория, используемая для описания того факта, что терминальные оксокомплексы не известны для металлоцентров с октаэдрической симметрией и числом d-электронов выше 5. [ 18 ] [ 19 ]
Оксосоединения ванадия через триады железа ( группы 3–8) хорошо известны, тогда как концевые оксосоединения металлов в кобальте через триады цинка (группы 9–12) редки и неизменно содержат металлы с координационными числами ниже 6. Тенденция сохраняется и для других кратных связей металл-лиганд. Заявленные исключения из этого правила [ 20 ] [ 21 ] [ 22 ] были отозваны. [ 23 ] [ 24 ] [ 25 ]
Оксокомплекс иридия Ir(O)(мезитил) 3 может показаться исключением из правила оксостенки, но это не потому, что комплекс неоктаэдрический. [ 7 ] Тригональная симметрия переупорядочивает металлические d-орбитали ниже вырожденной пары МО π*. В тройных симметричных комплексах допускается многократное связывание МО до 7 d-электронов. [ 18 ]
Концевые оксо-лиганды также достаточно редки для титановой триады, особенно циркония и гафния, и неизвестны для металлов 3-й группы (скандия, иттрия и лантана). [ 1 ]
См. также
[ редактировать ]- Множественная связь металл-лиганд
- Окись
- Полиоксометаллат
- Металлат
- оксофильный
- Дикислородный комплекс
Ссылки
[ редактировать ]- ^ Jump up to: а б с д Ньюджент, В.А., Майер, Дж.М. «Множественные связи металл-лиганд». Джон Уайли и сыновья, Нью-Йорк, 1988 год.
- ^ Делод, Лайонел; Ласло, Пьер (1 января 1996 г.). «Новый окислительный реагент на основе феррата калия (VI) 1» . Журнал органической химии . 61 (18): 6360–6370. дои : 10.1021/jo960633p . ISSN 0022-3263 . ПМИД 11667478 .
- ^ Холм, Р.Х. (1987). «Металлоцентрированные реакции переноса атома кислорода». хим. Откр. 87 (6): 1401–1449. дои : 10.1021/cr00082a005 .
- ^ Менье, Бернар; де Виссер, Самуэль П.; Шайк, Сасон (2004). «Механизм реакций окисления, катализируемых ферментами цитохрома P450». Химические обзоры . 104 (9): 3947–3980. дои : 10.1021/cr020443g . ISSN 0009-2665 . ПМИД 15352783 .
- ^ Ду, Г.; Абу-Омар, ММ (2008). «Оксо- и имидокомплексы рения и молибдена в каталитическом восстановлении». Современная органическая химия . 12 (14): 1185–1198. дои : 10.2174/138527208785740238 .
- ^ Jump up to: а б Гюнай, А.; Теопольд, К.Х. (2010). «Активация связи CH оксосоединениями металлов». хим. Откр. 110 (2): 1060–1081. дои : 10.1021/cr900269x . ПМИД 20143877 .
- ^ Jump up to: а б Хэй-Мазервелл, Робин С.; Уилкинсон, Джеффри ; Хусейн-Бейтс, Билкис; Херстхаус, Майкл Б. (1993). «Синтез и рентгеновская кристаллическая структура оксотримезитил-иридия (V)». Многогранник . 12 (16): 2009–2012. дои : 10.1016/S0277-5387(00)81474-6 .
- ^ Хуан, Сюнъи; Гроувс, Джон Т. (2017). «Помимо гидроксилирования, опосредованного феррилом: 40 лет механизма отскока и активации CH» . J Biol Inorg Chem . 22 (2–3): 185–207. дои : 10.1007/s00775-016-1414-3 . ПМК 5350257 . ПМИД 27909920 .
- ^ Хаузингер, Р.П. (январь – февраль 2004 г.). «Fe (II) / α-кетоглутарат-зависимые гидроксилазы и родственные ферменты». Крит. Преподобный Биохим. Мол. Биол . 39 (1): 21–68. дои : 10.1080/10409230490440541 . ПМИД 15121720 . S2CID 85784668 .
- ^ Ортис де Монтеллано, Пол Р. (2010). «Гидроксилирование углеводородов ферментами цитохрома P450» . Химические обзоры . 110 (2): 932–948. дои : 10.1021/cr9002193 . ISSN 0009-2665 . ПМК 2820140 . ПМИД 19769330 .
- ^ Кун, MJ (20 января 1998 г.). «Эпоксидирование олефинов цитохромом P450: данные сайт-специфического мутагенеза гидропероксо-железа как электрофильного окислителя» . Труды Национальной академии наук . 95 (7): 3555–60. Бибкод : 1998PNAS...95.3555V . дои : 10.1073/pnas.95.7.3555 . ЧВК 19874 . ПМИД 9520404 .
- ^ Фаринас, Эдгардо Т; Алькальде, Мигель; Арнольд, Фрэнсис (2004). «Эпоксидирование алкена, катализируемое цитохромом P450 BM-3 139-3». Тетраэдр . 60 (3): 525–528. дои : 10.1016/j.tet.2003.10.099 . ISSN 0040-4020 .
- ^ Корзеква, Кеннет; Трагер, Уильям; Гоутерман, Мартин ; Спенглер, Дейл; Лоу, Гильда (1985). «Ароматическое окисление, опосредованное цитохромом P450: теоретическое исследование». Журнал Американского химического общества . 107 (14): 4273–4279. дои : 10.1021/ja00300a033 . ISSN 0002-7863 .
- ^ Брунольд, ТК (2007). «Синтетическое железо-оксо-«алмазное ядро» имитирует структуру ключевого промежуточного продукта I в каталитическом цикле метанмонооксигеназы» . Учеб. Натл. акад. наук. США 104 (52): 20641–20642. Бибкод : 2007PNAS..10420641B . дои : 10.1073/pnas.0710734105 . ПМК 2409203 . ПМИД 18093936 .
- ^ Шварц, Г.; Мендель, Р.Р.; Риббе, М.В. (2009). «Молибденовые кофакторы, ферменты и пути». Природа . 460 (7257): 839–847. Бибкод : 2009Natur.460..839S . дои : 10.1038/nature08302 . ПМИД 19675644 . S2CID 205217953 .
- ^ Мукунд, С.; Адамс, MWW (1996). «Молибден и ванадий не заменяют вольфрам в каталитически активных формах трех вольфрамоферментов у гипертермофильных архей Pyrococcus Furiosus» . Дж. Бактериол. 178 (1): 163–167. дои : 10.1128/jb.178.1.163-167.1996 . ПМК 177634 . ПМИД 8550411 .
- ^ Jump up to: а б Умена, Ясуфуми; Каваками, Кейсуке; Шен, Цзянь-Рен; Камия, Нобуо (2011). «Кристаллическая структура фотосистемы II, выделяющей кислород, с разрешением 1,9 Å» (PDF) . Природа . 473 (7345): 55–60. Бибкод : 2011Природа.473...55У . дои : 10.1038/nature09913 . ISSN 0028-0836 . ПМИД 21499260 . S2CID 205224374 .
- ^ Jump up to: а б с Винклер, Джей Р .; Грей, Гарри Б. (2012). «Электронные структуры ионов оксометаллов». В Мингосе Дэвид Майкл П .; Дэй, Питер ; Даль, Йенс Педер (ред.). Молекулярно-электронные структуры комплексов переходных металлов I . Структура и связь. Том. 142. Спрингер Природа . стр. 17–28. дои : 10.1007/430_2011_55 . ISBN 978-3-642-27369-8 .
- ^ Ларсон, Вирджиния А.; Баттистелла, Беатрис; Рэй, Каллол; Ленерт, Николай; Нам, Вону (2020). «Оксокомплексы железа и марганца, оксостенка и не только». Обзоры природы Химия . 4 (8): 404–419. дои : 10.1038/s41570-020-0197-9 . S2CID 220295993 .
- ^ Андерсон, Трэвис М.; Нейверт, Уэйд А.; Кирк, Мартин Л.; Пикколи, Паула МБ; Шульц, Артур Дж.; Кетцле, Томас Ф.; Мусаев Джамаладдин Г.; Морокума, Кейджи; Цао, Руй; Хилл, Крейг Л. (17 декабря 2004 г.). «Оксокомплекс металла позднего перехода: K7Na9[O=PtIV(H2O)L2], L=[PW9O34]9-» . Наука 306 (5704): 2074–2077. дои : 10.1126/science.1104696 . ISSN 0036-8075 . ПМИД 15564312 . S2CID 41123922 . (Отозвано, см. дои : 10.1126/science.337.6092.290-а , PMID 22822129 , Часы втягивания )
- ^ Андерсон, Трэвис М.; Цао, Руй; Слонкина, Елена; Хедман, Бритт; Ходжсон, Кейт О.; Хардкасл, Кеннет И.; Нейверт, Уэйд А.; У, Шаосюн; Кирк, Мартин Л.; Ноттенбелт, Сушилла; Депперман, Эзра К. (1 августа 2005 г.). «Палладий-оксокомплекс. Стабилизация этого предлагаемого каталитического промежуточного продукта с помощью инкапсулирующего политвольфраматного лиганда» . Журнал Американского химического общества . 127 (34): 11948–11949. дои : 10.1021/ja054131h . ISSN 0002-7863 . ПМИД 16117527 . (Отозвано, см. два : 10.1021/ja207910h , PMID 22873777 , Часы втягивания )
- ^ Цао, Руй; Андерсон, Трэвис М.; Пикколи, Паула МБ; Шульц, Артур Дж.; Кетцле, Томас Ф.; Гелети Юрий В.; Слонкина, Елена; Хедман, Бритт; Ходжсон, Кейт О.; Хардкасл, Кеннет И.; Фанг, Сикуй (1 сентября 2007 г.). «Терминальные золото-оксокомплексы» . Журнал Американского химического общества . 129 (36): 11118–11133. дои : 10.1021/ja072456n . ISSN 0002-7863 . ПМИД 17711276 . (Отозвано, см. дои : 10.1021/ja207909y , PMID 22873776 , Часы втягивания )
- ^ О'Халлоран, Кевин П.; Чжао, Чунчао; Андо, Николь С.; Шульц, Артур Дж.; Кетцле, Томас Ф.; Пикколи, Паула МБ; Хедман, Бритт; Ходжсон, Кейт О .; и др. (2012). «Возвращаясь к комплексам поздний переходный металл-оксо на основе полиоксометаллата: стенды «оксо-стены»». Неорганическая химия . 51 (13): 7025–7031. дои : 10.1021/ic2008914 . ПМИД 22694272 .
- ^ Риттер, Стивен К. (12 июня 2012 г.). «Металл-оксо-документы отозваны» . cen.acs.org . Проверено 15 мая 2021 г.
- ^ Хэдлингтон2012-06-14T00:00:00+01:00, Саймон. «Стена Оксо все еще стоит, хотя неорганические бумаги убраны» . Химический мир . Проверено 15 мая 2021 г.
{{cite web}}: CS1 maint: числовые имена: список авторов ( ссылка )
