Карбеновый комплекс переходного металла
Карбеновый комплекс переходного металла представляет собой металлоорганическое соединение с двухвалентным углеродным лигандом , который сам по себе также называется карбеном . [1] Карбеновые комплексы были синтезированы из большинства переходных металлов и металлов f-блока . [2] используя множество различных синтетических путей, таких как нуклеофильное присоединение и абстракция альфа-водорода. [1] Термин «карбеновый лиганд» представляет собой формализм, поскольку многие из них не происходят напрямую из карбенов и большинство из них гораздо менее реакционноспособны, чем одиночные карбены. [2] Часто описывается как =CR 2 , карбеновые лиганды занимают промежуточное положение между алкилами. (-CR 3 ) и карбины (≡CR) . множество различных реагентов на основе карбена, таких как реагент Теббе В синтезе используется . Они также участвуют в каталитических реакциях, особенно в метатезисе алкенов , и представляют ценность как в промышленном гетерогенном, так и в гомогенном катализе для приготовления тонких химикатов в лабораторных и промышленных масштабах. [1] [3] [4]
Классификация
[ редактировать ]Карбеновые комплексы металлов часто делят на два типа. Карбены Фишера, названные в честь Эрнста Отто Фишера , имеют сильные π-акцепторы у металла и электрофильны по атому углерода карбена. Карбены Шрока , названные в честь Ричарда Р. Шрока , характеризуются более нуклеофильными карбеновыми углеродными центрами; эти виды обычно содержат металлы с более высокой степенью окисления (валентностью). N -Гетероциклические карбены (NHC) стали популяризироваться после того, как Ардуэнго в 1991 году выделил стабильный свободный карбен. [5] Отражая рост этой области, теперь известны карбеновые комплексы с широким диапазоном различной реакционной способности и разнообразными заместителями. Часто невозможно классифицировать карбеновый комплекс исключительно на основании его электрофильности или нуклеофильности. [1]
Карбены Фишера
[ редактировать ]
Общими характеристиками карбенов Фишера являются: [6]
- с низкой степенью окисления металлоцентр
- средние и поздние переходные металлы Fe(0) , Mo(0) , Cr(0)
- π -акцепторные металлические лиганды
- π-донорные заместители при карбеновом атоме, такие как алкокси- и алкилированные аминогруппы .
Примеры включают в себя (CO) 5 Вт=COMePh и (OC) 5Cr =C(NR2 ) Ph .

Карбеновые комплексы Фишера относятся к синглетной форме карбенов, где оба электрона занимают один и тот же sp. 2 орбиталь у углерода. Эта неподеленная пара отдает предпочтение пустой d-орбитали на основе металла, образуя σ-связь. Возможно π-связывание заполненной d-орбитали металла с пустой p-орбиталью атома углерода. Однако это взаимодействие обычно слабое, поскольку атомы альфа-донора также вносят вклад в эту орбиталь. По существу, карбены Фишера характеризуются наличием частичной двойной связи. Основные резонансные структуры карбенов Фишера передают отрицательный заряд металлическому центру, а положительный - атому углерода, что делает его электрофильным. [6]

Карбены Фишера можно сравнить с кетонами, причем атом углерода карбена является электрофильным, как и атом углерода карбонильной группы кетона. Это видно по резонансным структурам , где существенный вклад вносит структура, несущая положительный углеродный центр. [6] Как и кетоны, карбены Фишера могут вступать в альдольподобные реакции. Атомы водорода, присоединенные к атому углерода α к атому углерода карбена, являются кислотными и могут быть депротонированы основанием, таким как н -бутиллитий , с образованием нуклеофила, который может подвергаться дальнейшей реакции. [7]
Карбены Шрока
[ редактировать ]
Карбены Шрока не имеют π-принимающих лигандов на металлическом центре. Их часто называют алкилиденовыми комплексами . Обычно это подмножество карбеновых комплексов встречается с: [6]
- с высокой степенью окисления металлоцентр
- ранние переходные металлы Ti(IV) , Ta(V)
- σ-донорные, а иногда и π-донорные металлические лиганды
- водородные и алкильные заместители на карбеноидном углероде.
Примеры включают в себя ((CH 3 ) 3 CCH 2 )Ta=CHC(CH 3 ) 3 [9] и Os(PPh 3 ) 2 (NO)Cl(=CH 2 ) . [10]

Связывание в таких комплексах можно рассматривать как соединение металла в триплетном состоянии и триплетного карбена, образующее настоящую двойную связь. И металл, и атом углерода отдают по два электрона, по одному на каждую связь. Поскольку нет донорства атому карбена от соседних групп, степень обратной связи пи намного больше, образуя прочную двойную связь. Эти связи слабо поляризованы по отношению к углероду, поэтому атом карбена является нуклеофилом. Более того, основные резонансные структуры карбена Шрока передают отрицательный заряд атому углерода, делая его нуклеофильным. [6] Комплексы с метилиденовым лигандом ( =CH 2 ) — простейшие карбены типа Шрока.

N -Гетероциклические карбены
[ редактировать ]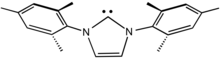
N -Гетероциклические карбены (NHC) являются особенно распространенными карбеновыми лигандами. [11] Они популярны, потому что их легче приготовить, чем карбены Шрока и Фишера. Фактически, многие NHC выделяются в виде свободных лигандов, поскольку они представляют собой стойкие карбены . [12] [13] Будучи сильно стабилизированными π-донорными заместителями, NHC являются мощными σ-донорами, но π-связь с металлом слабая. [14] По этой причине связь между углеродом и металлическим центром часто изображается одинарной дативной связью, тогда как карбены Фишера и Шрока обычно изображаются с двойными связями с металлом. Продолжая эту аналогию, NHC часто сравнивают с триалкилфосфиновыми лигандами . Подобно фосфинам, NHC служат лигандами-наблюдателями , которые влияют на катализ посредством комбинации электронных и стерических эффектов, но они не связывают субстраты напрямую. [15] [16]
Биметаллические карбеновые комплексы
[ редактировать ]Ранний пример этого режима связи был предоставлен [C 5 Me 5 Mn(CO) 2 ] 2 (μ-CO), полученный из диазометана :
- 2 C 5 Me 5 Mn(CO) 2 (thf) + CH 2 N 2 → [C 5 Me 5 Mn(CO) 2 ] 2 (μ−CH 2 ] + N 2 + 2 thf
Другим примером этого семейства соединений является реактив Теббе . Он имеет метиленовый мостик, соединяющий титан и алюминий . [17]
Применение металлических карбенов
[ редактировать ]Металлокарбеновые комплексы находят применение в гетерогенном и гомогенном катализе, а также в качестве реагентов для органических реакций.
Катализ
[ редактировать ]
Преобладающее применение карбенов металлов связано не с соединениями из вышеперечисленных классов, а с гетерогенными катализаторами, используемыми для метатезиса алкенов для синтеза высших алкенов. Для взаимного превращения легких алкенов, например бутенов, пропилена и этилена, используются различные родственные реакции. [18] Карбеновые комплексы используются в качестве промежуточных продуктов на пути Фишера-Тропша к углеводородам. [3]
Различные гомогенные карбеновые катализаторы, особенно рутениевые катализаторы Граббса и молибдено-имидные катализаторы Шрока, использовались для метатезиса олефинов в лабораторном синтезе природных продуктов и в материаловедении . [4]
Стехиометрические реакции
[ редактировать ]Гомогенные карбеновые комплексы типа Шрока, такие как реактив Теббе, можно использовать для олефинирования карбонилов, заменяя атом кислорода метилиденовой группой. Нуклеофильный атом углерода ведет себя аналогично атому углерода илида фосфора в реакции Виттига , атакуя электрофильный карбонильный атом кетона с последующим отщеплением оксида металла. [1]

В нуклеофильного отщепления реакции метильная группа может быть отделена от донорной группы карбена Фишера, что делает ее сильным нуклеофилом для дальнейшей реакции. [6]

Диазосоединения, такие как метилфенилдиазоацетат, можно использовать для циклопропанирования или для внедрения в связи CH органических субстратов. Эти реакции катализируются тетраацетатом диродия или родственными хиральными производными. Предполагается, что такой катализ протекает при посредничестве карбеновых комплексов. [19]

Реакция Вульфа-Детца
[ редактировать ]Карбены Фишера используются с алкинами в качестве исходных реагентов для реакции Вульфа-Детца с образованием фенолов. [20]

История
[ редактировать ]
Первым металлокарбеновым комплексом, о котором сообщалось, была красная соль Чугаева , впервые синтезированная еще в 1925 году, хотя карбеновый комплекс так и не был идентифицирован. [21] Характеристика (CO)5W(COCH3(Ph)) в 1960-х годах часто упоминается как отправная точка в этой области, и Эрнст Отто Фишер за это и другие достижения в металлоорганической химии был удостоен Нобелевской премии по химии 1973 года . [22] В 1968 году Ханс-Вернер Ванцлик и Карл Офеле по отдельности сообщили о N-гетероциклических карбенах с металлическими связями. [6] [23] [24] Синтез и характеристика ((CH 3 ) 3 CCH 2 )Ta=CHC(CH 3 ) 3 Ричардом Р. Шроком в 1974 году ознаменовали первый металл-алкилиденовый комплекс. [9] В 1991 году Энтони Дж. Ардуенго синтезировал и кристаллизовал первый стойкий карбен , NHC с большими адамантановыми алкильными группами, что способствовало развитию области N-гетерокарбеновых лигандов до его нынешнего использования. [5] [6]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с д и Эльшенбройх, Кристоф; Эльшенбройх, Кристоф (2011). Металлоорганические соединения (3, полное изд. и расширенное изд.). Вайнхайм: WILY-VCH. ISBN 978-3-527-29390-2 .
- ^ Jump up to: а б Арнольд, Полли Л.; Кейсли, Ян Дж. (12 августа 2009 г.). «F-Блок N-гетероциклических карбеновых комплексов» . Химические обзоры . 109 (8): 3599–3611. дои : 10.1021/cr8005203 . ISSN 0009-2665 .
- ^ Jump up to: а б Херрманн, Вольфганг А. (февраль 1982 г.). «Металлоорганические аспекты синтеза Фишера-Тропша» . Angewandte Chemie International Edition на английском языке . 21 (2): 117–130. дои : 10.1002/anie.198201171 . ISSN 0570-0833 .
- ^ Jump up to: а б Фюрстнер, Алоис (1 сентября 2000 г.). «Метатезис олефинов и не только» . Ангеванде Хеми . 39 (17): 3012–3043. doi : 10.1002/1521-3773(20000901)39:17<3012::AID-ANIE3012>3.0.CO;2-G .
- ^ Jump up to: а б Ардуэнго III AJ, Харлоу Р.Л., Клайн М. (1991). «Стабильный кристаллический карбен». Дж. Ам. хим. Соц. 113 (1): 361–363. дои : 10.1021/ja00001a054 .
- ^ Jump up to: а б с д и ж г час де Фремонт, Пьер; Марион, Николас; Нолан, Стивен П. (апрель 2009 г.). «Карбены: синтез, свойства и металлоорганическая химия» . Обзоры координационной химии . 253 (7–8): 862–892. дои : 10.1016/j.ccr.2008.05.018 . ISSN 0010-8545 .
- ^ Крэбтри Р.Х. (2005). Металлоорганическая химия переходных металлов (4-е изд.). Нью-Джерси: Wiley-Interscience. ISBN 978-0-471-66256-3 .
- ^ «Нейтронографическое исследование бис (циклопентадиенил) (метил) (метилен) тантала (V) при 15 К» . Acta Crystallographica Раздел C. Связь с кристаллической структурой . 44 (3): 439–443. 15 марта 1988 г. дои : 10.1107/S0108270187010527 . hdl : 1808/17672 .
- ^ Jump up to: а б Шрок, Ричард Р. (октябрь 1974 г.). «Алкилкарбеновый комплекс тантала путем внутримолекулярного отрыва альфа-водорода» . Журнал Американского химического общества . 96 (21): 6796–6797. дои : 10.1021/ja00828a061 . ISSN 0002-7863 .
- ^ Хилл, Энтони Ф.; Ропер, Уоррен Р.; Уотерс, Джойс М.; Райт, Энтони Х. (сентябрь 1983 г.). «Моноядерный, низковалентный, богатый электронами метиленовый комплекс осмия» . Журнал Американского химического общества . 105 (18): 5939–5940. дои : 10.1021/ja00356a050 . ISSN 0002-7863 .
- ^ Хан Ф.Е., Янке MC (2008). «Гетероциклические карбены: синтез и координационная химия». Ангеванде Хеми . 47 (17): 3122–72. дои : 10.1002/anie.200703883 . ПМИД 18398856 .
- ^ Альдеко-Перес Э., Розенталь А.Дж., Доннадье Б., Парамесваран П., Френкинг Г., Бертран Г. (октябрь 2009 г.). «Выделение C5-депротонированного имидазолия, кристаллического «аномального» N-гетероциклического карбена» . Наука . 326 (5952): 556–9. Бибкод : 2009Sci...326..556A . дои : 10.1126/science.1178206 . ПМЦ 2871154 . ПМИД 19900893 .
- ^ Ардуенго А.Дж., Герлих-младший, Маршалл У.Дж. (1 мая 2002 г.). «Стабильный диаминокарбен». Дж. Ам. хим. Соц. 117 (44): 11027–11028. дои : 10.1021/ja00149a034 .
- ^ Филлман К.Л., Пшойски Дж.А., Аль-Афьюни М.Х., Тонзетич З.Дж., Нейдиг М.Л. (февраль 2015 г.). «N-гетероциклические карбеновые комплексы» . Химическая наука . 6 (2): 1178–1188. дои : 10.1039/c4sc02791d . ПМК 4302958 . ПМИД 25621143 .
- ^ Пжойски Я.А., Веггеберг К.П., Арман Х.Д., Тонзетич З.Ю. (08 сентября 2015 г.). «Механистические исследования каталитического углерод-углеродного кросс-сочетания с помощью четко определенных комплексов железа NHC». АКС-катализ . 5 (10): 5938–5946. дои : 10.1021/acscatal.5b01445 .
- ^ Пжойски Я.А., Арман Х.Д., Тонзетич З.Ю. (18 декабря 2012 г.). «NHC-комплексы кобальта (II), имеющие отношение к каталитическим реакциям сочетания C – C». Металлоорганические соединения . 32 (3): 723–732. дои : 10.1021/om3010756 .
- ^ Херрманн, Вашингтон (1982). «Миленовый мостик: вызов синтетической, механистической и структурной металлоорганической химии». Чистая и прикладная химия . 54 : 65–82. дои : 10.1351/pac198254010065 .
- ^ Мол, Дж (13 апреля 2004 г.). «Промышленное применение метатезиса олефинов» . Журнал молекулярного катализа A: Химический . 213 (1): 39–45. doi : 10.1016/j.molcata.2003.10.049 . ISSN 1381-1169 .
- ^ Дэвис, Хью М.Л.; Мортон, Дэниел (21 марта 2011 г.). «Руководящие принципы сайт-селективной и стереоселективной межмолекулярной функционализации C – H донорно-акцепторными карбенами родия» . Обзоры химического общества . 40 (4): 1857–1869. дои : 10.1039/C0CS00217H . ISSN 1460-4744 .
- ^ Дания, Скотт Э., изд. (30 апреля 2004 г.). Органические реакции (1-е изд.). Уайли. дои : 10.1002/0471264180.или070.02 . ISBN 978-0-471-26418-7 .
- ^ Jump up to: а б Хан, Ф. Эккехардт; Янке, Марейке К. (14 апреля 2008 г.). «Гетероциклические карбены: синтез и координационная химия» . Международное издание «Прикладная химия» . 47 (17): 3122–3172. дои : 10.1002/anie.200703883 . ISSN 1433-7851 .
- ^ Фишер, Э.О.; Маасбёль, А. (август 1964 г.). «О существовании карбонилкарбенового комплекса вольфрама» . Angewandte Chemie International Edition на английском языке . 3 (8): 580–581. дои : 10.1002/anie.196405801 . ISSN 0570-0833 .
- ^ Ванцлик, Х.-В.; Шёнхерр, Х.-Й. (февраль 1968 г.). «Прямой синтез комплекса ртутной соли-карбена» . Angewandte Chemie International Edition на английском языке . 7 (2): 141–142. дои : 10.1002/anie.196801412 . ISSN 0570-0833 .
- ^ Офеле, К. (июнь 1968 г.). «1,3-Диметил-4-имидазолинилиден-(2)-пентакарбонилхром, новый карбеновый комплекс переходного металла» . Журнал металлоорганической химии . 12 (3): П42–П43. дои : 10.1016/s0022-328x(00)88691-x . ISSN 0022-328X .