Миграционная вставка
В металлоорганической химии мигрирующая вставка — это тип реакции , в которой соединяются два лиганда в металлокомплексе . Это подмножество реакций, которые очень похожи на реакции внедрения , и обе они различаются механизмом , который приводит к полученной стереохимии продуктов. Однако часто эти два понятия используются как взаимозаменяемые, поскольку механизм иногда неизвестен. Следовательно, мигрирующие реакции внедрения или, короче говоря, реакции внедрения определяются не механизмом, а общей региохимией , в которой одно химическое соединение внедряется в существующую связь , обычно второго химического соединения, например: [1]
Обзор
[ редактировать ]При мигрирующей вставке лиганд, который рассматривается как анионный лиганд (X), и лиганд, который рассматривается как нейтральная пара, генерируют новый анионный лиганд. Вступающие в реакцию анионы и нейтральные лиганды расположены рядом. Если -предшественник комплекс координационно насыщен , миграционная вставка часто приводит к образованию координационно ненасыщенного продукта. Затем новый (нейтральный) лиганд может вступить в реакцию с металлом, что приведет к дальнейшему внедрению. Этот процесс может происходить много раз на одном металле, как при полимеризации олефинов .
Анионный лиганд может быть: H − ( гидрид ), R − (алкил), ацил , Ar − ( арил ) или ИЛИ − ( алкоксид ). Способность этих групп мигрировать называется их миграционной способностью . Нейтральным лигандом может быть CO, алкен , алкин или в некоторых случаях даже карбен .
На мигрирующее прикрепление наблюдаются разнообразные реакции. Один из механизмов включает атаку анионного лиганда на электрофильную часть нейтрального лиганда (анионный лиганд мигрирует к нейтральному лиганду). Другой механизм заключается в том, что нейтральный лиганд вставляется между металлом и анионным лигандом.
введение CO
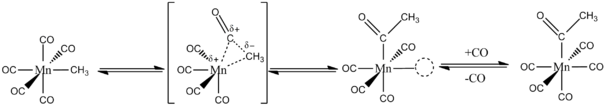
[ редактировать ]Введение монооксида углерода в связь металл-углерод с образованием ацильной группы лежит в основе реакций карбонилирования , которые дают множество коммерчески полезных продуктов. Механистические исследования показывают, что алкильная группа мигрирует внутримолекулярно к соседнему лиганду CO. [2] [3]
Первые исследования были проведены по конверсии CH 3 Mn(CO) 5 с получением ацетильного производного. [4] С использованием 13 CO, продукты - цис [Mn(COCH 3 )( 13 CO)(CO) 4 ] (схема 1).

Внедрение CO не всегда связано с миграцией. Обработка CpFe(L)(CO) 3 CH 13 CO дает смесь как продуктов миграции алкилов, так и продуктов, образовавшихся в результате истинного внедрения связанных карбонилов в метильную группу. На распределение продукта влияет выбор растворителя . [5]
Алкильные производные плоских квадратных комплексов особенно легко подвергаются внедрению CO. Реакции внедрения в плоские квадратные комплексы представляют особый интерес из-за их промышленного применения. Поскольку плоские квадратные комплексы часто являются координационно ненасыщенными , они склонны к образованию 5-координационных аддуктов, которые легко подвергаются мигрирующей вставке. [5] В большинстве случаев предпочтительным является путь миграции в плоскости, но, в отличие от нуклеофильного пути, он ингибируется избытком CO. [6]

Влияние на скорость реакции
[ редактировать ]- Штамм со стерическими эффектами . Увеличение стерического напряжения хелатной основной цепи в плоских квадратных комплексах сближает карбонильные и метильные группы, увеличивая реакционную способность реакций внедрения. [6]
- Степень окисления . Окисление металла имеет тенденцию увеличивать скорость реакции внедрения. Основной стадией, ограничивающей скорость в этом механизме, является миграция метильной группы на карбонильный лиганд, окисляющая металл за счет придания большего частичного положительного заряда ацетильному углероду и, таким образом, увеличения скорости реакции. [7]
- Кислоты Льюиса . Кислоты Льюиса также увеличивают скорость реакции по причинам, аналогичным окислению металлов, увеличивая положительный заряд углерода. Кислоты Льюиса связывают кислород CO и удаляют заряд, увеличивая электрофильность углерода. Это может увеличить скорость реакции в 10 раз. 8 , и образовавшийся комплекс достаточно стабилен, чтобы реакция протекала даже без дополнительного связывания CO с металлом. [7]
- Электроотрицательность уходящей группы . Увеличение электроотрицательности уходящей алкильной группы стабилизирует взаимодействие связи металл-углерод и, таким образом, увеличивает энергию активации, необходимую для миграции, снижая скорость реакции. [8]
- Транс -эффект . Известно, что лиганды в октаэдрическом или плоско-квадратном комплексе влияют на реакционную способность группы, по отношению к которой они находятся в транс . Это влияние лигандов часто называют транс -влиянием, и его интенсивность варьируется в зависимости от лиганда. Неполный список транс -влияющих лигандов выглядит следующим образом, от самого высокого транс -эффекта к самому низкому: [5] арил , алкил > NR 3 > PR 3 > AsR 3 > CO > Cl . Лиганды с большим транс -влиянием придают активному центру большую электрофильность. Экспериментально было показано, что увеличение электрофильности группы CO значительно увеличивает скорость реакции, а уменьшение электрофильности метильной группы немного увеличивает скорость реакции. Это можно продемонстрировать, реагируя плоскоквадратный комплекс [(PN)M(CO)(CH 3 )] с CO, где PN представляет собой бидентатный лиганд, связанный с фосфором или азотом. Эта реакция протекает с гораздо большим выходом, когда метильная группа представляет собой транс -P, а CO - транс -N, из-за более высокого транс -влияния более электроотрицательного азота. [6]
Обратная реакция
[ редактировать ]Декарбонилирование альдегидов : , противоположное внедрению CO, является хорошо известной реакцией
- RCHO → RH + CO
Реакция не получила широкого распространения отчасти потому, что алканы являются менее полезными материалами, чем предшественники альдегидов. Кроме того, реакция не часто проводится каталитически, поскольку экструдированный CO может медленно диссоциировать. [9] Экструзия CO из органического альдегида наиболее широко продемонстрирована с использованием катализатора Уилкинсона : [10]
- RhCl(PPh 3 ) 3 + RCHO → RhCl(CO)(PPh 3 ) 2 + RH + PPh 3
см. в разделе «Реакция декарбонилирования Цуджи-Уилкинсона». Пример этого элементарного металлоорганического этапа синтеза
Введение других оксидов
[ редактировать ]Многие электрофильные оксиды встраиваются в углеродные связи металлов; к ним относятся диоксид серы , диоксид углерода и оксид азота. Эти реакции имеют ограниченное практическое значение или вообще не имеют его, но представляют исторический интерес. С алкилами переходных металлов эти оксиды ведут себя как электрофилы и внедряются в связь между металлами и их относительно нуклеофильными алкильными лигандами. Как обсуждалось в статье о комплексах диоксида серы металлов , внедрение SO 2 было исследовано особенно подробно. Вставки SO 2 дают как O -сульфинаты, так и S -сульфинаты, в зависимости от металлического центра. [11] В случае плоских квадратных алкильных комплексов предполагается предварительное равновесие, связанное с образованием аддукта. [12]
Внедрение алкенов в связи металл-углерод.
[ редактировать ]Важное значение имеет внедрение алкенов как в металл-углерод. Введение этилена и пропилена в алкилы титана является краеугольным камнем катализа Циглера-Натта , основного источника полиэтилена и полипропилена. Большая часть этой технологии использует гетерогенные катализаторы, но широко распространено мнение, что принципы и наблюдения над гомогенными системами применимы и к твердотельным версиям. Сопутствующие технологии включают процесс производства высших олефинов Shell , который производит предшественники моющих средств .

Стадии полимеризации алкенов. Шаг i включает связывание мономера с металлом, а шаг ii включает этап мигрирующего внедрения. Эти этапы, чередующиеся с одной стороны металлического центра на другую, повторяются много раз для каждой полимерной цепи. Коробка представляет собой вакантный (или чрезвычайно лабильный) координационный участок.
Механизм
[ редактировать ]Факторы, влияющие на скорость внедрения олефина, включают образование циклического плоского четырехцентрового переходного состояния , включающего начальное образование связи между металлом и углеродом олефина. Из этого переходного состояния можно видеть, что на β-углероде образуется частичный положительный заряд, а на углероде, первоначально связанном с металлом, образуется частичный отрицательный заряд. Эта поляризация объясняет наблюдаемое впоследствии образование связи между отрицательно заряженным углеродом/водородом и положительно заряженным β-углеродом, а также одновременное образование связи металл-α-углерод. Это переходное состояние также подчеркивает два фактора, которые наиболее сильно влияют на скорость реакций внедрения олефина: (i) перекрытие орбиталей алкильной группы, первоначально присоединенной к металлу, и (ii) прочность связи металл-алкил. При большем перекрытии орбиталей между частично положительным β-углеродом и частично отрицательным углеродом водородной/алкильной группы облегчается образование новой связи CC. С увеличением прочности связи металл-алкил разрыв связи между металлом и связью водород/алкилуглерод с образованием двух новых связей с α-углеродом и β-углеродом (соответственно) происходит медленнее, что снижает скорость реакции внедрения. [13]
Внедрение алкенов по связям M–H
[ редактировать ]Введение алкенов в связи металл-водород является ключевым этапом реакций гидрирования и гидроформилирования . В реакции участвуют алкеновые и гидридные лиганды, объединяющиеся в координационной сфере катализатора. При гидрировании образующийся алкиллиганд соединяется со вторым гидридом, образуя алкан. Аналогичные реакции применимы и к гидрированию алкинов: алкенильный лиганд соединяется с гидридом, отщепляя алкен.

Механизм
[ редактировать ]По механизму внедрение алкенов по связи М–Н и по связям М–С описывается аналогично. Оба включают четырехчленные переходные состояния, в которых менее замещенный углерод оказывается в металле.
Обратным процессом внедрения олефина в связь металл-водород является отщепление β-гидрида . Принцип микроскопической обратимости требует, чтобы механизм отщепления β-гидрида следовал тому же пути, что и механизм внедрения алкенов в металлогидридные связи. Первым требованием для удаления β-гидрида является наличие водорода в положении β по отношению к металлу. β-элиминирование требует наличия вакантной координационной позиции на металле, которая будет вмещать отщепляемый водород. [14]
Промышленное применение
[ редактировать ]Карбонилирование
[ редактировать ]используемыми применениями мигрирующего внедрения карбонильных групп являются и производство уксусной кислоты карбонилированием гидроформилирование метанола Двумя широко . Первый превращает алкены, водород и окись углерода в альдегиды. Производство уксусной кислоты карбонилированием осуществляется двумя схожими промышленными процессами. Более традиционным является процесс получения уксусной кислоты Monsanto , в котором для преобразования метанола в уксусную кислоту используется родий-йодный катализатор. Этот процесс был заменен процессом Cativa , в котором используется родственный иридиевый катализатор [Ir(CO) 2 I 2 ]. − ( 1 ). [15] [16] К 2002 году годовое производство уксусной кислоты во всем мире составило 6 миллионов тонн, из которых примерно 60% производится по процессу Cativa. [15]
процесса Cativa Каталитический цикл , показанный выше, включает этапы как внедрения, так и удаления. Реакция окислительного присоединения йодистого метила с ( 1 ) включает формальное внедрение центра иридия(I) в связь углерод-йод, тогда как стадии ( 3 )-( 4 ) являются примером миграционного внедрения оксида углерода в иридий. -углеродная связь. Активные частицы катализатора регенерируются путем восстановительного удаления ацетилйодида 4 из ( ) - реакции деинсерции. [15]
Полимеризация алкенов
[ редактировать ]Промышленное применение алкеновых вставок включает катализируемые металлами пути получения полиэтилена и полипропилена. Обычно эти превращения гетерогенно катализируются трихлоридом титана, который активируется алкилами алюминия. Эта технология известна как катализаторы Циглера-Натта . [17] В этих реакциях этилен координируется с металлическим титаном с последующим его внедрением. Эти этапы можно повторять несколько раз, что потенциально может привести к получению полимеров с высокой молекулярной массой.
Ссылки
[ редактировать ]- ^ Эльшенбройх, К. (2006). Металлоорганические соединения . Вайнхайм: Wiley-VCH. ISBN 978-3-527-29390-2 .
- ^ Хартвиг, Дж. Ф. (2010). Химия органопереходных металлов: от связывания к катализу . Нью-Йорк, штат Нью-Йорк: Университетские научные книги. ISBN 978-1-891389-53-5 .
- ^ Ядав, М.С. (2005). Краткий обзор по неорганической химии . Публикации Анмола. п. 244. ИСБН 978-81-261-1898-4 .
- ^ Ф. Кальдераццо, Ф. А. Коттон. «Карбонилирование пентакарбонила метилмарганца и декарбонилирование ацетила.Пентакарбонил марганца». Неорг. хим. , 1962, 1, 30–36. https://doi.org/10.1021/ic50001a008 .
- ^ Jump up to: а б с Андерсон, ГК; Кросс, Р.Дж. (1984). «Реакции внедрения карбонила в плоские квадратные комплексы». Акк. хим. Рез. 17 (2): 67–74. дои : 10.1021/ar00098a005 .
- ^ Jump up to: а б с Кавелл, К.Дж. (1996). «Недавние фундаментальные исследования миграционного внедрения в металл-углеродные связи». Коорд. хим. Откр. 155 (11): 209–243. дои : 10.1016/S0010-8545(96)90182-4 .
- ^ Jump up to: а б Александр, Джей-Джей (1985). «Вставки в связи переходный металл-углерод». В Хартли; Патай (ред.). Химия связи металл-углерод . Том. 2. Джон Уайли и сыновья. дои : 10.1002/9780470771747.ch5 .
- ^ Шустерман, AJ; Тамир, И.; Просс, А. (1988). «Механизм реакций металлоорганической миграции. Подход с использованием конфигурационного смешивания (СМ)». Дж. Органомет. хим. 340 (2): 203–222. дои : 10.1016/0022-328X(88)80076-7 .
- ^ Фриструп, Питер; Крейс, Майкл; Пальмелунд, Андерс; Норрби, Пер-Ола; Мэдсен, Роберт (2008). «Механизм родий-катализируемого декарбонилирования альдегидов: комбинированное экспериментальное и теоретическое исследование». Дж. Ам. хим. Соц. 130 (15): 5206–5215. дои : 10.1021/ja710270j . ПМИД 18303836 . S2CID 207119793 .
- ^ Оно, К.; Цудзи, Дж. (1968). «Органический синтез с помощью соединений благородных металлов. XXXV. Новые реакции декарбонилирования альдегидов и ацилгалогенидов с использованием комплексов родия». Дж. Ам. хим. Соц. 90 (1): 99–107. дои : 10.1021/ja01003a018 .
- ^ Дуглас; МакДэниел; Александр (1994). Концепции и модели неорганической химии (3-е изд.). Джон Уайли и сыновья, Inc. ISBN 978-0-471-62978-8 .
- ^ Паддефатт, РА; Сталтери, Массачусетс (1980). «Конкуренция между внедрением диоксида серы в связь метил- или фенил-переходного металла». Журнал металлоорганической химии . 193 : C27–C29. дои : 10.1016/S0022-328X(00)86091-X .
- ^ Бургер, Би Джей; Томпсон, Мэн; Коттер, штат Вашингтон; Беркоу, Дж. Э. (1990). «Внедрение этилена и удаление β-водорода в алкильные комплексы перметилскандоцена. Исследование стадий роста и обрыва цепи при полимеризации этилена по Циглеру-Натте». Дж. Ам. хим. Соц. 112 (4): 1566–1577. дои : 10.1021/ja00160a041 .
- ^ Крэбтри, Р. Х. (2009). Металлоорганическая химия переходных металлов . Джон Уайли и сыновья . п. 192. ИСБН 978-0-470-25762-3 .
- ^ Jump up to: а б с Джонс, Джейн Х. (2000). «Процесс Cativa производства уксусной кислоты» . Обзор платиновых металлов . 44 (3): 94–105.
- ^ Санли, Дж.Дж.; Уотсон, диджей (2000). «Высокопроизводительный катализ карбонилирования метанола с использованием иридия - процесс Cativa для производства уксусной кислоты». Катализ сегодня . 58 (4): 293–307. дои : 10.1016/S0920-5861(00)00263-7 .
- ^ Кисин Ю.В. (2008). «Синтез, химический состав и структура компонентов переходных металлов и сокатализаторов в каталитических системах полимеризации алкенов» . Реакции полимеризации алкенов с катализаторами из переходных металлов . Амстердам: Эльзевир . стр. 207–290. ISBN 978-0-444-53215-2 .