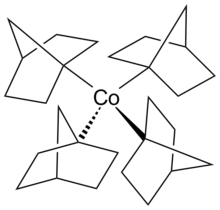
Металл тетранорборнил
В металлоорганической химии тетранорборнилы металлов представляют собой соединения формулы M(nor) 4 (M = металл в степени окисления +4) (1-нор = 4бицикло[2.2.1]гепт-1-ил) и являются одними из Крупнейшая серия тетраалкильных комплексов, происходящих от идентичных лигандов . [1] [2] Металлические тетранорборнилы демонстрируют однородную стехиометрию , низкоспиновые конфигурации и высокую стабильность , что можно объяснить их металлическим центром в степени окисления +4 . Считается, что стабильность тетранорборнилов металлов обусловлена преимущественно неблагоприятным удалением β-гидрида . Компьютерные расчеты показали, что эффекты дисперсии Лондона вносят существенный вклад в стабильность тетранорборнилов металлов. В частности, Fe(nor) 4 имеет стабилизацию 45,9 ккал/моль. −1 . Известные тетранорборнилы металлов синтезируются с металлическими центрами кобальта , марганца или железа . [3]
Подготовка
[ редактировать ]Традиционно тетранорборнилы металлов получают путем реакции алкиллития , такого как 1-норборниллития, с переходных металлов галогенидами при перемешивании стеклянными шариками в пентане . За этим следует этап фильтрации с использованием колонки с оксидом алюминия для удаления побочных продуктов пентана. Наконец, этап перекристаллизации из пентана для получения кристаллического соединения. [1]
Предложены альтернативные методы получения тетранорборнилов металлов. В частности, комплекс тетракис(1-норборнил)хрома можно получить в условиях инертной атмосферы с растворением 1-норборниллития в гексане . Добавляют CrCl 3 (ТГФ) 3 и перемешивают в течение 48 часов. После этого раствор центрифугируют для удаления LiCl . Полученный супернатант наносят на колонку с оксидом алюминия, используя гексан в качестве элюирующего растворителя. Использование колонки с оксидом алюминия позволяет собрать фиолетовую фракцию, которая подвергается выпариванию растворителя и сублимации с получением желаемого комплекса Cr(nor) 4 . [4]
Комплекс тетракис (1-норборнил)кобальта(IV) можно получить следующим образом:
- CoCl 2 ·THF + 4norLi → [пентан] [Co(nor) 4 ] + CO + 4 LiCl + 2THF [5]
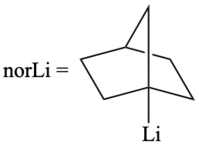
1-норборниллитий
Комплекс тетракис(1-норборнил)молибдена(IV) был получен Уильямом М. Дэвисом, Ричардом Р. Шроком и Ричардом М. Колодзием следующим образом:
- MoCl 3 (ТГФ) 3 + 4норLi → [Эфир/ТГФ ( 30 / 1 )] Мо(нор) 4 [6]
MoCl 3 (ТГФ) 3 перемешивали с 1-норборниллитием в смеси ТГФ и диэтилового эфира при температуре . Затем реакционную смесь нагревали до и примерно через 90 минут наблюдалось появление красного цвета с синим осадком . Реакционную смесь затем фильтровали для удаления синего осадка. Красный фильтрат затем восстанавливали в вакууме с получением красных кристаллов Mo(nor) 4 . [6]
Структура и связь
[ редактировать ]Обычно считается, что стабильность тетранорборнилов металлов является результатом неблагоприятного отщепления β-водорода. Разновидности металлоалкилов с β-атомами водорода, присутствующими в алкильной группе, оказываются в невыгодном положении из-за миграции β-водорода к металлическому центру, что приводит к удалению олефина и образованию соответствующего гидрида металла . 1-норборнил не подвергается миграции β-водорода, хотя он содержит 6 атомов β-водорода из-за неблагоприятного образования олефина, 1-норборнена. Согласно правилу Бредта , один из sp 2 атомы углерода атомов углерода с двойной связью будут расположены на мостике, что приведет к сильному напряжению 1-норборнена. [7] Удаление β-водорода не объясняет образование комплексов тетранорборнилов металлов, которые синтезируются из предшественников центров металлов с более низкой валентностью , укороченные длины связей между металлическим центром и атомами углерода 1-норборнильного лиганда или возникающую в результате низкоспиновую тетраэдрическую молекулярную геометрию . [1] [3]

Неблагоприятная миграция β-водорода, приводящая к образованию 1-норборнена из металлокомплекса 1-норборнила. [7]
Квантово-механические расчеты показали, что дисперсионные силы Лондона между норборнильными лигандами ответственны за стабильность и молекулярную геометрию гомолептических тетранорборнильных металлокомплексов. [3] [7]
Комплексы тетранорборнилов металлов, состоящие из двухвалентных и трехвалентных металлов в центрах Cr , Mn , Fe и Co, галогенидов подвергаются образованию отрицательно заряженных комплексов с последующим окислением , которое индуцируется другими видами переходных металлов в реакции. Факторы, которые приводят к диспропорционированию, традиционно считаются производными от третичного карбанионного лиганда, 1-норборниллития, и отсутствия возможности у пентанового растворителя действовать в качестве лиганда. Следовательно, тетранорборнилы металлов, состоящие из переходных металлов первого ряда, недоступны для проникновения небольшими реагентами из-за координационной сферы металлоцентра. [1]
Тетракис(1-норборнил)кобальт(IV)
[ редактировать ]Тетракис(1-норборнил)кобальт(IV) представляет собой термостабильный гомолептический комплекс, наблюдаемый с σ-связывающими лигандами. Металл-тетранорборниловый комплекс был первым изолированным низкоспиновым комплексом с тетраэдрической молекулярной геометрией. Комплекс тетракис(1-норборнил)кобальта(IV) был впервые синтезирован Бартоном К. Бауэром и Говардом Г. Теннентом в 1972 году. [1] [8] [9]
Степень окисления тетракис (1-норборнил)кобальта(IV) представляет собой обратимую реакцию с использованием O 2 в качестве окислителя . [10] Координационное окружение металлического центра кобальта имеет искаженную тетраэдрическую структуру. При исследовании рентгеновской кристаллографии металл тетранорборнил имеет кристаллографическую симметрию C s благодаря наличию шести атомов углерода, уложенных в зеркальной плоскости. Однако четыре атома углерода, связанные с металлическим центром кобальта, напоминали тетрагонально сжатый тетраэдр, который проявлялся как псевдоD 2d - симметрия.
Центр металлического кобальта в степени окисления +4 имеет d 5 конфигурация . [11] Как правило, д 5 Ожидается, что конфигурация приведет к образованию высокоспинового комплекса, содержащего 5 неспаренных электронов и только 1 неспаренный электрон в низкоспиновом тетраэдрическом комплексе. Единственный неспаренный электрон находится на разрыхляющей орбитали t 2 , что может вызвать в структуре ян-теллеровское искажение . Однако Теопольд и его коллеги предположили, что небольшое тетрагональное сжатие могло быть результатом стерических взаимодействий между норборнильными лигандами и силами упаковки кристаллов. [10]
Тетракис(1-норборнил)железо(IV)
[ редактировать ]Комплекс тетракис(1-норборнил)железа(IV) был впервые синтезирован Бартоном К. Бауэром и Говардом Г. Теннентом в 1972 году. [1] 1-норборнильные лиганды комплекса обладают сильным дисперсионным притяжением и высокой деформацией кольца , что, как следствие, затрудняет реакции отщепления α- и β-гидридов. Кроме того, идентичные лиганды вызывают пониженную химическую активность из-за скученной химической среды, затрудняющей взаимодействие малых молекул со связями Fe-C. [12]
Синтезированные комплексы
[ редактировать ]Бартон К. Бауэр и Говард Г. Теннент смогли успешно синтезировать и охарактеризовать следующие тетранорборнилы металлов, полученные из переходных металлов первого , второго и третьего ряда : [1]
- тетракис(1-норборнил)гафний
- тетракис(1-норборнил)цирконий
- тетракис(1-норборнил)титан
- тетракис(1-норборнил)ванадий
- тетракис(1-норборнил)хром
- тетракис(1-норборнил)марганец
- тетракис(1-норборнил)железо
- тетракис(1-норборнил)молибден
Металлические тетранорборнильные комплексы гафния , циркония , титана и ванадия демонстрируют тетраэдрическую молекулярную геометрию , которая аналогична тетрахлоридной форме металлов. Для сравнения, комплексы кобальта , марганца и железа имеют тетрагональную молекулярную геометрию. [1] Комбинация дисперсионной силы Лондона и стерических эффектов 1-норборнильных лигандов приводит к стабильности, наблюдаемой для металлического центра. [3]
Характеристика
[ редактировать ]Магнитные измерения
[ редактировать ]Результирующая молекулярная геометрия комплексов тетранорборнилов металлов обусловлена наличием неспаренных и спаренных d-электронов . Магнитные измерения показали, что d-электроны тетракис(1-норборнил)хрома (d 2 ) и тетракис(1-норборнил)марганец (d 3 ) не являются спин-спаренными. Четыре d-электрона тетракис(1-норборнил)железа и тетракис(1-норборнил)кобальта спарены по спинам. [1]
Спектроскопия электронного парамагнитного резонанса
[ редактировать ]Тетранорборнилы металлов обычно характеризуются с помощью спектроскопии электронного парамагнитного резонанса (ЭПР). Тетракис(1-норборнил)молибден наблюдался как сигнал ЭПР при комнатной температуре, возникающий из-за 2 металлоцентр, который, как считалось, имел два неспаренных электрона на eg- орбитали . Кроме того, результирующий сигнал ЭПР тетракис(1-норборнил)хрома был сопоставим. [6] [13]
Циклическая вольтамперометрия
[ редактировать ]В 1988 году Клаус Х. Теопольд и Эрин К. Бирн провели электрохимический эксперимент, циклическую вольтамперометрию , чтобы определить, насколько окисляющим является металлический центр комплекса тетракис (1-норборнил) кобальта (IV). В ТГФ наблюдались две обратимые волны переноса электронов при -0,65 и -2,02 В, что показало, что разница в пиковых потенциалах соответствует двум процессам одноэлектронного переноса по сравнению с парой феррицений/ ферроцен . [5] В том же году Уильям М. Дэвис, Ричард Р. Шрок и Ричард М. Колодзей построили циклическую вольтамперограмму тетракис (1-норборнил) молибдена. наблюдались две волны окисления при -0,15 и +1,25 В ДХМ В. Окисление при -0,15 В считалось обратимым. Для сравнения, второе окисление при +1,25 В считалось необратимым. [6]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я Бауэр, Бартон К.; Теннент, Ховард Г. (апрель 1972 г.). «Бицикло[2.2.1]гепт-1-илы переходных металлов» . Журнал Американского химического общества . 94 (7): 2512–2514. дои : 10.1021/ja00762a056 . ISSN 0002-7863 .
- ^ Абрахамсон, Хармон Б.; Бранденбург, Кэтрин Л.; Лусеро, Барбара; Мартин, Мэри Э.; Деннис, Элеонора (сентябрь 1984 г.). «Спектроскопия и фотохимия тетранорборнильных комплексов титана и хрома» . Металлоорганические соединения . 3 (9): 1379–1386. дои : 10.1021/om00087a010 . ISSN 0276-7333 .
- ^ Jump up to: а б с д Липтрот, Дэвид Дж.; Го, Цзин-Донг; Нагасе, Сигэру; Пауэр, Филип П. (14 ноября 2016 г.). «Дисперсионные силы, диспропорционирование и стабильные высоковалентные алкилы поздних переходных металлов» . Angewandte Chemie, международное издание . 55 (47): 14766–14769. дои : 10.1002/anie.201607360 . ISSN 1433-7851 . ПМИД 27778428 .
- ^ Бранденбург, Кэтрин Линн. Фотоиндуцированные реакции комплексов переходных металлов VI группы . OCLC 83966357 .
- ^ Jump up to: а б Бирн, Эрин К.; Теопольд, Клаус Х. (февраль 1987 г.). «Окислительно-восстановительная химия тетракис(1-норборнил)кобальта. Синтез и характеристика алкила кобальта(V) и скорость самообмена пары Co(III)/Co(IV)» . Журнал Американского химического общества . 109 (4): 1282–1283. дои : 10.1021/ja00238a066 . ISSN 0002-7863 .
- ^ Jump up to: а б с д Колодзей, Р.М.; Шрок, Р.Р.; Дэвис, WM (27 декабря 1988 г.). "ХимИнформ Реферат: Синтез и характеристика Мо(нор)4 (нор: 1-норборнила)" . ХимИнформ . 19 (52). дои : 10.1002/chin.198852222 . ISSN 0931-7597 .
- ^ Jump up to: а б с «Эффекты дисперсии при стабилизации металлоорганических соединений: тетра-1-норборнильные производные переходных металлов первого ряда как исключительные примеры» . doi : 10.1021/acs.jpca.9b06769.s001 . Проверено 12 марта 2023 г.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Бирн, Эрин К.; Ричесон, Дэррин С.; Теопольд, Клаус Х. (1986). «Тетракис(1-норборнил)кобальт, низкоспиновый тетраэдрический комплекс переходного металла первого ряда» . Журнал Химического общества, Chemical Communications (19): 1491–1492. дои : 10.1039/c39860001491 . ISSN 0022-4936 .
- ^ Бирн, Эрин К.; Теопольд, Клаус Х. (май 1989 г.). «Синтез, характеристика и способность к переносу электронов норборнильных комплексов кобальта в необычно высоких степенях окисления» . Журнал Американского химического общества . 111 (11): 3887–3896. дои : 10.1021/ja00193a021 . ISSN 0002-7863 .
- ^ Jump up to: а б Бирн, Эрин К.; Ричесон, Дэррин С.; Теопольд, Клаус Х. (1986). «Тетракис(1-норборнил)кобальт, низкоспиновый тетраэдрический комплекс переходного металла первого ряда» . Журнал Химического общества, Chemical Communications (19): 1491. doi : 10.1039/c39860001491 . ISSN 0022-4936 .
- ^ Грин, Малкольм Л.Х.; Паркин, Джерард (28 апреля 2014 г.). «Применение метода классификации ковалентных связей для преподавания неорганической химии» . Журнал химического образования . 91 (6): 807–816. Бибкод : 2014ЖЧЭд..91..807Г . дои : 10.1021/ed400504f . ISSN 0021-9584 .
- ^ Ли, Хуэйдун; Ван, Линьшен; Ху, Юйчэн; Чжан, Цзе; Ван, Ди; Фан, Цюньчао; Кинг, Р. Брюс; Шефер, Генри Ф. (27 августа 2020 г.). "Сравнительное исследование термической стабильности экспериментально известных высоковалентных соединений Fe(IV) Fe(1-норборнил) 4 и Fe(циклогексил) 4" . Журнал физической химии А. 124 (34): 6867–6876. Бибкод : 2020JPCA..124.6867L . doi : 10.1021/acs.jpca.0c04055 . ISSN 1089-5639 . ПМИД 32786998 . S2CID 221127617 .
- ^ Уорд, Джорджия; Бауэр, Британская Колумбия; Финдли, М.; Чиен, Джеймс К.В. (7 мая 1974 г.). "ХимИнформ Реферат: Электронный парамагнитный резонанс тетракис(1-норборнил)хрома" . Chemischer Informationsdienst . 5 (18). дои : 10.1002/chin.197418348 . ISSN 0009-2975 .