Реакция Гриньяра
| Классическая реакция Гриньяра | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Назван в честь | Виктор Гриньяр | ||||||||||
| Тип реакции | Реакция сцепления | ||||||||||
| Реакция | |||||||||||
| |||||||||||
| Идентификаторы | |||||||||||
| Портал органической химии | реакция Гриньяра | ||||||||||
| RSC Идентификатор онтологии | RXNO: 0000014 | ||||||||||

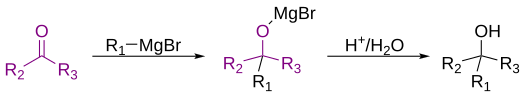
Реакция Гриньяра ( Французский: [ɡʁiɲaʁ] ) — металлоорганическая химическая реакция , в которой, согласно классическому определению, углерод- алкил , аллил , винил или арилмагнийгалогениды ) . ( реагент Гриньяра добавляются к карбонильным группам альдегида или кетона в безводных условиях . [1] [2] [3] Эта реакция важна для образования углерод-углеродных связей . [4] [5]
История и определения
[ редактировать ]Реакции и реагенты Гриньяра были открыты и названы в честь французского химика Франсуа Огюста Виктора Гриньяра ( Университет Нанси , Франция), который описал их в 1900 году. [6] За эту работу он был удостоен Нобелевской премии по химии 1912 года . [7]
Реакция органического галогенида с магнием не является реакцией Гриньяра, но дает реактив Гриньяра. [8]

Классически реакция Гриньяра относится к реакции между кетоновой или альдегидной группой с реагентом Гриньяра с образованием первичного или третичного спирта. [1] Однако некоторые химики понимают под этим определением все реакции любых электрофилов с реактивами Гриньяра. [9] Поэтому существуют споры по поводу современного определения реакции Гриньяра. В индексе Merck , опубликованном в Интернете Королевским химическим обществом , признается классическое определение, за которым следует: «Более современная интерпретация расширяет рамки реакции, включая добавление реагентов Гриньяра к широкому спектру электрофильных субстратов». [9] Такое разнообразие определений показывает, что в химическом сообществе существуют некоторые споры по поводу определения реакции Гриньяра.
Ниже показаны некоторые реакции с участием реагентов Гриньяра , но сами они классически не понимаются как реакции Гриньяра.

Механизм реакции
[ редактировать ]Поскольку углерод более электроотрицательен , чем магний, углерод, присоединенный к магнию, действует как нуклеофил и атакует электрофильный атом углерода в полярной связи карбонильной группы. шестичленного кольца Присоединение реактива Гриньяра к карбонильной группе обычно происходит через переходное состояние , как показано ниже. [10]

На основе обнаружения побочных продуктов радикального сочетания также был предложен альтернативный механизм одноэлектронного переноса (SET), который включает первоначальное образование промежуточного кетильного радикала. [11] что механизм действия (полярный или радикальный) зависит от субстрата, при этом потенциал восстановления карбонильного Недавнее компьютерное исследование показывает , соединения служит ключевым параметром. [12]
Условия
[ редактировать ]
Реакцию Гриньяра проводят в безводных условиях . [3] В противном случае реакция завершится неудачей, поскольку реактив Гриньяра будет действовать как основание, а не как нуклеофил, и захватывать лабильный протон, а не атаковать электрофильный участок. Это приведет к отсутствию образования желаемого продукта, поскольку R-группа реактива Гриньяра станет протонированной, а часть MgX стабилизирует депротонированные частицы.
Чтобы предотвратить это, реакции Гриньяра завершаются в инертной атмосфере , чтобы удалить всю воду из реакционной колбы и обеспечить образование желаемого продукта. [13] Кроме того, если в исходном материале есть кислые протоны, как показано на рисунке справа, это можно преодолеть, защитив кислотный центр реагента, превратив его в простой или силиловый эфир, чтобы исключить лабильный протон из раствор до реакции Гриньяра.
Варианты
[ редактировать ]Было обнаружено, что другие варианты реактива Гриньяра улучшают хемоселективность реакции Гриньяра, включая, помимо прочего: Турбо-Гриньяра, церийорганические реагенты и купраторганические реагенты (Гилмана).
Турбо-Гриньяр
[ редактировать ]Турбо-Гриньяра – это реактивы Гриньяра, модифицированные хлоридом лития . По сравнению с обычными реактивами Гриньяра, Турбо-Гриньяр более хемоселективен ; сложные эфиры , амиды и нитрилы не вступают в реакцию с реактивом Турбо-Гриньяра. [14]

Реагенты Гриньяра, модифицированные гетерометаллами.
[ редактировать ]
Поведение реактивов Гриньяра можно с пользой изменить в присутствии других металлов. Соли меди(I) дают органокупраты , которые преимущественно вызывают 1,4-присоединение . [15] Трихлорид церия допускает селективное 1,2-присоединение к одним и тем же субстратам. Галогениды никеля и палладия катализируют реакции кросс-сочетания .
См. также
[ редактировать ]- реактив Гриньяра
- Реакция Виттига
- Реакция Хорнера-Уодсворта-Эммонса
- Реакция Барбье
- Синтез альдегидов Бодру – Чичибабина
- Реакция Фудзимото-Белло
- Литийорганические реагенты
- Реакция Сакурая
- Аллирование, опосредованное индием
- Алкинилирование
Ссылки
[ редактировать ]- ^ Jump up to: а б Смит, Майкл Б.; Марч, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Глава 19: Карбоновые кислоты . Органическая химия 4e Кэри. mhhe.com
- ^ Jump up to: а б с Уэллетт, Роберт Дж.; Рон, Дж. Дэвид (1 января 2014 г.), Уэллетт, Роберт Дж.; Раун, Дж. Дэвид (ред.), «15 – Спирты: реакции и синтез» , Органическая химия , Бостон: Elsevier, стр. 491–534, doi : 10.1016/b978-0-12-800780-8.00015-2 , ISBN 978-0-12-800780-8 , получено 6 ноября 2023 г.
- ^ Ширли, Д.А. (1954). «Синтез кетонов из галогенангидридов и металлоорганических соединений магния, цинка и кадмия». Орг. Реагировать. 8 : 28–58.
- ^ Гурин, Д.М. (1991). «Карбанионы щелочных и щелочноземельных катионов: (ii) Селективность реакций присоединения карбонила». Трост , BM ; Флеминг, И. (ред.). Комплексный органический синтез, Том 1: Дополнения к π-связям C—X, Часть 1 . Эльзевир Наука . стр. 49–75. дои : 10.1016/B978-0-08-052349-1.00002-0 . ISBN 978-0-08-052349-1 .
- ^ текст, Академия наук (Франция) Автор (1 января 1900 г.). «Еженедельные отчеты сессий Академии наук / издаваемые... бессменными секретарями» . Галлика . Проверено 23 апреля 2023 г.
- ^ Гриньяр, В. (1900). «О некоторых новых металлоорганических соединениях магния и их применении в синтезе спиртов и углеводородов» . Счет Возвращает . 130 :1322–25.
- ^ ИЮПАК. Сборник химической терминологии, 2-е изд. («Золотая книга»). Составлено А.Д. Макнотом и А. Уилкинсоном. Научные публикации Блэквелла, Оксфорд (1997). ISBN 0-9678550-9-8 . два : 10.1351/goldbook .
- ^ Jump up to: а б «Реакция Гриньяра | Индекс Merck Online» . www.rsc.org . Проверено 23 апреля 2023 г.
- ^ Маруяма, К.; Катагири, Т. (1989). «Механизм реакции Гриньяра». Дж. Физ. Орг. Хим . 2 (3): 205–213. дои : 10.1002/poc.610020303 .
- ^ Эшби, ЕС; Гоэл, AB (август 1981 г.). «Прямые доказательства, подтверждающие единый путь переноса электронов при восстановлении кетонов первичными, вторичными и третичными реагентами Гриньяра» . Журнал Американского химического общества . 103 (16): 4983–4985. дои : 10.1021/ja00406a070 . ISSN 0002-7863 .
- ^ Пельтцер, Рафаэль Матиас; Гаусс, Юрген; Эйзенштейн, Одиль; Каселла, Микеле (12 февраля 2020 г.). «Реакция Гриньяра – разгадка химической загадки» . Журнал Американского химического общества . 142 (6): 2984–2994. дои : 10.1021/jacs.9b11829 . hdl : 10852/83918 . ISSN 0002-7863 . ПМИД 31951398 . S2CID 210709021 .
- ^ Кэри, Фрэнсис А. «Реагент Гриньяра» . Британника .
- ^ Германн, Андреас; Сеймен, Рана; Бригер, Люк; Кляйнхайдер, Йоханнес; Грабе, Бастиан; Хиллер, Вольф; Строманн, Карстен (2023). «Комплексное исследование повышенной реакционной способности реагентов Турбо-Гриньяра*» . Международное издание «Прикладная химия» . 62 (25). дои : 10.1002/anie.202302489 . S2CID 257765567 .
- ^ Вудворд, Саймон (1 января 2000 г.). «Расшифровка реакционной способности« черного ящика », которая представляет собой химию присоединения органокупратного конъюгата» . Обзоры химического общества . 29 (6): 393–401. дои : 10.1039/B002690P . ISSN 1460-4744 .