Карбен Фишера
Карбен Фишера представляет собой тип карбенового комплекса переходного металла , который представляет собой металлоорганическое соединение, содержащее двухвалентный органический лиганд . В карбене Фишера карбеновый лиганд представляет собой σ-донорный π-акцепторный лиганд. Поскольку π-обратное донорство от металлического центра обычно слабое, карбеновый углерод является электрофильным .
Карбены Фишера названы в честь Эрнста Отто Фишера .
Структура
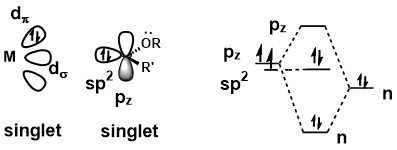
[ редактировать ]Металлокарбеновый комплекс можно считать карбеном Фишера, когда карбен находится в синглетном состоянии. Делокализация неподеленной пары от заместителя на углероде карбена повышает энергию p z -орбитали, тем самым вынуждая два электрона карбена оставаться электронной парой. Связь между карбеном и металлическим центром предполагает сильное донорство σ от sp. 2 орбитали на пустую d-орбиталь металлического центра и слабую обратную передачу π от металлического центра на пустую p z- орбиталь. Поскольку донорство π слабое, карбеновый углерод имеет электрофильную природу. [ 1 ]
Из-за этого связующего свойства карбены Фишера часто имеют:
- металлоцентр с низкой степенью окисления
- средние и поздние переходные металлы Fe(0), Mo(0), Cr(0)
- π-акцепторные металлические лиганды
- π-донорные заместители при карбеновом атоме, такие как алкокси- и алкилированные аминогруппы.
Подготовка
[ редактировать ]Наиболее распространенной стратегией получения карбена Фишера является реакция карбонильного комплекса металла с литийорганическими соединениями . Соответствующая структура, подобная еноляту лития , высоко стабилизирована и, следовательно, должна быть подавлена высокоэлектрофильным алкилирующим реагентом, таким как соль Меервейна . [ 2 ] Алкилирование MeI можно осуществить с помощью системы фазового переноса. [ 3 ] В альтернативном варианте катион лития можно заменить катионом тетраалкиламмония с получением более реакционноспособного енолята. Эту соль тетраалкиламмония можно ацилировать с образованием высокоэлектрофильного смешанного ангидрида, подобного карбену Фишера, который может подвергаться нуклеофильному замещению спиртом. [ 4 ]
Карбены Фишера с α-водородом получают реакцией карбонильного аниона металла с формамидом . Обработка промежуточного продукта избыточным количеством триметилсилилхлорида дает именно эту группу карбенового комплекса Фишера. [ 5 ]
Разработка карбенов Фишера
[ редактировать ]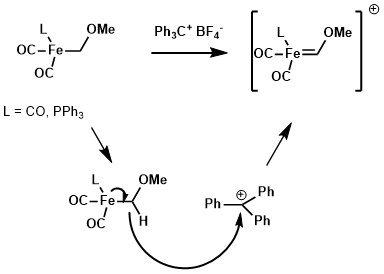
С помощью подходящего реагента для отделения гидрида, такого как тритильный катион , гидрид на алкильном лиганде металлокомплекса можно отделить с образованием карбена Фишера. [ 6 ]
Декарбонилирование из нестабилизированного металлического карбеноида.
[ редактировать ]Недавно исследователи в Испании сообщили, что карбен Фишера может быть эффективно получен методом декарбонилирования металлического карбеноида, полученного из стабилизированного диазосоединения . [ 7 ]

Реактивность
[ редактировать ]Карбонилоподобная реакционная способность
[ редактировать ]Карбеновый углерод карбена Фишера имеет электрофильную природу. Таким образом, карбены Фишера проявляют аналогичную реакционную способность по сравнению с карбонильными соединениями . Многие реакции можно понять, используя карбоксильную эквивалентную структуру, такую как переэтерификация , присоединение Михаэля и альдольная реакция . Фрагмент Cr(CO) 5 представляет собой сильную электроноакцепторную группу, делающую α-протон очень кислотным. Карбен метоксихрома с метильной боковой цепью имеет pK a 12,5 в водном ацетонитриле (объемное соотношение 1:1). [ 8 ] [ 9 ] Для сравнения, метилацетат имеет pK a 25,6, что демонстрирует сильную электроноакцепторную природу фрагмента Cr(CO) 5 .
Сильная электроноакцепторная природа карбенов Фишера также отражается во многих реакциях. Например, реакция Дильса-Альдера между метилакрилатом и изопреном завершается за 7 дней при комнатной температуре с низкой селективностью по пара-мета. С другой стороны, карбеновый аналог Фишера закончился за 3 часа при комнатной температуре с гораздо более высокой селективностью по пара-мета. [ 10 ]
Уротропин , слабый нуклеофил, может участвовать в присоединении Михаэля к алкинилкарбену Фишера, давая интересный продукт двойного присоединения. [ 11 ]
Енолятоподобная структура, полученная депротонированием карбена Фишера, может быть алкилирована. Однако, поскольку карбанион высоко стабилизирован, реактивный алкилирующий реагент, такой как метилфторсульфонат («магический метиловый реагент») или метилбромацетат . необходим [ 12 ] [ 13 ]
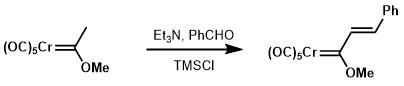
Альдольная конденсация карбенов Фишера может быть достигнута с использованием гораздо более слабых оснований по сравнению с его карбонильным аналогом, таким как триэтиламин . [ 14 ] [ 15 ]
Деметаллизация
[ редактировать ]Карбены Фишера можно окислить до соответствующих карбонильных соединений с использованием мягких окислителей, таких как нитрат церия-аммония (CAN). [ 16 ]
Если боковая цепь карбена Фишера содержит α-протон, она может быть обратимо депротонирована слабым основанием, таким как пиридин . Это облегчает образование гидридов хрома, которые могут подвергаться восстановительному элиминированию с образованием эфира цисенола . [ 17 ]
Фотохимические свойства карбенов Фишера
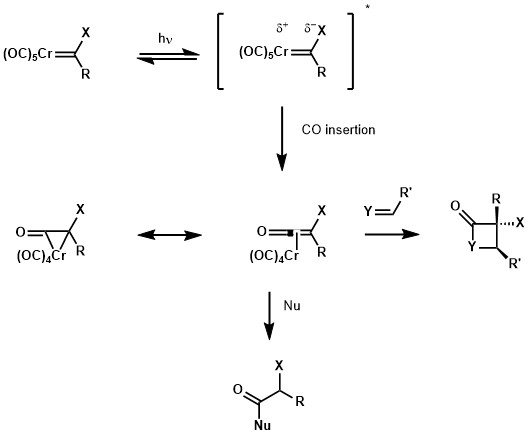
[ редактировать ]УФ -видимый спектр карбена Фишера показывает полосу переноса заряда от металла к лиганду в ближнем ультрафиолете. С одной стороны, это возбуждение переводит электрон с металлоцентрической орбитали на лиганд-центрированную орбиталь, делая карбеновый углерод более богатым электронами. С другой стороны, металлоцентр, уже обедненный электронами из-за карбонильных лигандов, становится еще более бедным электронами, что облегчает мигрирующее присоединение к лиганду CO. Эта мигрирующая вставка дает металлациклопропанон хрома, который представляет собой резонансную форму металлированного кетена . Обладая реакционной способностью кетена, эти виды могут захватываться несколькими нуклеофилами, такими как спирты и амины, или могут реагировать в результате [2+2] циклоприсоединения с алкенами, иминами или альдегидами, образуя соответствующие аддукты циклобутан, β-лактам и β-лактон. [ 18 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Крэбтри, Роберт (18 июля 2019 г.). Металлоорганическая химия переходных металлов 7-е издание . Джон Уайли и сыновья. ISBN 978-1119465881 .
- ^ Дётц, Карл Хайнц (август 1984 г.). «Карбеновые комплексы в органическом синтезе [Новые методы синтеза (47)]». Angewandte Chemie International Edition на английском языке . 23 (8): 587–608. дои : 10.1002/anie.198405871 .
- ^ Хой, Томас Р.; Чен, Кецзян; Вивиан, Джеймс Р. (июль 1993 г.). «Получение карбеновых комплексов Фишера алкилированием ацилметаллатов алкилиодидами». Металлоорганические соединения . 12 (7): 2806–2809. дои : 10.1021/om00031a056 .
- ^ Бейтс, Родерик (2012). Органический синтез с использованием переходных металлов (2-е изд.). Чичестер, Западный Суссекс: Уайли. ISBN 9781119978947 .
- ^ Бейтс, Родерик (2012). Органический синтез с использованием переходных металлов (2-е изд.). Чичестер, Западный Суссекс: Уайли. ISBN 9781119978947 .
- ^ Дётц, Карл Хайнц (август 1984 г.). «Карбеновые комплексы в органическом синтезе [Новые методы синтеза (47)]». Angewandte Chemie International Edition на английском языке . 23 (8): 587–608. дои : 10.1002/anie.198405871 .
- ^ Альварес, Мэри; Бесора, Мэри; Молина, Фрэнсис; Масерас, Фелиу; Бельдеррейн, Томас Р.; Перес, Питер Дж. (31 марта 2021 г.). «Два медь-карбена из одного диазосоединения». Журнал Американского химического общества . 143 (12): 4837–4843. дои : 10.1021/jacs.1c01483 . hdl : 10272/19704 . ПМИД 33733762 .
- ^ Бернаскони, Клод Ф.; Сунь, Вэйтао (1 апреля 1997 г.). «Физико-органическая химия карбеновых комплексов переходных металлов. 8.1. Кинетическая и термодинамическая кислотность алкоксиалкилкарбеновых пентакарбонильных комплексов Cr, Mo и W в водном ацетонитриле. Зависимость от металла, алкильной группы и алкоксигруппы». Металлоорганические соединения . 16 (9): 1926–1932. дои : 10.1021/om960936 .
- ^ Бернаскони, Клод Ф.; Лейес, Акилес Э.; Рагейнс, Марк Л.; Ши, Ян; Ван, Хуан; Вульф, Уильям Д. (1 сентября 1998 г.). «Физико-органическая химия карбеновых комплексов переходных металлов. 14.1. Термодинамические измерения кислотности карбеновых комплексов Фишера в ацетонитриле». Журнал Американского химического общества . 120 (34): 8632–8639. дои : 10.1021/ja980608w .
- ^ Вульф, Уильям Д.; Ян, Доминик К. (октябрь 1983 г.). «Реакции Дильса-Альдера карбеновых комплексов Фишера». Журнал Американского химического общества . 105 (22): 6726–6727. дои : 10.1021/ja00360a037 .
- ^ Ауманн, Рудольф; Хинтердинг, Питер; Крюгер, Карл; Годдард, Ричард (октябрь 1993 г.). «Органические синтезы с комплексами переходных металлов LXV. Альдегиды путем гидролиза связи M = C комплексов алкоксикарбен-хром с водой / уротропином. Двухъядерный мостиковый (β-амино)винилкарбен-хром комплекс путем фрагментации уротропина». Журнал металлоорганической химии . 459 (1–2): 145–149. дои : 10.1016/0022-328X(93)86066-Q .
- ^ Кейси, Чарльз П.; Боггс, Роджер А.; Андерсон, Рональд Л. (декабрь 1972 г.). «Генерация и реакции анионов альфа на карбеновый атом углерода комплексов переходный металл-карбен». Журнал Американского химического общества . 94 (25): 8947–8949. дои : 10.1021/ja00780a073 .
- ^ Кейси, Чарльз П.; Андерсон, Рональд Л. (1974). «Реакции сопряженных оснований карбеновых комплексов металлов с эксоксидами и с α-бромэфирами». Журнал металлоорганической химии . 73 (2): C28–C30. дои : 10.1016/S0022-328X(00)85646-6 .
- ^ Ауманн, Рудольф; Хайнен, Генрих (апрель 1987 г.). «Органический синтез с комплексами переходных металлов, 211) 1-хрома-1,3-бутадиены и 1-хрома-1,3,5-гексатриены из (CO)5Cr=C(OC2H5)CH3 карбонильным олефинированием триэтиламином/хлортриметилсиланом» . Химические отчеты . 120 (4): 537–540. дои : 10.1002/cber.19871200413 .
- ^ Кейси, Чарльз П.; Брунсволд, Уильям Р. (декабрь 1975 г.). «Синтез α-метилен-γ-бутиролактона через карбеновые комплексы переходных металлов». Журнал металлоорганической химии . 102 (2): 175–183. дои : 10.1016/S0022-328X(00)88585-X .
- ^ Дётц, Карл Хайнц (август 1984 г.). «Карбеновые комплексы в органическом синтезе [Новые методы синтеза (47)]». Angewandte Chemie International Edition на английском языке . 23 (8): 587–608. дои : 10.1002/anie.198405871 .
- ^ Содерберг, Бьёрн К.; Лю, Цзянь; Болл, Томас В.; Турбевилл, Майкл Дж. (август 1997 г.). «Термическое разложение комплексов пентакарбонила (1-ацилоксиалкилиден) хрома (0): образование эфиров Z-енола». Журнал органической химии . 62 (17): 5945–5952. дои : 10.1021/jo962197c .
- ^ Хегедус, Луи С. (март 1997 г.). «Фотохимия карбенового комплекса хрома в органическом синтезе». Тетраэдр . 53 (12): 4105–4128. дои : 10.1016/S0040-4020(96)01186-6 .