Димеризация (химия)
Эта статья нуждается в дополнительных цитатах для проверки . ( апрель 2009 г. ) |
В химии димеризация — это процесс соединения двух одинаковых или сходных молекулярных образований посредством связей . Возникающие в результате связи могут быть как сильными, так и слабыми. Многие симметричные химические соединения описываются как димеры , даже если мономер неизвестен или очень нестабильен. [1]
Термин гомодимер используется, когда две субъединицы идентичны (например, А-А), и гетеродимер, когда они не идентичны (например, А-В). Обратная димеризация часто называется диссоциацией . Когда два противоположно заряженных иона объединяются в димеры, их называют парами Бьеррума . [2] в честь датского химика Нильса Бьеррума .
Нековалентные димеры [ править ]

Безводные карбоновые кислоты образуют димеры за счет водородных связей кислого водорода и карбонильного кислорода. Например, уксусная кислота образует димер в газовой фазе, где мономерные звенья удерживаются вместе водородными связями . [3] Многие ОН-содержащие молекулы образуют димеры, например димер воды .
Эксимеры и эксиплексы представляют собой возбужденные структуры с коротким временем жизни. Например, благородные газы не образуют стабильных димеров, но образуют эксимеры Ar 2 *, Kr 2 * и Xe 2 * под высоким давлением и электростимуляцией. [4]
Ковалентные димеры [ править ]

Молекулярные димеры часто образуются в результате реакции двух идентичных соединений, например: 2А → А-А . В этом примере говорят, что мономер «А» димеризуется с образованием димера « А-А ». Примером является диаминокарбен , который димеризуется с образованием тетрааминоэтилена :
Карбены обладают высокой реакционной способностью и легко образуют связи.
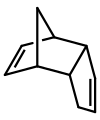
Дициклопентадиен представляет собой асимметричный димер двух молекул циклопентадиена , которые прореагировали в реакции Дильса-Альдера с образованием продукта. При нагревании он «раскалывается» (претерпевает ретрореакцию Дильса-Альдера) с образованием идентичных мономеров:
Многие неметаллические элементы встречаются в виде димеров: водород , азот , кислород и галогены (т.е. фтор , хлор , бром и йод ). Благородные газы могут образовывать димеры, связанные связями Ван-дер-Ваальса , например дигелий или диаргон . Ртуть встречается в виде катиона ртути(I) ( Hg 2+ 2 ), формально димерный ион. Другие металлы могут образовывать часть димеров в паровой фазе. Известные металлические димеры включают дилитий ( Li 2 ), динатрий ( Na 2 ), дикалий ( К 2 ), дирубидий ( Rb 2 ) и дицезий ( Сс 2 ). Такие элементарные димеры представляют собой гомоядерные двухатомные молекулы .
Многие небольшие органические молекулы, особенно формальдегид , легко образуют димеры. Димер формальдегида ( CH 2 O ) — диоксетан ( С 2 Н 4 О 2 ).
Бораны ( BH 3 ) встречается в виде димера диборана ( B 2 H 6 ), из-за высокой льюисовской кислотности борного центра .
Полимерная химия [ править ]
В контексте полимеров «димер» также относится к степени полимеризации 2, независимо от стехиометрии или реакции конденсации .
Одним из случаев, когда это применимо, является дисахарид . Например, целлобиоза представляет собой димер глюкозы , хотя в результате реакции образования образуется вода :
При этом образующийся димер имеет стехиометрию, отличную от исходной пары мономеров.
дисахариды не обязательно должны состоять из одних и тех же моносахаридов Чтобы считаться димерами, . Примером является сахароза , димер фруктозы и глюкозы, который подчиняется тому же уравнению реакции, что представлено выше.
Аминокислоты также могут образовывать димеры, которые называются дипептидами . Примером является глицилглицин , состоящий из двух молекул глицина, соединенных пептидной связью . Другие примеры включают аспартам и карнозин .
Неорганические димеры [ править ]
Многие молекулы и ионы описываются как димеры, даже если мономер неуловим.
13 Димеры группы
Бораны [ править ]

Диборан (B 2 H 6 ) представляет собой неорганический димер борана . B 2 H 6 существует в виде структуры, в которой два атома водорода соединяют два атома бора . [5]
Алюминий [ править ]

Соединения триалкилалюминия могут существовать как в виде мономеров, так и в виде димеров, в зависимости от стерической массы присоединенных групп. Например, триметилалюминий существует в виде димера, но тримезитилалюминий принимает мономерную структуру. [6]
димеры Биохимические
Пиримидиновые димеры [ править ]
Димеры пиримидина (также известные как димеры тимина) образуются в результате фотохимической реакции из пиримидиновых оснований ДНК при воздействии ультрафиолетового света. [6] Это перекрестное связывание вызывает мутации ДНК , которые могут быть канцерогенными и вызывать рак кожи . [6] Когда пиримидиновые димеры присутствуют , они могут блокировать полимеразы , снижая функциональность ДНК до тех пор, пока она не будет восстановлена. [6]
Белковые димеры [ править ]

Белковые димеры возникают в результате взаимодействия двух белков , которые могут взаимодействовать дальше с образованием более крупных и сложных олигомеров . [7] Например, тубулин образуется в результате димеризации α-тубулина и β-тубулина , и этот димер затем может полимеризоваться дальше с образованием микротрубочек . [8] Для симметричных белков более крупный белковый комплекс может быть разбит на более мелкие идентичные белковые субъединицы , которые затем димеризуются, чтобы уменьшить генетический код, необходимый для создания функционального белка. [7]
с G-белком связанные , Рецепторы
(GPCR) , как самое большое и разнообразное семейство рецепторов в геноме человека, Рецепторы , связанные с G-белком широко изучались, а недавние исследования подтвердили их способность образовывать димеры. [9] Димеры GPCR включают как гомодимеры, так и гетеродимеры, образованные из родственных членов семейства GPCR. [10] Хотя это и не все, некоторые GPCR для функционирования требуют димеризации, например, рецептор ГАМК B , что подчеркивает важность димеров в биологических системах. [11]

Рецептор тирозинкиназы [ править ]
Как и в случае с рецепторами, связанными с G-белком, димеризация необходима для того, чтобы рецепторные тирозинкиназы (RTK) выполняли свою функцию по передаче сигнала , влияя на множество различных клеточных процессов. [12] RTK обычно существуют в виде мономеров, но претерпевают конформационные изменения при связывании лиганда , что позволяет им димеризоваться с близлежащими RTK. [13] [14] Димеризация активирует цитоплазматические киназные домены , которые отвечают за дальнейшую передачу сигнала . [12]
См. также [ править ]
Ссылки [ править ]
- «Определение «Золотой книги» ИЮПАК» . дои : 10.1351/goldbook.D01744 . S2CID 242984652 . Проверено 30 апреля 2009 г.
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь )
- ^ «Димеризация» .
- ^ Адар, Рам М.; Маркович, Томер; Андельман, Дэвид (17 мая 2017 г.). «Пары Бьеррума в ионных растворах: подход Пуассона-Больцмана». Журнал химической физики . 146 (19): 194904. arXiv : 1702.04853 . Бибкод : 2017JChPh.146s4904A . дои : 10.1063/1.4982885 . ISSN 0021-9606 . ПМИД 28527430 . S2CID 12227786 .
- ^ Карл, Дж.; Броквей, Лоу (1944). «Электронографическое исследование мономеров и димеров муравьиной, уксусной и трифторуксусной кислот и димера ацетата дейтерия 1» . Журнал Американского химического общества . 66 (4): 574–584. дои : 10.1021/ja01232a022 . ISSN 0002-7863 .
- ^ Биркс, Дж. Б. (1 августа 1975 г.). «Эксимеры» . Отчеты о прогрессе в физике . 38 (8): 903–974. дои : 10.1088/0034-4885/38/8/001 . ISSN 0034-4885 . S2CID 240065177 .
- ^ Шрайвер, Дювард (2014). Неорганическая химия (6-е изд.). WH Фриман и компания. стр. 306–307. ISBN 9781429299060 .
- ^ Jump up to: Перейти обратно: а б с д Шрайвер, Дювард (2014). Неорганическая химия (6-е изд.). WH Фриман и компания. стр. 377–378. ISBN 9781429299060 .
- ^ Jump up to: Перейти обратно: а б Марианаягам, Нилан Дж.; Сунде, Маргарет; Мэтьюз, Жаклин М. (2004). «Сила двух: димеризация белков в биологии» . Тенденции биохимических наук . 29 (11): 618–625. дои : 10.1016/j.tibs.2004.09.006 . ISSN 0968-0004 . ПМИД 15501681 .
- ^ Купер, Джеффри М. (2000). «Микротрубочки» . Клетка: молекулярный подход. 2-е издание .
- ^ Фарон-Гуречка, Агата; Шляхта, Марта; Коласа, Магдалена; Солич, Джоанна; Гурецкий, Анджей; Кусьмидер, Мацей; Журавек, Дариуш; Дзедзицка-Васильевска, Марта (01.01.2019), Шукла, Арун К. (редактор), «Глава 10 - Понимание димеризации GPCR» , Методы клеточной биологии , Рецепторы, связанные с G-белком, Часть B, 149 , Academic Press : 155–178, doi : 10.1016/bs.mcb.2018.08.005 , ISBN 9780128151075 , PMID 30616817 , S2CID 58577416 , получено 27 октября 2022 г.
- ^ Риос, CD; Джордан, бакалавр; Гомес, И.; Деви, Луизиана (1 ноября 2001 г.). «Димеризация рецептора, связанного с G-белком: модуляция функции рецептора» . Фармакология и терапия . 92 (2): 71–87. дои : 10.1016/S0163-7258(01)00160-7 . ISSN 0163-7258 . ПМИД 11916530 .
- ^ Лозе, Мартин Дж (01 февраля 2010 г.). «Димеризация в подвижности и передаче сигналов GPCR» . Современное мнение в фармакологии . ГПКР. 10 (1): 53–58. дои : 10.1016/j.coph.2009.10.007 . ISSN 1471-4892 . ПМИД 19910252 .
- ^ Jump up to: Перейти обратно: а б Хаббард, Стеван Р. (1 апреля 1999 г.). «Структурный анализ рецепторов тирозинкиназ» . Прогресс биофизики и молекулярной биологии . 71 (3): 343–358. дои : 10.1016/S0079-6107(98)00047-9 . ISSN 0079-6107 . ПМИД 10354703 .
- ^ Леммон, Марк А.; Шлезингер, Джозеф (25 июня 2010 г.). «Передача сигналов клетками рецепторными тирозинкиназами» . Клетка . 141 (7): 1117–1134. дои : 10.1016/j.cell.2010.06.011 . ISSN 0092-8674 . ПМК 2914105 . ПМИД 20602996 .
- ^ Леммон, Марк А.; Шлезингер, Джозеф; Фергюсон, Кэтрин М. (01 апреля 2014 г.). «Семейство EGFR: не совсем прототипические тирозинкиназы рецепторов» . Перспективы Колд-Спринг-Харбор в биологии . 6 (4): а020768. doi : 10.1101/cshperspect.a020768 . ISSN 1943-0264 . ПМЦ 3970421 . ПМИД 24691965 .


