Синтез индола Неницеску
| Синтез индола Неницеску | |
|---|---|
| Назван в честь | Костин Ненитеску |
| Тип реакции | Реакция образования кольца |
Синтез индола Неницеску представляет собой химическую реакцию , в ходе которой образуются производные 5-гидрокси индола из бензохинона и эфиров β-аминокротоновой кислоты.

Эта реакция была названа в честь ее первооткрывателя Костина Ненишеску , который впервые сообщил о ней в 1929 году. [1] Его можно осуществить с рядом различных комбинаций R-групп, которые включают метильные, метокси-, этильные, пропильные и H-заместители. [2] Существует также твердофазный вариант, в котором реакция происходит на каркасе из сильно сшитого полимера. [3] Синтез особенно интересен тем, что индолы являются основой ряда биохимически важных молекул, включая нейротрансмиттеры и новый класс противоопухолевых соединений. [4]
Механизм
[ редактировать ]Механизм реакции Неницеску состоит из присоединения Михаэля с последующей нуклеофильной атакой пи- связи енамина и последующим отщеплением . [5]

Реакция была впервые опубликована Неницеску в 1929 году. [1] и с тех пор был уточнен Allen et al. [2] В своей публикации 1996 года Аллен и его коллеги исследовали влияние различных заместителей в исходном бензохиноне на расположение конечного продукта. Эти стерические эффекты также доказали, что один из двух предложенных в настоящее время механизмов более вероятен, чем другой, что привело к публикации механизма, показанного выше.
Условия
[ редактировать ]Предварительное исследование, проведенное Katkevica et al. исследовал условия реакции синтеза Неницеску и сообщил о поведении реакции, когда она протекает в различных растворителях. [6] Их результаты показали, что реакция лучше всего протекает в высокополярном растворителе, и были предложены дальнейшие кинетические исследования, включающие изменение субстрата, реагентов, растворителей и присутствия кислот и оснований Льюиса. Два года спустя Вележева и др. продолжил сообщать об альтернативной версии синтеза с использованием катализатора на основе кислоты Льюиса . [7] Они сообщают, что катализирующий эффект возникает в результате активации енамина через комплекс дикетодиенамин-ZnCl 2 .
Однако, несмотря на улучшение условий, традиционный синтез Неницеску не был пригоден для использования в промышленных масштабах из-за относительно низкого выхода и полимеризации в нормальных условиях реакции. Первоначально считалось, что бензохинон необходимо использовать в 100% избытке, чтобы довести реакцию до завершения в таком масштабе, но Huang et al. сообщили, что превышение на 20–60% является наиболее эффективным. [8] Кроме того, они сообщили, что для идеальных условий для крупномасштабной реакции должно быть мольное соотношение между бензохиноном и этил-3-аминокротонатом 1: 1,2-1,6, и реакция должна проходить при комнатной температуре. Этих условий достаточно для производства партий массой 100 кг и более.
Вариации и связанные с ними реакции
[ редактировать ]Одним из наиболее распространенных вариантов реакции Неницеску является твердофазный вариант. Об этой реакции впервые сообщили Ketcha et al. , показано ниже. [3]
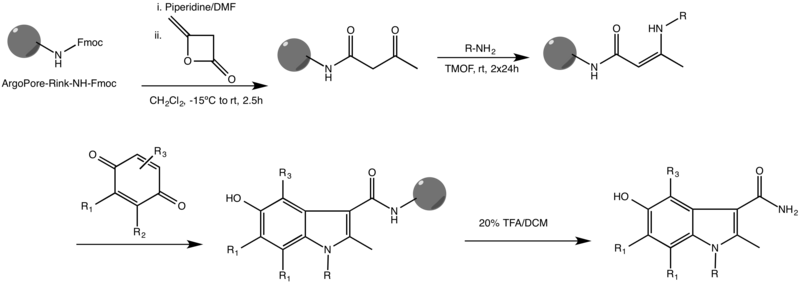
Он происходит на смоле ArgoPore®-Rink-NH-Fmoc с высокой степенью поперечных связей и действует с различными заместителями в обоих реагентах. Сообщалось также о других твердофазных синтезах индола, в некоторых из которых используются различные каркасы и металлические катализаторы для доведения реакции до завершения.
Существует также множество других реакций, которые приводят к образованию того же индольного скелета. В обзорной статье Taber et al. разделили эти реакции на девять основных типов синтеза индола: Фишера , Мори, Хемецбергера , Бухвальда , Сундберга, Маделунга , Неницеску, ван Лейзена и Канемацу. [9]
Приложения
[ редактировать ]Скелет 5-гидроксииндола является основой ряда биохимически важных молекул. Среди них серотонин , нейромедиатор; индометацин , нестероидное противовоспалительное средство; L-761066, ингибитор ЦОГ-2 ; и LY311727, ингибитор секреторной фосфолипазы. [3] В настоящее время одним из наиболее интересных применений синтеза Неницеску является его способность производить предшественник противоопухолевых соединений. Этот синтез, о котором сообщалось в 2006 году, включает реакцию 1,4,9,10-антрадихинона с различными енаминами. [4] Продукты этой реакции составляют новый класс ведущих структур для разработки противораковых лекарств.
Ссылки
[ редактировать ]- ^ Jump up to: а б Неницеску, CD (1929). «Производные 2-метил-5-гидроксииндола». Бык. Соц. Хим. Румыния . 11 : 37–43.
- ^ Jump up to: а б Аллен, Г.; Пидакс, К.; Вайс, М. (5 июня 1996 г.). «Антибиотики Митомицина. Синтетические исследования». Дж. Ам. хим. Соц. 88 (11): 2536–2544. дои : 10.1021/ja00963a032 . ПМИД 5941382 .
- ^ Jump up to: а б с Кетча, Дэниел М.; Уилсон, LJ; Портлок, Делавэр (2000). «Твердофазный синтез индола Неницеску». Буквы тетраэдра . 41 (33): 6253–6257. дои : 10.1016/S0040-4039(00)00697-3 .
- ^ Jump up to: а б Шенк, Лотар Вернер; Куна, К.; Франк, В.; Альберт, А.; Аше, К.; Куклаендер, У. (10 января 2006 г.). «1,4,9,10-антрадихинон как предшественник противоопухолевых соединений». Биоорганическая и медицинская химия . 14 (10): 3599–3614. дои : 10.1016/j.bmc.2006.01.026 . ПМИД 16458517 .
- ^ Ли, Цзе Джек (2009). Имя Реакции, 4-е изд . Берлин: Springer-Verlag. стр. 391–392 . ISBN 978-3642010521 .
- ^ Каткевича, Дейз; Трапенсьерис, П.; Боман, А.; Кальвинс, И.; Лундштедт, Т. (2004). «Реакция Неницеску: первоначальный отбор экспериментальных условий для улучшения выхода модельной реакции». Дж. Хемометрика . 18 (34): 1883–187. дои : 10.1002/cem.863 . S2CID 95058789 .
- ^ Вельхеева Валерия С.; Соколов А.И.; Корниенко А.Г.; Лысенко, К.А.; Нелюбина Ю.В.; Годовиков И.А.; Перегудов А.С.; Миронов А.Ф. (15 сентября 2008 г.). «Орл кислоты Льюиса в синтезе индола Неницеску». Буквы тетраэдра . 49 (50): 7106–7109. дои : 10.1016/j.tetlet.2008.09.087 .
- ^ Хуан, Юнь-Шэн; Чжан, В.; Чжан, X.; Ван, Дж. (2010). «Производственный синтез 5-гидрокси-2-метил-1Н-индола». Исследования химических промежуточных продуктов . 36 (8): 975–983. дои : 10.1007/s11164-010-0210-x . S2CID 94168531 .
- ^ Табер, Дуглас Ф.; Тирунахари, ПК (21 июня 2011 г.). «Синтез индола: обзор и предлагаемая классификация» . Тетраэдр . 67 (38): 7195–7210. дои : 10.1016/j.tet.2011.06.040 . ПМЦ 4255418 . ПМИД 25484459 .