Винилология

В органической химии винилология — это передача электронных эффектов через систему сопряженных органических связей. [1] Эта концепция была введена в 1926 году Людвигом Кляйзеном для объяснения кислотных свойств формилацетона и родственных ему кетоальдегидов . Формалацетон, технически CH 3 (C=O)CH 2 CH=O , существует только в ионизированной форме. СН 3 (C-O − )=CH-CH=O или СН 3 (С=О)-СН=СН-О − . [2] Его прилагательная форма, винилологическая , используется для описания функциональных групп , в которых стандартные фрагменты группы разделены двойной связью углерод-углерод .
Например, карбоновая кислота определяется как карбонильная группа ( C=O ), непосредственно связанный с гидроксильной группой ( ОН ): O=C–OH. Винилологичная карбоновая кислота имеет виниловое звено ( −HC=CH- , винилен) между двумя группами, определяющими кислоту: O=C–C=C–OH. Обычный резонанс карбоксилата может распространяться через алкен винилологического карбоксилата. Аналогично, 3-диметиламиноакролеин является винилологичным амидным аналогом диметилформамида .
Из-за передачи электронной информации посредством конъюгации винилологические функциональные группы часто обладают « аналогичной » реакционной способностью или химическими свойствами по сравнению с исходной функциональной группой. Следовательно, винилология является полезной эвристикой для предсказания поведения систем, которые структурно схожи, но содержат промежуточные связи C=C, сопряженные с присоединенными функциональными группами. Например, ключевым свойством карбоновых кислот является их кислотность по Бренстеду . Простейшая карбоновая кислота — муравьиная кислота ( HC(=O)−OH ), представляет собой умеренно сильную органическую кислоту с ap K a 3,7. Мы могли бы ожидать, что винилологические карбоновые кислоты будут иметь аналогичную кислотность. Действительно, винилолог муравьиной кислоты, 2-формил-1-этен-1-ол, HC(=O)-CH=CH-OH имеет значительную бренстедовскую кислотность с расчетным p K a ~ 5–6. В частности, винилологические карбоновые кислоты являются существенно более сильными кислотами, чем типичные енолы (рКа ~ 12 ). Витамин С ( аскорбиновая кислота , см. ниже ) является биологически важным примером винилологической карбоновой кислоты.
Введение о- или п - фенилена (т.е. бензольного кольца в 1,2- или 1,4-ориентации) также приводит к некоторому сходству в реакционной способности (так называемой «фенилогии»), хотя эффект обычно слабее. поскольку сопряжение через арильное кольцо требует рассмотрения резонансных форм или промежуточных продуктов, в которых ароматичность . нарушается [3] [4]
Считается, что винилологические реакции происходят, когда орбитали двойных связей винильной группы и присоединенной электроноакцепторной группы (EWG; π-орбитали) выровнены и поэтому могут перекрываться и смешиваться (т. е. сопрягаться ). электронов Делокализация позволяет ЭРГ получить электронную плотность за счет участия сопряженной системы.
Винилогичная реактивность
[ редактировать ]Классическим примером винилологии является относительно высокая кислотность γ-водорода в СН 3 СН=CHC(O)R . Кислотность концевой метильной группы аналогична кислотности метилкетона. СН 3 С(О)R . [5]
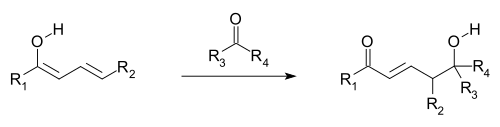
Винилогичные реакции также включают присоединение конъюгатов , когда нуклеофил реагирует на виниловом конце, аналогично присоединению нуклеофила к карбонилу метилкетона. В винилологическом варианте альдольной реакции электрофил (см . подвергается атаке нуклеофильного винилологичного енолята первое и следующее изображения). Винологичный енолят реагирует в концевом положении системы двойной связи (γ-углерод), а не в α-углероде, непосредственно примыкающем к карбонилу, как это происходит в случае простого енолята. Аллильные электрофилы часто реагируют винилологической атакой нуклеофила, а не прямым присоединением.
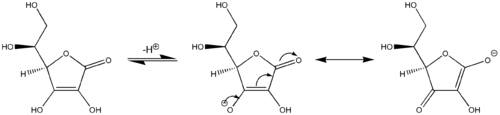
Еще один пример винилологической реакционной способности: аскорбиновая кислота (витамин С) ведет себя как винилологичная карбоновая кислота за счет участия ее карбонильного фрагмента, винильной группы внутри кольца и неподеленной пары гидроксильной группы, действующей как сопряженная система . Кислотность гидроксильного протона на конце винильной группы в аскорбиновой кислоте более сопоставима с типичной карбоновой кислотой, чем со спиртом , поскольку две основные резонансные структуры стабилизируют отрицательный заряд на сопряженном основании аскорбиновой кислоты (центральная и правая структуры на последнем изображении). ), аналогичный двум резонансным структурам, которые стабилизируют отрицательный заряд аниона, возникающий в результате удаления протона из простой карбоновой кислоты (см. первое изображение). Аналогично, производные сорбиновой кислоты , дополненные еще одним «виниловым» фрагментом, также демонстрируют винилологическое поведение.
Дальнейшее чтение
[ редактировать ]- Лиссабон, Марильда П.; Хоанг, Тунг Т.; Дадли, Грегори Б. (2011). «Тандемное нуклеофильное присоединение/фрагментация виниловых ацилтрифлатов: 2-метил-2-(1-оксо-5-гептинил)-1,3-дитиан» . Органические синтезы . 88 : 353. дои : 10.15227/orgsyn.088.0353 .
Ссылки
[ редактировать ]- ^ Винилогичная альдольная реакция: ценный, но недооцененный маневр по образованию углерод-углеродных связей Джованни Казираги, Франка Занарди, Джованни Аппендино и Глория Рассу Chem. Версия 2000 г .; 100(6) стр. 1929–1972 гг.; (Обзор) два : 10.1021/cr990247i
- ^ Об О-алкилпроизводных бензоилацетона и образующихся на их основе изоксазолах. (Ответ г-ну О. Вейганду.) Отчеты Немецкого химического общества (серии A и B), том 59, выпуск 2, дата: 10 февраля 1926 г., страницы: 144–153 Л. Клайзен. два : 10.1002/cber.19260590206
- ^ Ямасаки, Рю; Икеда, Хирокадзу; Масу, Хьюма; Адзумая, Исао; Сайто, Шиничи (07 октября 2012 г.). «Синтез и свойства фенилогичных амидов» . Тетраэдр . 68 (40): 8450–8456. дои : 10.1016/j.tet.2012.07.084 . ISSN 0040-4020 .
- ^ Лоуренс, Энтони Дж.; Хатчингс, Майкл Г.; Кеннеди, Алан Р.; Макдуалл, Джозеф Дж.В. (5 февраля 2010 г.). «Бензодифурантрион: стабильный фенилогичный енол» . Журнал органической химии . 75 (3): 690–701. дои : 10.1021/jo9022155 . ISSN 0022-3263 . ПМИД 20055373 .
- ^ Смит, Майкл Б.; Марч, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, стр. 633, ISBN 978-0-471-72091-1