дикарбонил
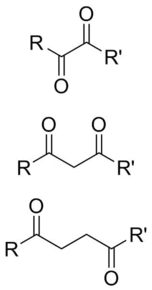
В органической химии дикарбонилом содержащую называют молекулу, два карбонила ( C=O ) группы . Хотя этот термин может относиться к любому органическому соединению , содержащему две карбонильные группы, более конкретно он используется для описания молекул, в которых оба карбонила находятся достаточно близко, чтобы их реакционная способность изменилась, например, 1,2-, 1,3- и 1,4-дикарбонилы. Их свойства часто отличаются от свойств монокарбонилов, поэтому их обычно считают собственными функциональными группами. Эти соединения могут иметь симметричные или несимметричные заместители на каждом карбониле, а также могут быть функционально симметричными (диальдегиды , дикетоны , диэфиры и т . д. ) или несимметричными (кетоэфиры, кетокислоты и т. д. ).
1,2-дикарбонилы
[ редактировать ]1,2-диальдегид
[ редактировать ]Единственный 1,2-диальдегид — глиоксаль . (ЧО) 2 . Как и многие алкилдиальдегиды, глиоксаль встречается почти исключительно в виде его гидрата и его олигомеров. Эти производные часто ведут себя так же, как альдегиды , поскольку гидратация обратима. Глиоксаль легко конденсируется с аминами . В результате таких реакций он является предшественником многих гетероциклов , например имидазолов .

1,2-Дикетоны
[ редактировать ]Основным дикетоном является диацетил , также известный как 2,3-бутандион. СН 3 С(О)С(О)СН 3 . 1,2-Дикетоны часто образуются в результате окисления (дегидрирования) диолов : [1]
2,3-Бутандион, 2,3-пентандион и 2,3-гександион содержатся в небольших количествах в различных продуктах питания. Их используют в качестве ароматических компонентов в безалкогольных напитках и хлебобулочных изделиях. [1] Бензил , (PhCO) 2 представляет собой соответствующее дифенильное производное.
Отличительной особенностью 1,2-дикетонов является длинная связь CC, соединяющая карбонильные группы. Это расстояние связи составляет около 1,54 Å по сравнению с 1,45 Å для соответствующей связи в 1,3-бутадиене . Эффект объясняется отталкиванием частичных положительных зарядов карбонильных атомов углерода. [2]
1,2-Дикетоны конденсируются со многими бифункциональными нуклеофилами, такими как мочевина и тиомочевина, с образованием гетероциклов. Конденсация с ароматическими аминами дает дикетимин ( (RC=NAr) 2 ).
В случае 1,2-циклогександиона и 1,2-циклопентандиона енол примерно на 1-3 ккал/моль более стабилен , чем дикето-форма. [3]
орто-хинон , C 4 H 4 (CO) 2 является родителем большого семейства 1,2-дикетонов.
1,2-кетоальдегиды
[ редактировать ]
Хорошо известное соединение этого класса — метилглиоксаль . CH 3 C(O)CHO , также известный как пирувальдегид. Эти соединения также известны как 2-оксоальдегиды. [4] или α-кетоальдегиды.
1,2-диэфиры и двухосновные кислоты
[ редактировать ]Щавелевая кислота и ее эфиры определяют это семейство соединений. Двухкислотную кислоту производят в промышленных масштабах путем окисления отходов сахара. Он встречается в природе (как конъюгированное основание), особенно у растений вида Oxalis . Конденсация диэфиров с диаминами дает циклические диамиды.
α-кето- и формилкарбоновые кислоты
[ редактировать ]
α-Кетокислоты и -эфиры хорошо известны. Пировиноградная кислота ( англ. CH 3 C(O)CO 2 H ) является исходной α-кетокислотой. Его сопряженное основание пируват ( CH 3 C(O)CO - 2 ), является компонентом цикла трикарбоновых кислот и продуктом метаболизма глюкозы ( гликолиза ). Соответствующей альдегидной кислотой является глиоксалевая кислота ( HC(O)CO 2 H ).
1,3-дикарбонилы
[ редактировать ]1,3-диальдегиды
[ редактировать ]Исходным 1,3-диальдегидом является малоновый диальдегид ( CH 2 (CHO) 2 ), β-дикарбонил. Как и большинство диальдегидов, он редко встречается как таковой. Вместо этого с ним обращаются почти исключительно как с его гидратом, метилацеталем и его олигомерами. Эти производные часто ведут себя как родительские. Известно множество 2-замещенных производных. Их часто получают алкилированием енолята малонового диальдегида.
1,3-Дикетоны
[ редактировать ]1,3-Дикетоны также называют β-дикетонами. Важным членом является ацетилацетон , СН 3 С(О)СН 2 С(О)СН 3 . Димедон представляет собой циклический 1,3-дикетон. 1,3-Индандион представляет собой циклический 1,3-дикетон, конденсированный с бензольным кольцом. Ацетилацетон получают в промышленности термической перегруппировкой изопропенилацетата. [1] Другим циклическим 1,3-дикетоном является 2,2,4,4-тетраметилциклобутандион , который является предшественником полезного диола .
1,3-Дикетоны часто таутомеризуются с образованием енола и кетола. Обычно они существуют преимущественно в енольной форме. [ нужна ссылка ] . Процент енола в ацетилацетоне , трифторацетилацетоне и гексафторацетилацетоне составляет 85, 97 и 100% соответственно (в чистом виде, 33 °C). [5] Циклические 1,3-дикетоны, такие как 1,3-циклогександион и димедон , также существуют в значительной степени в енольной форме.
Как и другие дикетоны, 1,3-дикетоны являются универсальными предшественниками гетероциклов. Основание-конъюгат, полученное из 1,3-кетонов, может служить лигандом для образования координационных комплексов ацетилацетоната металла . В реакции ДеМайо 1,3-дикетоны реагируют с алкенами в фотохимической перициклической реакции с образованием (замещенных) 1,5-дикетонов.
Классически 1,3-дикетоны получают конденсацией Кляйзена кетона со сложным эфиром.
1,3-Диэфиры и двухосновные кислоты
[ редактировать ]Малоновая кислота и ее эфиры являются исходными представителями этого класса дикарбонилов. Также распространены 2-замещенные производные формулы RCH(CO 2 R) 2 , которые возникают в результате C-алкилирования сопряженного основания (енолята) NaCH(CO 2 R) 2 .
β-кето-эфиры
[ редактировать ]β-кетоэфиры легко возникают в результате конденсации пары сложных эфиров. Хорошо известным примером является этилацетоацетат (хотя его получают путем этанолиза кетена ).
1,4-дикарбонилы
[ редактировать ]1,4-диальдегиды
[ редактировать ]Сукцинальдегид (CH 2 CHO) 2 — простейший и родительский 1,4-диальдегид. Ароматическое производное — фталальдегид .
1,4-Дикетоны
[ редактировать ]
Дикетоны с двумя метиленовыми группами, разделяющими карбонильные группы, также называемые γ-дикетонами, обычно сосуществуют со своими енольными таутомерами . Наиболее выдающимся представителем является ацетонилацетон . 1,4-Дикетоны являются полезными предшественниками гетероциклов посредством синтеза Паала-Кнорра , который дает пирролы :
Эта реактивность лежит в основе нейротоксичности γ -дикетонов. [6] 1,4-Дикетоны также являются предшественниками фуранов и тиофенов . Конденсация 1,4-дикетонов (и родственных субстратов) с гидразинами дает дигидропиридазины, которые можно превратить в пиридазины .
пара -хинон , C 4 H 4 (CO) 2 , является родителем большого семейства 1,4-дикетонов.
1,4-диэфиры и двухосновные кислоты
[ редактировать ]Янтарная кислота и ее эфиры являются родительскими членами этого семейства 1,4-дикарбонилов. Янтарная кислота известна как компонент цикла лимонной кислоты . Образует ангидрид циклической кислоты, янтарный ангидрид . К ненасыщенным членам относятся малеиновая и фумаровая кислоты и их сложные эфиры.
1,5-дикарбонилы
[ редактировать ]1,5-диальдегиды
[ редактировать ]Глутаральдегид (CH 2 ) 3 (CHO) 2 является простейшим и исходным 1,5-диальдегидом. Он легко увлажняет. Ароматический аналог — изофталевый альдегид . [7]
1,5-Дикетоны
[ редактировать ]Эти дикетоны имеют три метиленовые группы, разделяющие карбонильные группы.
1,5-диэфиры и двухосновные кислоты
[ редактировать ]Глутаровая кислота (CH 2 ) 3 (CO 2 H) 2 является исходной 1,5-дикислотой.
Гидратация и циклизация
[ редактировать ]
Малые альдегиды имеют тенденцию к гидратации. Для диальдегидов преобладает гидратация. Глиоксаль образует ряд циклических гидратов. Сукцинальдегид легко гидратируется с образованием 2,5-дигидрокситетрагидрофурана. Ароматический фталальдегид также образует гидратированный.

Аналогичные равновесия гидратации и циклизации применимы к малеиновому диальдегиду. [8] [9] глутаровый альдегид и адипальдегид .
Безопасность
[ редактировать ]Ряд дикарбонильных соединений биоактивны. Известно, что диацетил вызывает облитерирующий бронхиолит у лиц, подвергающихся его воздействию на производстве. [10] Диальдегиды, например глутаровый альдегид и малоновый альдегид, являются фиксаторами или стерилизаторами.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с Хардо Сигел; Манфред Эггерсдорфер (2007). «Кетоны». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. п. 16. дои : 10.1002/14356007.a15_077 . ISBN 978-3527306732 .
- ^ Эрикс, К.; Хайден, ТД; Ян, С. Си; Чан, И.Ю. (1983). «Кристаллическая и молекулярная структура биацетила (2,3-бутандиона) (H 3 CCO) 2 при -12 и -100 °С». Дж. Ам. хим. Соц . 105 (12): 3940–3942. дои : 10.1021/ja00350a032 .
- ^ Яна, Кальянашис; Гангули, Бишваджит (2018). «Исследование методом DFT для изучения важности размера кольца и влияния растворителей на процесс кето-енольной таутомеризации α- и β-циклодионов» . АСУ Омега . 3 (7): 8429–8439. дои : 10.1021/acsomega.8b01008 . ПМК 6644555 . ПМИД 31458971 .
- ^ «CHEBI:27659 — 2-оксоальдегид» . Химические соединения биологического интереса (ХЭБИ).
- ^ Джейн Л. Бердетт; Макс Т. Роджерс (1964). «Кето-енольная таутомерия в β-дикарбонилах, изученная методом спектроскопии ядерного магнитного резонанса. I. Химические сдвиги протонов и константы равновесия чистых соединений». Дж. Ам. хим. Соц . 86 : 2105–2109. дои : 10.1021/ja01065a003 .
- ^ Стивен Р. Клаф; Лейна Малхолланд (2005), «Гексан», Энциклопедия токсикологии , том. 2 (2-е изд.), Elsevier, стр. 522–525.
- ^ Акерман, Дж. Х.; Суррей, Арканзас (1967). «Изофталальдегид». Органические синтезы . 47:76 . дои : 10.15227/orgsyn.047.0076 .
- ^ Харди, премьер-министр; Николлс, AC; Райдон, Х.Н. (1972). «Гидратация и полимеризация сукцинальдегида, глутаральдегида и адипальдегида». Журнал Химического общества, Perkin Transactions 2 (15): 2270. doi : 10.1039/P29720002270 .
- ^ Д.М. Бернесс (1960). «2,5-Дигидро-2,5-Диметоксифуран». Органические синтезы . 40:29 . дои : 10.15227/orgsyn.040.0029 .
- ^ Крайсс, Кэтлин (август 2017 г.). «Признание профессионального воздействия диацетила: чему мы можем научиться из этой истории?» . Токсикология . 388 : 48–54. дои : 10.1016/j.tox.2016.06.009 . ПМЦ 5323392 . ПМИД 27326900 .



