Перегруппировка Штиглица
| Перегруппировка Штиглица | |
|---|---|
| Назван в честь | Юлиус Штиглиц |
| Тип реакции | Реакция перегруппировки |
| Примеры и связанные реакции | |
| Подобные реакции | Перегруппировка Бекмана |
Перегруппировка Штиглица — это реакция перегруппировки в органической химии , названная в честь американского химика Юлиуса Штиглица (1867–1937) и впервые исследованная им и Полом Николасом Личем в 1913 году. [1] Он описывает -перегруппировку тритиламина 1,2 производных в триарилимины . [1] [2] Это сравнимо с перегруппировкой Бекмана , которая также включает замещение атома азота посредством сдвига углерода на азот. [3] Например, триарилгидроксиламины могут подвергаться перегруппировке Штиглица путем дегидратации и сдвига фенильной группы после активации пентахлоридом фосфора соответствующего триарилимина с образованием , основания Шиффа . [4] [5]

В общем, термин «перегруппировка Штиглица» используется для описания широкого спектра реакций перегруппировки аминов в имины . [4] Хотя это обычно связано с перегруппировкой триарилгидроксиламинов , о которой хорошо сообщается в научной литературе, перегруппировки Штиглица могут также происходить на алкилированных аминов . производных [6] галогенамины [7] [8] и азиды [9] [10] а также другие активированные амина . производные [4]
Общий механизм и связь с перегруппировкой Бекмана
[ редактировать ]
Механизм реакции перегруппировки Штиглица, а также используемые продукты и исходные материалы делают ее тесно связанной с перегруппировкой Бекмана , которую можно использовать для синтеза карбоксамидов . [11] Обе реакции перегруппировки включают сдвиг углерода в азот, обычно после электрофильной активации уходящей группы атома азота. [4] [12] [13] Однако основным отличием исходных материалов является степень их насыщенности. В то время как перегруппировка Штиглица происходит на производных насыщенных аминов с σ-одинарной связью, типичным исходным материалом для перегруппировки Бекмана является оксим ( гидроксилимин) с двойной связью C=N. [4] [14] При перегруппировке Бекмана катализируемая кислотой миграция углерода в азот происходит на оксиме с образованием промежуточного иона нитрилия . [15] В принципе, первый шаг перегруппировки Стиглица протекает аналогично. [4] Однако после образования положительно заряженного иона иминия в результате π-взаимодействия между неподеленной парой азота и электронодефицитным углеродом в перегруппировке Штиглица пути расходятся. При перегруппировке Штиглица зарядно-нейтральное состояние молекулы может быть достигнуто за счет диссоциации протона. Альтернативно, если исходный материал не содержал аминопротонов, нейтральное состояние может быть достигнуто с помощью внешнего восстановителя, такого как боргидрид натрия . Он восстанавливает промежуточный иминий-ион до соответствующего насыщенного амина . [4] [16] В перегруппировке Бекмана такой протон также отсутствует, и стабилизация интермедиата происходит за счет нуклеофильного присоединения молекулы воды, диссоциации протона и таутомерии от имидовой кислоты к карбоксамиду . [17]

Вариации
[ редактировать ]Хотя первоначальная реакция Штиглица наиболее известна благодаря перегруппировке тритилгидроксиламинов, существует несколько вариантов, которые включают хорошие уходящие группы в качестве N -заместителей (таких как галогены и сульфонаты). Обычно применяются разные реагенты, в зависимости от точной природы субстрата. [4]
Перегруппировка Штиглица N -гидроксилированных аминов, N -алкоксилированных аминов и N -сульфированных аминов
[ редактировать ]Перегруппировка Штиглица N- гидроксилированных аминов
[ редактировать ]Для перегруппировки тритилгидроксиламинов кислоты Льюиса, такие как пентахлорид фосфора (PCl 5 ) , пятиокись фосфора (P 2 O 5 ) или трифторид бора (BF 3 ) . можно использовать [4] Они действуют как электрофильные активаторы гидроксильной группы, повышая качество уходящей группы. Например, при использовании PCl 5 в качестве реагента тритилгидроксиламин сначала превращается в активированное промежуточное соединение посредством нуклеофильного замещения. [18] Образовавшийся промежуточный продукт может затем подвергнуться перегруппировке за счет миграции фенильной группы и диссоциации частиц фосфора (V) с образованием N -фенилбензофенонимина. [18]

Перегруппировка Штиглица N -алкоксилированных аминов
[ редактировать ]Помимо N -гидрокситритиламинов возможны также перегруппировки в N -алкокситритиламины. Однако эти реакции известны своими низкими выходами. [19] Например, N -бензилоксизамещенный тритиламин может подвергаться перегруппировке Штиглица в присутствии пентахлорида фосфора (160 °C, выход 40%) или с BF 3 в качестве реагента (60 °C, выход 29%). [20] В последнем случае BF 3 действует как кислота Льюиса при электрофильной активации бензильного кислорода, обеспечивая нуклеофильную атаку соседнего атома азота. [20]

Перегруппировка Штиглица N -сульфированных аминов
[ редактировать ]Перегруппировки Штиглица также легко протекают с активными сульфонатами в качестве уходящей группы. [21] N -сульфированные амины можно получить из соответствующих гидроксиламинов и подходящих реагентов сульфирования. Например, Хердерин и др. синтезировали свой вторичный гидроксиламин (исходный материал в перегруппировке, показанной ниже), подвергая соответствующий гидроксиламин воздействию тозилхлорида и гидроксида натрия в ацетонитриле . [22]
Перегруппировка Штиглица особенно реакционноспособна в случае мостиковых бициклических N -сульфированных аминов в качестве исходных материалов, где мягкие условия достаточны для протекания эффективной реакции. [23] Например, перегруппировка бициклического N -тозилированного амина легко протекает в водном диоксане при комнатной температуре. [24] Однако соответствующий имин в этом случае не образуется, предположительно из-за напряжения, которое термодинамически невыгодно такой структуре, несущей двойную связь у атома-мостика ( правило Бредта ). [25] Вместо этого тозилат нуклеофильно добавляется в геминальное положение азота посредством атаки на ион иминия. [22]
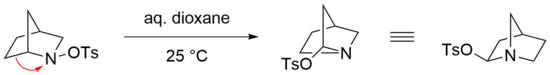
Перегруппировка Штиглица азидов
[ редактировать ]Перегруппировки Штиглица могут протекать и на органических азидах, в которых молекулярный азот является хорошей уходящей группой. [4] Эти реакции протекают аналогично стадиям реакции Шмидта , с помощью которой карбоновые кислоты могут превращаться в амины путем добавления азотистоводородной кислоты в кислых водных условиях. [26] Перегруппировка Штиглица в азидах обычно происходит за счет протонного взаимодействия. [16] или термический [4] активация, которую также можно комбинировать. [10] В обоих случаях молекулярный азот высвобождается в виде газа на необратимой стадии. Было высказано предположение, что перегруппировка после диссоциации молекулы N 2 происходит через реакционноспособный нитреновый интермедиат. [10] Эти промежуточные соединения были бы очень похожи на те, которые были предложены в качестве ключевых промежуточных продуктов в реакциях перегруппировки, названных в честь Гофмана и Курциуса . [27] но с тех пор считались маловероятными. [28] При воздействии на азид кислотой Бренстеда протонирование азида активирует базальный азот и снижает прочность связи с соседним, так что диссоциация и изгнание молекулярного азота облегчаются. [16] После перегруппировки протон может диссоциировать от иона иминия с образованием имина.
Альтернативным способом получения протонированных органических азидов является нуклофильное присоединение азотистоводородной кислоты к карбокатионам, которые затем также могут подвергаться перегруппировке Штиглица. [16]
Перегруппировка Штиглица N -галогенированных аминов
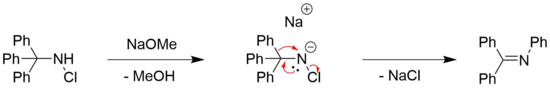
[ редактировать ]Перегруппировку Штиглица N -галогенированных аминов можно наблюдать для хлора. [7] и бром [8] замещенные амины, часто в сочетании с органическим основанием, например метоксидом натрия . [4] Потребность в основании обычно связана с необходимостью депротонирования амина. [4]
Однако также сообщалось о примерах безосновных перегруппировок Штиглица N- галогенированных аминов. Примером этого может служить полный синтез (±)-ликоподина, проведенный Полом Грико и др. [6] [29] Там образование кольца происходит путем перегруппировки вторичного галоамина при воздействии на него тетрафторбората серебра. [6] Известно, что AgBF 4 действует как источник Ag. + ионы, которые могут способствовать диссоциации галогенидов из органических молекул с образованием соответствующего галогенида серебра в качестве движущей силы. [30] Желаемый продукт затем получают восстановлением цианоборгидридом натрия , мягким восстановителем, который обычно используется при восстановлении иминов до аминов. [31]

Перегруппировка Штиглица аминов, активированных тетраацетатом свинца
[ редактировать ]Было также обнаружено, что добавление тетраацетата свинца может облегчить перегруппировку Штиглица производных амина. [32] После образования интермедиата активированного производного амина путем координации со свинцовым центром последующая перегруппировка вновь протекает через миграцию ароматической группы с образованием связи C–N, диссоциацию свинца и депротонирование образовавшегося иминиевого иона. [33]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б Юлиус Штиглиц , Пол Николас Лич (1914). «Молекулярная перегруппировка триарилметилгидроксиламинов и перегруппировка Бекмана кетоксимов» . Журнал Американского химического общества . 36 (2): 272–301. дои : 10.1021/ja02179a008 .
- ^ Берт Аллен Стагнер (1914). «Молекулярная перегруппировка триарилметилгидроксиламинов» . Журнал Американского химического общества . 36 (2): 2069–2081. дои : 10.1021/ja02267a018 .
- ^ Ван, Зеронг (2010). Комплексные органические реакции и реагенты . John Wiley & Sons, Inc., стр. 288–295. ISBN 9780471704508 .
- ^ Jump up to: а б с д и ж г час я дж к л м Ван, Зеронг (сентябрь 2010 г.). Комплексные органические реакции и реагенты . Джон Уайли. стр. 2673–2676. ISBN 9780471704508 .
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « База Шиффа ». дои : 10.1351/goldbook.S05498
- ^ Jump up to: а б с Греко, Пол А.; Дай, Юцзя (май 1998 г.). «Конструирование карбоциклического кольца посредством внутримолекулярной реакции Дильса-Альдера с генерируемым in-situ аллильным катионом, стабилизированным гетероатомом: полный синтез (±)-ликоподина». Журнал Американского химического общества . 120 (20): 5128–5129. дои : 10.1021/ja980117b .
- ^ Jump up to: а б Восбург, Изабелла (октябрь 1916 г.). «Молекулярная перегруппировка трифенил-метилгалогенаминов» . Журнал Американского химического общества . 38 (10): 2081–2095. дои : 10.1021/ja02267a019 .
- ^ Jump up to: а б ДеТар, ДеЛос Ф.; Бродерик, Эдвард; Фостер, Джордж; Хилтон, Бенджамин Д. (май 1950 г.). «Попытка перегруппировки 9-бромметиленфлуорена в 9-бромфенантрен». Журнал Американского химического общества . 72 (5): 2183–2184. дои : 10.1021/ja01161a086 .
- ^ Морган, Агнес Фэй (октябрь 1916 г.). «Молекулярные перегруппировки некоторых триарилметилхлораминов». Журнал Американского химического общества . 38 (10): 2095–2101. дои : 10.1021/ja02267a020 .
- ^ Jump up to: а б с Кун, Джеймс (декабрь 1916 г.). «Молекулярная перегруппировка триарилметилазидов». Журнал Американского химического общества . 38 (12): 2718–2726. дои : 10.1021/ja02269a014 .
- ^ Блатт, AH (апрель 1933 г.). «Перегруппировка Бекмана». Химические обзоры . 12 (2): 215–260. дои : 10.1021/cr60042a002 .
- ^ Табер, Дуглас Ф.; Стрейни, Патрик Дж. (декабрь 2010 г.). «Синтез лауролактама из циклододеканона посредством перегруппировки Бекмана». Журнал химического образования . 87 (12): 1392. Бибкод : 2010ЖЧЭд..87.1392Т . дои : 10.1021/ed100599q .
- ^ Фуруя, Ёсиро; Исихара, Кадзуаки; Ямамото, Хисаси (август 2005 г.). «Цианурхлорид как мягкий и активный катализатор перегруппировки Бекмана». Журнал Американского химического общества . 127 (32): 11240–11241. дои : 10.1021/ja053441x . ПМИД 16089442 .
- ^ Гай Донарума, Л.; Хелдт, Уолтер З. (2011). «Органические реакции: перегруппировка Бекмана»: 1–59. дои : 10.1002/0471264180.или011.01 .
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ ван Дейк, Том; Крис Слотвег, судья; Ламмертсма, Куп (2017). «Ионы нитрила – синтез и применение» . Органическая и биомолекулярная химия . 15 (48): 10134–10144. дои : 10.1039/C7OB02533E . hdl : 11245.1/6b602f30-dfe7-4ef5-a945-9f6942fab8b4 . ПМИД 29188244 .
- ^ Jump up to: а б с д Пирсон, Уильям Х. (сентябрь 1996 г.). «Алифатические азиды как основания Льюиса. Применение к синтезу гетероциклических соединений». Журнал гетероциклической химии . 33 (5): 1489–1496. дои : 10.1002/jhet.5570330506 . hdl : 2027.42/96395 .
- ^ Клейден, Джонатан; Гривз, Ник; Уоррен, Стюарт (2012). Органическая химия (2-е изд.). Издательство Оксфордского университета. п. 958. ИСБН 978-0-19-927029-3 .
- ^ Jump up to: а б Ли, Цзе Джек (2003). Назовите реакции: сборник подробных механизмов реакций (2-е изд.). Спрингер. п. 361. ИСБН 978-3-662-05338-6 .
- ^ Мецгер, Карл Хорст; Мюллер, Питер; Мюллер-Долезаль, Хайди; Швалль, Хорст; Зёлль, Ханна (2014). Методы органической химии Губена-Вейля Том . Издательство Георга Тиме. п. 1266. ИСБН 9783131805546 .
- ^ Jump up to: а б Эйрс, Эрл Б.; Хаузер, Чарльз Р. (январь 1948 г.). «Перегруппировка N -трифенилметил-О-бензилгидроксиламина с помощью амида калия и трифторида бора». Журнал органической химии . 13 (1): 116–119. дои : 10.1021/jo01159a015 . ПМИД 18917716 .
- ^ Пирсон, Уильям Х.; Шкерьянц, Джеффри М. (сентябрь 1992 г.). «Внутримолекулярная реакция Шмидта алкилазида с карбокатионом. Генерация и перегруппировка конформационно ограниченного вторичного иона аминодиазония». Буквы тетраэдра . 33 (37): 5291–5294. дои : 10.1016/s0040-4039(00)79075-7 . hdl : 2027.42/29850 .
- ^ Jump up to: а б Хесинг, А.; Гердеринг, В. (январь 1981 г.). «Введение кислорода при перегруппировке производных 2-аза-бицикло[2.2.1]гепт-2-ена». Буквы тетраэдра . 22 (47): 4675–4678. дои : 10.1016/s0040-4039(01)83010-0 .
- ^ Ренсло, Адам Р.; Данхайзер, Рик Л. (октябрь 1998 г.). «Синтез замещенных пиридинов путем региоконтролируемого [4 + 2] циклоприсоединения оксиминосульфонатов». Журнал органической химии . 63 (22): 7840–7850. дои : 10.1021/jo981014e .
- ^ Гассман, Пол Г.; Хартман, Джордж Д. (январь 1973 г.). «Химия ионов нитрена. XXVII. Эффективность уходящей группы при генерации ионов нитрена из производных гидроксиламина». Журнал Американского химического общества . 95 (2): 449–454. дои : 10.1021/ja00783a023 .
- ^ Фосетт, Фрэнк С. (октябрь 1950 г.). «Правило Бредта о двойных связях в структурах с атомными мостиками». Химические обзоры . 47 (2): 219–274. дои : 10.1021/cr60147a003 . ПМИД 24538877 .
- ^ Вольф, Ганс (2011). Органические реакции . John Wiley and Sons, Inc., стр. 307–336. дои : 10.1002/0471264180.или003.08 .
- ^ Гош, Арун К.; Саркар, Аниндья; Бриндизи, Маргарита (2018). «Перегруппировка Курциуса: понимание механизма и недавние применения в синтезе натуральных продуктов» . Органическая и биомолекулярная химия . 16 (12): 2006–2027. дои : 10.1039/c8ob00138c . ПМЦ 5864567 . ПМИД 29479624 .
- ^ Раук, Арви; Алвуд, Пол Ф. (1 мая 1977 г.). «Теоретическое исследование перегруппировки Курциуса. Электронные структуры и взаимные превращения разновидностей CHNO». Канадский химический журнал . 55 (9): 1498–1510. дои : 10.1139/v77-209 .
- ^ Хагер, Анастасия; Врилинк, Нина; Хагер, Доминик; Лефранк, Жюльен; Траунер, Дирк (2016). «Синтетические подходы к алкалоидам, содержащим α-третичные амины» . Отчеты о натуральных продуктах . 33 (3): 491–522. дои : 10.1039/c5np00096c . ПМИД 26621771 .
- ^ Ахилону, Мэтью Чилака; Умесиоби, Деннис О. (ноябрь 2016 г.). «Образование связей углерод-углерод и углерод-гетероатом с использованием тетрафторбората серебра в качестве промотора» . Арабский химический журнал . 9 : 1984–2003. дои : 10.1016/j.arabjc.2015.06.038 .
- ^ Христиане, Ганс; Мейер, Герд (1997). Основы общей и неорганической химии (1-е изд.). Салле + Зауэрландер. п. 824. ИСБН 978-3-7935-5493-6 .
- ^ Систи, Энтони Джозеф (1968). «Реакция тетраацетата свинца с фенилметиламинами». Химические коммуникации (21): 1272. doi : 10.1039/C19680001272 .
- ^ Систи, Энтони Дж.; Мильштейн, Стэнли Р. (декабрь 1974 г.). «Перегруппировка Штиглица с тетраацетатом свинца и триарилметиламинами». Журнал органической химии . 39 (26): 3932–3936. дои : 10.1021/jo00940a030 .