Перегруппировка Гофмана
| Перегруппировка Гофмана | |
|---|---|
| Назван в честь | Август Вильгельм фон Хофманн |
| Тип реакции | Реакция перегруппировки |
| Идентификаторы | |
| RSC Идентификатор онтологии | RXNO: 0000410 |
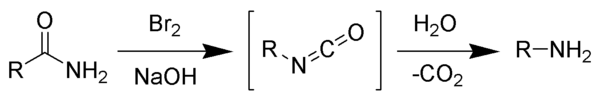
Перегруппировка Гофмана ( деградация Гофмана ) — это органическая реакция первичного амида с образованием первичного амина с одним атомом углерода меньше . [1] [2] [3] Реакция включает окисление азота с последующей перегруппировкой карбонила и азота с образованием промежуточного изоцианата . В результате реакции может образовываться широкий спектр продуктов, включая алкилы и ариламины .
Реакция названа в честь ее первооткрывателя, Августа Вильгельма фон Гофмана , и ее не следует путать с элиминированием Хофмана , еще одним названием реакции, с которым он является одноименным .
Механизм
[ редактировать ]Реакция брома с гидроксидом натрия образует гипобромит натрия in situ , который превращает первичный амид в промежуточный изоцианат. Образование промежуточного нитрена невозможно, поскольку оно предполагает также образование гидроксамовой кислоты в качестве побочного продукта, чего никогда не наблюдалось. Промежуточный изоцианат гидролизуется до первичного амина с выделением углекислого газа . [2]
- Основание отрывает кислый протон NH, образуя анион.
- Анион реагирует с бромом в реакции α-замещения с образованием N -бромамида.
- Отщепление оставшегося амидного протона дает анион бромамида.
- Бромамид-анион перегруппировывается, когда группа R, присоединенная к карбонильному углероду, мигрирует к азоту, в то время как бромид-ион уходит, образуя изоцианат.
- Изоцианат добавляет воду на стадии нуклеофильного присоединения с образованием карбаминовой кислоты (также известной как уретан ).
- Карбаминовая кислота самопроизвольно теряет CO 2 , образуя аминный продукт.
Вариации
[ редактировать ]Бром можно заменить несколькими реагентами. Гипохлорит натрия , [4] тетраацетат свинца , [5] N -бромсукцинимид и (бис(трифторацетокси)иод)бензол [6] может повлиять на перегруппировку Гофмана.
Промежуточный изоцианат может быть захвачен различными нуклеофилами с образованием стабильных карбаматов или других продуктов вместо того, чтобы подвергаться декарбоксилированию. В следующем примере промежуточный изоцианат улавливается метанолом . [7]
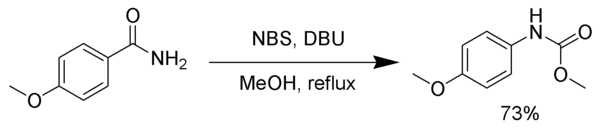
Подобным же образом промежуточный изоцианат может быть захвачен трет -бутиловым спиртом , образуя трет -бутоксикарбонил (Boc)-защищенный амин.
Перегруппировку Гофмана также можно использовать для получения карбаматов из α,β - ненасыщенных или α- гидроксиамидов . [2] [8] или нитрилы из α,β ацетиленамидов - [2] [9] с хорошей урожайностью (≈70%).
Приложения
[ редактировать ]- При получении антраниловой кислоты из фталимида [10]
- Никотинамид превращается в 3-аминопиридин. [11]
- Симметричная структура [ нужны разъяснения ] α -фенилпропанамида не изменяется после реакции Гофмана.
- В синтезе габапентина , начиная с моноамидирования ангидрида 1,1-циклогександиуксусной кислоты аммиаком до моноамида 1,1-циклогександиуксусной кислоты с последующей перегруппировкой Гофмана. [12]
См. также
[ редактировать ]- Перегруппировка Бекмана
- Более короткая перестановка
- Йодоформная реакция
- Свободная перестановка
- реакция Шмидта
- Деградация метеоролога
Ссылки
[ редактировать ]- ^ Хофманн, AW (1881). «О действии брома в щелочных растворах на амиды» . Отчеты Немецкого химического общества . 14 (2): 2725–2736. дои : 10.1002/cber.188101402242 .
- ^ Jump up to: а б с д Эверетт, Уоллис; Лейн, Джон (1946). Реакция Гофмана . Том. 3. С. 267–306. дои : 10.1002/0471264180.или003.07 . ISBN 9780471005285 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Сиойри, Такаюки (1991). «Реакции деградации». Комплексный органический синтез . Том. 6. С. 795–828. дои : 10.1016/B978-0-08-052349-1.00172-4 . ISBN 9780080359298 .
- ^ Мохан, Рам С.; Монк, Кейт А. (1999). «Перегруппировка Гофмана с использованием бытового отбеливателя: синтез 3-нитроанилина» . Журнал химического образования . 76 (12): 1717. Бибкод : 1999ЖЧЭд..76.1717М . дои : 10.1021/ed076p1717 .
- ^ Баумгартен, Генри; Смит, Ховард; Стаклис, Андрис (1975). «Реакции аминов. XVIII. Окислительная перегруппировка амидов с тетраацетатом свинца». Журнал органической химии . 40 (24): 3554–3561. дои : 10.1021/jo00912a019 .
- ^ Алмонд, Меррик Р.; Стиммель, Джули Б.; Томпсон, Алан; Лаудон, Марк (1988). «Перегруппировка Гофмана в слабокислых условиях с использованием [I,I-бис(трифторацетокси)]йодбензола: гидрохлорид циклобутиламина из циклобутанкарбоксамида». Органические синтезы . 66 : 132. дои : 10.15227/orgsyn.066.0132 .
- ^ Кейллор, Джеффри В.; Хуан, Сицай (2002). «Образование метилкарбамата посредством модифицированных реакций перегруппировки Гофмана: метил N - ( п -метоксифенил) карбамат». Органические синтезы . 78 : 234. дои : 10.15227/orgsyn.078.0234 .
- ^ Верман, Р.А. (1913). «Действие гипохлорита натрия на амиды ненасыщенных кислот» . «Анналы химии» Юстуса Либиха . 401 (1): 1–20. дои : 10.1002/jlac.19134010102 .
- ^ Ринкес, IJ (1920). «О действии гипохлорита натрия на амиды кислот». Коллекция химических предприятий Нидерландов . 39 (12): 704–710. дои : 10.1002/recl.19200391204 .
- ^ Маки, Такао; Такеда, Кадзуо (2000). «Бензойная кислота и производные». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a03_555 . ISBN 3527306730 . .
- ^ Аллен, CFH; Вольф, Кэлвин Н. (1950). «3-Аминопиридин» . Органические синтезы . 30 :3. дои : 10.15227/orgsyn.030.0003 ; Сборник томов , т. 4, с. 45 .
- ^ США 20080103334 , «Способ синтеза габапентина».
Библиография
[ редактировать ]- Клейден, Джонатан (2007). Органическая химия . Oxford University Press Inc., стр. 1073 . ISBN 978-0-19-850346-0 .
- Физер, Луи Ф. (1962). Продвинутая органическая химия . Reinhold Publishing Corporation, Chapman & Hall, Ltd., стр. 499–501.
