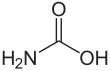
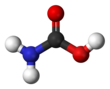
Карбаминовая кислота
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Карбаминовая кислота [ 1 ] | |||
| Другие имена
Аминометановая кислота
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Лекарственный Банк | |||
| КЕГГ | |||
| МеШ | Карбамин+кислота | ||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| NH 3 CO 2 | |||
| Молярная масса | 61.040 g·mol −1 | ||
| Родственные соединения | |||
Родственные соединения
|
формамид Дитиокарбамат Угольная кислота Мочевина Этилкарбамат Сульфаминовая кислота | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Карбаминовая кислота , которую также можно назвать аминомуравьиной кислотой или аминокарбоновой кислотой . [ 2 ] это химическое соединение формулы Н 2 NCOOH . Его можно получить реакцией аммиака. NH 3 и диоксид углерода CO 2 при очень низких температурах, что также дает карбамат аммония. [НХ 4 ] + [NH 2 CO 2 ] − . Соединение стабильно только примерно до 250 К (-23 ° C); при более высоких температурах он разлагается на эти два газа. [ 3 ] Твердое вещество, по-видимому, состоит из димеров , две молекулы которых соединены водородными связями между двумя карбоксильными группами –СООН. [ 4 ]
Карбаминовую кислоту можно рассматривать как амин и карбоновую кислоту , и, следовательно, как аминокислоту ; [ 3 ] однако присоединение карбоксильной группы –COOH непосредственно к атому азота (без какой-либо промежуточной углеродной цепи) заставляет ее вести себя совсем иначе, чем аминокислоты с промежуточной углеродной цепью. ( Глицин NH 2 CH 2 COOH обычно считается простейшей аминокислотой.) Гидроксильная группа –OH, присоединенная к углероду, также исключает его из класса амидов .
Термин «карбаминовая кислота» также используется в общем для любых соединений формы RR'NCOOH, где R и R' представляют собой органические группы или водород. [ 5 ]
Депротонирование карбаминовой кислоты дает карбамат- анион. РР'НКОО − , соли которого могут быть относительно стабильными. Карбамат — это также термин, используемый для сложных эфиров карбаминовых кислот, таких как метилкарбамат. H 2 N-C(=O)-OCH 3 . Карбамоильная RR'N–C(=O)– ( часто функциональная группа обозначаемая Cbm ) представляет собой молекулу карбаминовой кислоты за вычетом OH-части карбоксила.
Структура
[ редактировать ]Карбаминовая кислота представляет собой плоскую молекулу. [ 3 ]
The Группа H 2 N- карбаминовой кислоты, в отличие от группы большинства аминов, не может быть протонирована до аммониевой группы. H3H3N + − . Цвиттер -ионная форма H3H3N + −COO − очень нестабилен и быстро разлагается на аммиак и углекислый газ, [ 6 ] однако есть сообщения о его обнаружении во льдах, облученных протонами высокой энергии . [ 3 ]
Производные
[ редактировать ]Карбаминовая кислота формально является исходным соединением нескольких важных семейств органических соединений:
-
карбаминовые кислоты
-
карбамат-анионы
-
карбаматные эфиры
Карбаминовые кислоты
[ редактировать ]Многие замещенные карбаминовые кислоты (RHNCOOH или RR'NCOOH) можно легко синтезировать путем барботирования диоксида углерода через растворы соответствующего амина ( RNH 2 или RR'NH соответственно) в подходящем растворителе, таком как ДМСО или сверхкритический диоксид углерода. [ 5 ] Эти карбаминовые кислоты обычно нестабильны при комнатной температуре, превращаясь в исходный амин и диоксид углерода. [ 7 ]
Карбаматные эфиры
[ редактировать ]В отличие от карбаминовых кислот, сложные эфиры карбаматов обычно стабильны при комнатной температуре в более высоком состоянии. Их получают реакцией карбамоилхлоридов со спиртами, присоединением спиртов к изоцианатам и реакцией карбонатных эфиров с аммиаком. [ 8 ] Метилкарбамат и этилкарбамат являются одними из простейших примеров и исторически использовались в текстильной промышленности; оба в настоящее время считаются канцерогенами. бензилкарбамат Известен также .
Встречаемость в природе
[ редактировать ]Фермент . класса карбаматкиназы , участвующий в нескольких метаболических путях живых организмов, катализирует образование карбамоилфосфата H 2 N-C(=O)-O-PO 2- 3 :
Важным примером фермента с такой активностью является карбамоилфосфатсинтетаза , например карбамоилфосфатсинтетаза I, выполняющая первую стадию цикла мочевины для утилизации отработанного аммиака.
Одна молекула гемоглобина четыре молекулы углекислого газа может переносить в легкие в виде карбаматных групп, образующихся в результате реакции CO 2 с четырьмя концевыми аминогруппами в дезокси-форме . Полученное соединение называется карбаминогемоглобином .
Использование
[ редактировать ]Промышленный
[ редактировать ]Карбаминовая кислота является промежуточным продуктом промышленного производства мочевины , в котором участвует реакция углекислого газа и аммиака. [ 9 ]
- CO 2 + NH 3 → H 2 NCOOH
- H 2 NCOOH + NH 3 → CO(NH 2 ) 2 + H 2 O
Медицинский
[ редактировать ]Некоторые сложные эфиры карбаматов используются в качестве миорелаксантов , в том числе Эмилкамат , Фенпробамат , Стирамат и другие представители кода АТС M03BA . Они связываются с барбитуратным участком ГАМК А. рецептора [ 10 ]
Инсектициды
[ редактировать ]несколько инсектицидов Было разработано на основе карбаминовой кислоты; например алдикарб , карбарил , карбофуран . [ 11 ]
Химический синтез
[ редактировать ]Аминная функциональная группа −NH 2 может быть защищен от нежелательных реакций, образуясь в виде остатка сложного эфира карбаматной кислоты –NHC(=O)–OR. Затем при гидролизе сложноэфирной связи образуется карбаминовая кислота –NHC(=O)OH, которая затем теряет диоксид углерода с образованием желаемого амина.
Ссылки
[ редактировать ]- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 . Королевское химическое общество . п. 778. дои : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ^ «Сводка соединений PubChem для CID 277, карбаминовая кислота» . Национальный центр биотехнологической информации. 2020 . Проверено 10 октября 2020 г.
- ^ Перейти обратно: а б с д Р.К. Ханна и М.Х. Мур (1999): «Карбаминовая кислота: молекулярная структура и ИК-спектры». Spectrochimica Acta Часть A: Молекулярная и биомолекулярная спектроскопия , том 55, выпуск 5, страницы 961-967. два : 10.1016/S1386-1425(98)00228-5 PMID 10347902 Бибкод : 1999AcSpA..55..961K
- ^ Ж. Б. Босса, П. Теуле, Ф. Дюверне, Ф. Борже и Т. Кьявасса (2008): «Образование карбаминовой кислоты и карбамата во льдах NH 3 :CO 2 – УФ-облучение в сравнении с термическими процессами». Астрономия и астрофизика , том 492, выпуск 3, страницы 719-724. дои : 10.1051/0004-6361:200810536
- ^ Перейти обратно: а б З. Дж. Дейкстра, А. Р. Доорнбос, Х. Вейтен, Дж. М. Эрнстинг, К. Дж. Эльзевир и Дж. Т. Ф. Кеурентьес (2007): «Образование карбаминовой кислоты в органических растворителях и в сверхкритическом диоксиде углерода». Журнал сверхкритических жидкостей , том 41, выпуск 1, страницы 109-114. два : 10.1016/j.supflu.2006.08.012
- ^ Ю.-Дж. Чен, М. Нуэво, Ж.-М. Се, Т.-С. Йи, В.-Х. Сан, В.-Х. ИП, Х.-С. Фунг, С.-Ю. Чан, Ю.-Ю. Ли, Ж.-М. Чен и К.-Ю.Р. Ву (2007): «Карбаминовая кислота, полученная путем УФ/ЭУФ-облучения аналогов межзвездного льда». Астрономия и астрофизика , том 464, выпуск 1, страницы 253-257. дои : 10.1051/0004-6361:20066631
- ^ Лемке, Томас Л. (2003). Обзор органических функциональных групп: введение в медицинскую органическую химию . Филадельфия, Пенсильвания: Липпинкотт, Уильямс и Уилкинс. п. 63. ИСБН 978-0-7817-4381-5 .
- ^ Ягер, Питер; Рентзеа, Костин Н.; Кечка, Хайнц (2000). «Карбаматы и карбамоилхлориды». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a05_051 . ISBN 3527306730 .
- ^ Мессен, Дж. Х.; Петерсен, Х. «Мочевина». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a27_333 . ISBN 978-3527306732 .
- ^ Блок, Джон Х.; Бил, Джон М., ред. (2004). «Депрессант центральной нервной системы» . Учебник органической медицинской и фармацевтической химии Уилсона и Гисволда . Филадельфия, Пенсильвания: Липпинкотт, Уильямс и Уилкинс. п. 495. ИСБН 978-0-7817-3481-3 .
- ^ Ришер, Джон Ф.; Минк, Франклин Л.; Стара, Джерри Ф. (1987). «Токсикологическое действие карбаматного инсектицида алдикарба на млекопитающих: обзор» . Перспективы гигиены окружающей среды . 72 : 267–281. дои : 10.2307/3430304 . JSTOR 3430304 . ПМЦ 1474664 . ПМИД 3304999 .