Перестановка копа
| Перестановка копа | |
|---|---|
| Назван в честь | Артур С. Коуп |
| Тип реакции | Реакция перегруппировки |
| Идентификаторы | |
| Портал органической химии | перестройка поведения |
| RSC Идентификатор онтологии | RXNO: 0000028 |
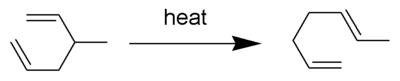
Перегруппировка Коупа — широко изученная органическая реакция, включающая [3,3]-сигматропную перегруппировку 1,5- диенов . [1] [2] [3] [4] Его разработали Артур К. Коуп и Элизабет Харди . Например, 3-метилгекса-1,5-диен, нагретый до 300 °C, дает гепта-1,5-диен.
Перегруппировка Коупа вызывает флюкционные состояния молекул семейства буллваленов .
Механизм
[ редактировать ]Перегруппировка Коупа является типичным примером согласованной сигматропной перегруппировки. Она классифицируется как [3,3]-сигматропная перегруппировка с символом Вудворда-Хоффмана [ π 2 s + σ 2 s + π 2 s ] и поэтому термически разрешена. Иногда полезно думать о нем как о переходном состоянии, энергетически и структурно эквивалентном дирадикалу , хотя дирадикал обычно не является настоящим промежуточным продуктом (минимум потенциальной энергии). [5] Проиллюстрированное здесь переходное состояние стула является предпочтительным в системах с открытой цепью (как показали эксперименты Деринга-Рота). Однако конформационно ограниченные системы, такие как цис -1,2-дивинилциклопропаны, могут подвергаться перегруппировке в конформации лодочки.
В настоящее время общепринято, что большинство перегруппировок Коупа происходят по разрешенному согласованному пути через ароматическое переходное состояние Хюккеля и что дирадикальный промежуточный продукт не образуется. Однако согласованная реакция часто может быть асинхронной, а электронно-возмущенные системы могут иметь в переходном состоянии значительный дирадикальный характер. [6] Типичная иллюстрация переходного состояния перегруппировки Коупа электронно нейтрального гекса-1,5-диена представлена ниже. Здесь видно, что две π-связи разрываются и образуются две новые π-связи, и одновременно разрывается σ-связь и образуется новая σ-связь. В отличие от перегруппировки Кляйзена , перегруппировки Коупа без снятия напряжения или электронного возмущения часто близки к термически нейтральным и поэтому могут достигать лишь частичной конверсии из-за недостаточно благоприятной константы равновесия . В случае гекса-1,5-диена перегруппировка вырожденная (продукт идентичен исходному), поэтому K = 1 по необходимости.
В асимметричных диенах часто необходимо учитывать стереохимию, которую в случае перициклических реакций, таких как перегруппировка Коупа, можно предсказать с помощью правил Вудворда-Гоффмана и рассмотрения предпочтения геометрии переходного состояния кресла.
Примеры
[ редактировать ]Перегруппировка широко используется в органическом синтезе. допускается Симметрия , когда она надлицевая по всем компонентам. Переходное состояние молекулы проходит через лодку или стул, как переходное состояние. Примером перегруппировки Коупа является расширение циклобутанового кольца до циклоокта-1,5-диенового кольца:

В этом случае реакция должна пройти через «лодочка», переходное состояние чтобы образовать две двойные цис -связи . Двойная транс-связь в кольце будет слишком натянутой . Реакция протекает в термических условиях. Движущей силой реакции является потеря напряжения циклобутанового кольца.
Об органокаталитической перегруппировке Копа впервые сообщалось в 2016 году. В этом процессе используется альдегидзамещенный 1,5-диен, что позволяет достичь «иминиевого катализа» с использованием гидразидного катализатора и умеренных уровней энантиоселективности (до 47% э.и.). быть достигнутым. [7]
Ряд ферментов катализирует перегруппировку Копа, хотя в природе она встречается редко. [8] [9]
Перегруппировка Окси-Копа и родственные варианты
[ редактировать ]При перегруппировке окси-Копа гидроксильная группа добавляется к C3 , образуя еналь или енон после кето-енольной таутомерии промежуточного енола. [10] [11] [12]

В своей первоначальной реализации реакция окси-Коупа требовала высоких температур. Последующие работы показали, что соответствующие алкоксиды калия перегруппировываются быстрее на 10 10 до 10 17 . [13] Благодаря этому нововведению реакция хорошо протекает при комнатной температуре или даже при 0 °C. Обычно гидрид калия и 18-краун-6 используются для получения диссоциированного алкоголята калия: [14]

Показанный выше диастереомер . исходного вещества с экваториальной винильной группой не вступает в реакцию, что свидетельствует о согласованном характере этой реакции Тем не менее считается, что переходное состояние реакции имеет высокую степень дирадикального характера. Следовательно, анион-ускоренная реакция окси-копа может протекать с высокой эффективностью даже в системах, которые не допускают эффективного перекрытия орбиталей , что иллюстрируется ключевым этапом синтеза перипланона B : [15]
![Пример от [Стюарта Шрайбера]](http://upload.wikimedia.org/wikipedia/commons/thumb/5/5a/Schreiber.png/600px-Schreiber.png)
Соответствующие нейтральные перегруппировки окси-копа и силокси-копа оказались неудачными, давая только продукты элиминирования при 200 ° C.
Другой разновидностью перегруппировки Коупа является аза-перегруппировка Коупа .
См. также
[ редактировать ]- Перегруппировка Кляйзена — еще одна широко изученная [3,3] сигматропная перегруппировка.
- перегруппировка дивинилциклопропан-циклогептадиена
Ссылки
[ редактировать ]- ^ Артур К. Коуп ; Элизабет М. Харди ; Дж. Ам. хим. Соц. 1940 , 62 , 441.
- ^ Роудс, С.Дж.; Раулинс, Северная Каролина; Орг. Реагировать. 1975 , 22 , 1–252. (Обзор)
- ^ Хилл, РК; Компр. Орг. Синтез. 1991 , 5 , 785–826.
- ^ Уилсон, SR; Орг. Реагировать. 1993 , 43 , 93–250. (Обзор)
- ^ Майкл Б. Смит и Джерри Марч: Передовая органическая химия Марча, стр. 1659-1673. Джон Уайли и сыновья, 2007 г. ISBN 978-0-471-72091-1
- ^ Уильямс, Р.В., Chem. Ред. 2001, 101 (5), 1185–1204.
- ^ Кальдре, Дайнис; Глисон, Джеймс Л. (2016). «Органокаталитическая перегруппировка копов» . Angewandte Chemie, международное издание . 55 (38): 11557–11561. дои : 10.1002/anie.201606480 . ISSN 1521-3773 . ПМИД 27529777 .
- ^ Тан, Сюэке ; кальциевая зависимость стигциклаз» . RSC Advances . 9 (23): 13182–13185. : 10.1039 /C9RA00960D . ISSN 2046-2069 . PMC 9063808. . PMID 35520811 doi
- ^ Тан, Мань-Ченг; Цзоу, И; Ватанабэ, Кендзи; Уолш, Кристофер Т.; Тан, И (26 апреля 2017 г.). «Окислительная циклизация в биосинтезе природных продуктов» . Химические обзоры . 117 (8): 5226–5333. doi : 10.1021/acs.chemrev.6b00478 . ISSN 0009-2665 . ПМК 5406274 . ПМИД 27936626 .
- ^ Синтез кетонов путем термической изомеризации 3-гидрокси-1,5-гексадиенов. Перегруппировка Окси-Коупа Джером А. Берсон, Мейтленд Джонс, младший Дж. Ам. хим. Соц. 1964 год ; 86(22); 5019–5020. два : 10.1021/ja01076a067
- ^ Ступенчатые механизмы перегруппировки окси-копа Джером А. Берсон и Мейтленд Джонс, стр. 5017–5018; Дж. Ам. хим. Соц. 1964 год ; два : 10.1021/ja01076a066
- ^ Кэри, Фрэнсис А.; Сундберг, Ричард Дж. (2007). Продвинутая органическая химия: Часть B: Реакции и синтез (5-е изд.). Нью-Йорк: Спрингер. стр. 555–556. ISBN 978-0387683546 .
- ^ Кэри, Фрэнсис А.; Сундберг, Ричард Дж. (2007). Продвинутая органическая химия: Часть B: Реакции и синтез (5-е изд.). Нью-Йорк: Спрингер. п. 556. ИСБН 978-0387683546 .
- ^ Эванс, Д.А.; Голоб, А.М. (1975). «[3,3]Сигматропные перегруппировки 1,5-диеналкоксидов. Мощное ускоряющее действие алкоксидного заместителя». Журнал Американского химического общества . 97 (16): 4765–4766. дои : 10.1021/ja00849a054 .
- ^ Шрайбер, Стюарт Л.; Сантини, Конрад (1984). «Олефиновый путь к циклобутеновому плацдарму к половому феромону американских тараканов, перипланону-Б». Журнал Американского химического общества . 106 (14): 4038–4039. дои : 10.1021/ja00326a028 .

