Комплекс Васьки

| |
| |

| |

| |
| Имена | |
|---|---|
| Название ИЮПАК
( SP -4-1)-карбонилхлорид
| |
| Другие имена
Иридий(I)бис(трифенилфосфин)
карбонилхлорид Комплекс Васьки Подворье Васьки | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.035.386 |
| Номер ЕС |
|
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
| Характеристики | |
| IrCl(CO)[P(C 6 H 5 ) 3 ] 2 . | |
| Молярная масса | 780.25 g/mol |
| Появление | желтые кристаллы |
| Температура плавления | 215 ° C (419 ° F, 488 К) ( разлагается ) |
| Точка кипения | 360 ° С (680 ° F, 633 К) |
| стелька | |
| Структура | |
| кв. плоский | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
никто |
| СГС Маркировка : | |
 
| |
| Опасность | |
| Х301 , Х302 , Х311 , Х312 , Х315 , Х319 , Х331 , Х332 , Х335 | |
| P261 , P264 , P270 , P271 , P280 , P301+P310 , P301+P312 , P302+P352 , P304+P312 , P304+P340 , P305+P351+P338 , P311 , P312 , P321 , P322 , P330 , P332+P313 , P337+P313 , P361 , P362 , P363 , P403+P233 , P405 , P501 | |
| Родственные соединения | |
Другие анионы
|
IrI(CO)[P(C 6 H 5 ) 3 ] 2 |
Другие катионы
|
RhCl(CO)[ C6H5 P 3 ) 2 ] ( |
Родственные соединения
|
Pd[P(C 6 H 5 ) 3 ] 4 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
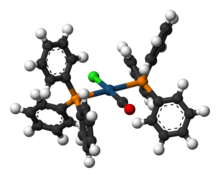
Комплекс Васьки — это тривиальное название химического соединения транс -карбонилхлорбис(трифенилфосфин)иридий(I), которое имеет формулу IrCl(CO)[P(C 6 H 5 ) 3 ] 2 . Этот квадратный плоский диамагнитный металлоорганический комплекс состоит из центрального атома иридия, связанного с двумя взаимно транс -трифенилфосфиновыми лигандами , окисью углерода и ионом хлорида . Впервые о комплексе сообщили Дж. У. ДиЛуцио и Лаури Васка в 1961 году. [ 1 ] Комплекс Васки может подвергаться окислительному присоединению и отличается способностью обратимо связываться с О 2 . Это ярко-желтое кристаллическое твердое вещество.
Подготовка
[ редактировать ]Синтез включает нагревание практически любой соли хлорида иридия с трифенилфосфином и источником монооксида углерода . Самый популярный метод использует диметилформамид (ДМФ) в качестве растворителя, а иногда анилин для ускорения реакции добавляется . Другой популярный растворитель — 2-метоксиэтанол . Реакцию обычно проводят в атмосфере азота. В синтезе трифенилфосфин служит одновременно лигандом и восстановителем, а карбонильный лиганд образуется в результате разложения диметилформамида, вероятно, путем деинсерции промежуточных частиц Ir-C(O)H. Ниже приведено возможное сбалансированное уравнение этой сложной реакции. [ 2 ]
- IrCl 3 (H 2 O) 3 + 3 P(C 6 H 5 ) 3 + HCON(CH 3 ) 2 + C 6 H 5 NH 2 → IrCl(CO)[P(C 6 H 5 ) 3 ] 2 + [ (CH 3 ) 2 NH 2 ]Cl + OP(C 6 H 5 ) 3 + [C 6 H 5 NH 3 ]Cl + 2 Н 2 О
Типичными источниками иридия, используемыми в этом препарате, являются IrCl 3 · x H 2 O и H 2 IrCl 6 .
Реакции
[ редактировать ]Исследования комплекса Васки помогли создать концептуальную основу для гомогенного катализа . Комплекс Васки с 16 валентными электронами считается «координационно ненасыщенным» и, таким образом, может связываться с одним двухэлектронным или двумя одноэлектронными лигандами, становясь электронно насыщенными 18 валентными электронами. Присоединение двух одноэлектронных лигандов называется окислительным присоединением . [ 3 ] При окислительном присоединении степень окисления иридия повышается от Ir(I) до Ir(III). Четырехкоординатное плоско-квадратное расположение в стартовом комплексе превращается в октаэдрическое шестикоординатное произведение. Комплекс Васки подвергается окислительному присоединению с обычными окислителями, такими как галогены, сильные кислоты, такие как HCl, и другими молекулами, которые, как известно, реагируют как электрофилы , такие как йодметан (CH 3 I).
Комплекс Васки обратимо связывает О 2 :
- IrCl(CO)[P(C 6 H 5 ) 3 ] 2 + O 2 ⇌ IrCl(CO)[P(C 6 H 5 ) 3 ] 2 O 2
Дикислородный лиганд связан с Ir обоими атомами кислорода, что называется боковой связью. В миоглобине и гемоглобине, напротив, O 2 связывается с конца, прикрепляясь к металлу только через один из двух атомов кислорода. Образующийся дикислородный аддукт возвращается в исходный комплекс при нагревании или продувке раствора инертным газом, о чем свидетельствует изменение цвета с оранжевого обратно на желтый. [ 2 ]
Спектроскопия
[ редактировать ]Инфракрасная спектроскопия может быть использована для анализа продуктов окислительного присоединения к комплексу Васки, поскольку реакции вызывают характерные сдвиги частоты растяжения координированного монооксида углерода. [ 4 ] Эти сдвиги зависят от количества π-обратных связей, допускаемых вновь связанными лигандами. Частоты растяжения CO для комплекса Васки и лигандов, добавленных окислительно, документированы в литературе. [ 5 ]
- Комплекс Васьки: 1967 см. −1
- Комплекс Васьки + О 2 : 2015 см. −1
- Комплекс Васьки + МэИ: 2047 см. −1
- Комплекс Васьки + I 2 : 2067 см. −1
Окислительное присоединение с образованием продуктов Ir(III) уменьшает π-связь от Ir к C, что вызывает увеличение частоты карбонильной валентной полосы. Изменение частоты растяжения зависит от добавленных лигандов, но частота всегда превышает 2000 см-1. −1 для комплекса Ir(III).
История
[ редактировать ]Самое раннее упоминание IrCl(CO)(PPh 3 ) 2 принадлежит Васке и ДиЛуцио. [ 6 ] Близкородственный IrBr(CO)(PPh 3 ) 2 был описан в 1959 году Марией Анголеттой, которая получила комплекс обработкой IrBr(CO) 2 ( п -толуидин) PPh 3 в растворе ацетона. [ 7 ] В 1957 году Линда Валлерино сообщила о RhCl(CO)(PPh 3 ) 2 . [ 8 ]
Ссылки
[ редактировать ]- ^ Лаури Васька ; Дж. В. ДиЛуцио (1961). «Карбонильные и гидридо-карбонильные комплексы иридия по реакции со спиртами. Гидридокомплексы по реакции с кислотой». Журнал Американского химического общества . 83 (12): 2784–2785. дои : 10.1021/ja01473a054 .
- ^ Перейти обратно: а б Джиролами, Г.С.; Раухфус, ТБ; Анжеличи, Р.Дж. (1999). Синтез и техника в неорганической химии (3-е изд.). Саусалито, Калифорния: Университетские научные книги. п. 190. ИСБН 0-935702-48-2 .
- ^ Лабингер, Джей А. (2015). «Учебник по окислительному присоединению». Металлоорганические соединения . 34 (20): 4784–4795. doi : 10.1021/acs.organomet.5b00565 .
- ^ Лаури Васька; ДиЛуцио, JW (1962). «Активация водорода комплексом переходного металла в нормальных условиях, приводящая к стабильному молекулярному дигидриду». Журнал Американского химического общества . 84 (4): 679–680. дои : 10.1021/ja00863a040 .
- ^ Крэбтри, Р. (2001). Металлоорганическая химия переходных металлов (3-е изд.). Канада: Джон Уайли и сыновья. п. 152.
- ^ Рейн У. Кирсс (2013). «Пятьдесят лет Васькиному подворью». Бык. Хист. Хим . 38 .
- ^ Мария Анголетта (1959). «Карбонильные производные иридия. Примечание III. Галогениды дикарбониламиридия (I)». Итальянский химический журнал . 89 : 2359–2370.
- ^ Валларино, Л. (1957). «Карбонильные комплексы родия. I. Комплексы с триарилфосфинами, триариларсинами и триарилстибинами». Журнал Химического общества : 2287–92. дои : 10.1039/jr9570002287 .