Селен
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Селен | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | / s ɪ ˈ l iː n i ə m / | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Появление | серые металлические, красные и стекловидно-черные (без изображения) аллотропы | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес А р °(Се) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Селен в таблице Менделеева | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный номер ( Z ) | 34 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа | группа 16 (халькогены) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Период | период 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Блокировать | p-блок | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [ Ар ] 3d 10 4 с 2 4р 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроны на оболочку | 2, 8, 18, 6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза в СТП | твердый | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 494 К (221 °С, 430 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка кипения | 958 К (685 °С, 1265 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность (около комнатной температуры ) | серый: 4,81 г/см 3 альфа: 4,39 г/см 3 стекловидное тело: 4,28 г/см 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| в жидком состоянии (при температуре плавления ) | 3,99 г/см 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Критическая точка | 1766 К, 27,2 МПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота плавления | серый: 6,69 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота испарения | 95,48 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная теплоемкость | 25,363 Дж/(моль·К) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Давление пара
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомные свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стадии окисления | −2 , −1, 0, [3] +1, [4] +2 , +3, +4 , +5, +6 (сильнокислотный оксид ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 2,55. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Энергии ионизации |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный радиус | эмпирический: 120 вечера | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 120±16.00 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Радиус Ван-дер-Ваальса | 190 вечера | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Другие объекты недвижимости | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Естественное явление | первобытный | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кристаллическая структура | серый: шестиугольный ( hP3 ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Константы решетки | а = 16:436,46 с = 495,77 вечера (при 20 ° C) [5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тепловое расширение | аморфный: 37 мкм/(м⋅К) (при 25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплопроводность | аморфный: 0,519 Вт/(м⋅К) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнитный заказ | диамагнитный [6] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная магнитная восприимчивость | −25.0 × 10 −6 см 3 /моль (298 К) [7] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль Юнга | 10 ГПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль сдвига | 3,7 ГПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Объемный модуль | 8,3 ГПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Скорость звука тонкого стержня | 3350 м/с (при 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| коэффициент Пуассона | 0.33 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по шкале Мооса | 2.0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Бринеллю | 736 МПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Номер CAS | 7782-49-2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| История | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Мы | в честь Селены , греческой богини луны. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Открытие и первая изоляция | Йёнс Якоб Берцелиус и Иоганн Готлиб Ган (1817 г.) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изотопы селена | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Селен — химический элемент ; он имеет символ Se и атомный номер 34. Это неметалл (реже считается металлоидом ) со свойствами, занимающими промежуточное положение между элементами выше и ниже в таблице Менделеева , серой и теллуром , а также имеет сходство с мышьяком . [9] Он редко встречается в элементарном состоянии или в виде чистых рудных соединений в земной коре . Селен (от древнегреческого σελήνη ( selḗnē ) «луна») был открыт в 1817 году Йёнсом Якобом Берцелиусом , который отметил сходство нового элемента с ранее открытым теллуром (названным в честь Земли).
Селен встречается в сульфидных рудах металлов , где он частично заменяет серу. В промышленных масштабах селен производится как побочный продукт при переработке этих руд, чаще всего во время производства. Минералы, представляющие собой чистые селенидные или селенатные соединения, известны, но редки. Сегодня основными коммерческими сферами применения селена являются производство стекла и производство пигментов . Селен является полупроводником и используется в фотоэлементах . Приложения в электронике , когда-то важные, в основном заменены кремниевыми полупроводниковыми устройствами. Селен до сих пор используется в нескольких типах устройств перенапряжения постоянного тока защиты от и в одном типе флуоресцентных квантовых точек .
Хотя следовые количества селена необходимы для клеточного функционирования у многих животных, включая человека, как элементарный селен, так и (особенно) соли селена токсичны даже в небольших дозах, вызывая селеноз . [10] Селен указан в качестве ингредиента во многих поливитаминах и других пищевых добавках, а также в детских смесях и является компонентом антиоксидантных ферментов глутатионпероксидазы и тиоредоксинредуктазы (которые косвенно восстанавливают некоторые окисленные молекулы в животных и некоторых растениях), а также в трех ферментах дейодиназах . Потребности растений в селене различаются в зависимости от вида: некоторым растениям требуется относительно большое количество селена, а другим, по-видимому, вообще не требуется. [11]
Характеристики
[ редактировать ]Физические свойства
[ редактировать ]
Селен образует несколько аллотропов , которые преобразуются при изменении температуры , в некоторой степени в зависимости от скорости изменения температуры. Селен, полученный химическими реакциями, обычно представляет собой аморфный порошок кирпично-красного цвета. При быстром плавлении он образует черную стекловидную форму, обычно продаваемую в виде шариков. [12] Структура черного селена нерегулярна и сложна и состоит из полимерных колец, содержащих до 1000 атомов в каждом. Черный селен представляет собой хрупкое блестящее твердое вещество, слабо растворимое в CS 2 . При нагревании он размягчается при 50 °С и превращается в серый селен при 180 °С; температура превращения снижается за счет присутствия галогенов и аминов . [9]
Красные α-, β- и γ-формы получают из растворов черного селена путем изменения скорости испарения растворителя (обычно CS 2 ). Все они имеют относительно низкую моноклинную кристаллическую симметрию ( пространственная группа 14) и содержат почти идентичные сморщенные кольца циклооктаселена (Se 8 ) с разным геометрическим расположением, как и в сере . [13] Восемь атомов кольца неэквивалентны (т.е. они не отображаются один на другой посредством какой-либо операции симметрии), и фактически в γ-моноклинной форме половина колец находится в одной конфигурации (и ее зеркальном отображении), а половина в другой. [14] [15] Упаковка наиболее плотна в α-форме. В кольцах Se 8 расстояние Se–Se варьируется в зависимости от того, где находится пара атомов в кольце, но в среднем составляет 233,5 пм, а угол Se–Se–Se составляет в среднем 105,7°. Другие аллотропы селена могут содержать кольца Se 6 или Se 7 . [9]
Наиболее стабильная и плотная форма селена — серая и имеет хиральную гексагональную кристаллическую решетку (пространственная группа 152 или 154 в зависимости от хиральности). [16] состоящий из спиральных полимерных цепей, где расстояние Se-Se составляет 237,3 пм, а угол Se-Se-Se составляет 103,1 °. Минимальное расстояние между цепями — 343,6 м. Серый селен образуется при умеренном нагревании других аллотропов, медленном охлаждении расплавленного селена или конденсации паров селена чуть ниже точки плавления. В то время как другие формы селена являются изоляторами , серый селен является полупроводником, обладающим значительной фотопроводимостью . В отличие от других аллотропов, он нерастворим в CS 2 . [9] Он устойчив к окислению воздухом и не подвергается воздействию неокисляющих кислот . С сильными восстановителями образует полиселениды. Селен не демонстрирует таких изменений вязкости, как сера при постепенном нагревании. [12] [17]
изотопы
[ редактировать ]Селен имеет семь встречающихся в природе изотопов . Пять из них, 74 с 76 с 77 с 78 с 80 Se, стабильны, с 80 Se является наиболее распространенным (49,6% естественного содержания). В природе также встречается долгоживущий первичный радионуклид. 82 Se, с периодом полураспада 8,76×10. 19 годы. [8] Непервичный радиоизотоп 79 Se также встречается в незначительных количествах в урановых рудах как продукт ядерного деления . Селен также имеет множество нестабильных синтетических изотопов, начиная от 64 Смотри это 95 Се; наиболее стабильными являются 75 Se с периодом полураспада 119,78 дней и 72 Se с периодом полураспада 8,4 дня. [18] Изотопы более легкие, чем стабильные изотопы, в первую очередь подвергаются бета-распаду до изотопов мышьяка , а изотопы более тяжелые, чем стабильные изотопы, подвергаются бета-распаду до изотопов брома с некоторыми незначительными ветвями эмиссии нейтронов в самых тяжелых известных изотопах.
| Изотоп | Природа | Источник | Период полураспада |
|---|---|---|---|
| 74 Се | Первозданный | Стабильный | |
| 76 Се | Первозданный | Стабильный | |
| 77 Се | Первозданный | Продукт деления | Стабильный |
| 78 Се | Первозданный | Продукт деления | Стабильный |
| 79 Се | След | Продукт деления | 327 000 в год [19] [20] |
| 80 Се | Первозданный | Продукт деления | Стабильный |
| 82 Се | Первозданный | Продукт деления* | 8.76 × 10 19 тот [8] [а] |
Химические соединения
[ редактировать ]Соединения селена обычно существуют в степенях окисления -2, +2, +4 и +6.
Халькогенные соединения
[ редактировать ]
Селен образует два оксида : диоксид селена (SeO2 ) и триоксид селена (SeO3 ) . Диоксид селена образуется при сгорании элементарного селена: [12]
Это полимерное твердое вещество, образующее мономерные молекулы SeO 2 в газовой фазе. Растворяется в воде с образованием селенистой кислоты H 2 SeO 3 . Селенистую кислоту также можно получить непосредственно путем окисления элементарного селена азотной кислотой : [21]
В отличие от серы, которая образует стабильный триоксид , триоксид селена термодинамически нестабилен и при температуре выше 185 °C разлагается на диоксид: [12] [21]
Триоксид селена получают в лаборатории реакцией безводного селената калия (K 2 SeO 4 ) и триоксида серы (SO 3 ). [22]
Соли селенистой кислоты называются селенитами. К ним относятся селенит серебра (Ag 2 SeO 3 ) и селенит натрия (Na 2 SeO 3 ).
Сероводород реагирует с водным раствором селенистой кислоты с образованием дисульфида селена :
Дисульфид селена состоит из 8-членных колец. Он имеет приблизительный состав SeS 2 , с отдельными кольцами разного состава, например Se 4 S 4 и Se 2 S 6 . Дисульфид селена использовался в шампунях в качестве средства против перхоти , ингибитора в химии полимеров, красителя для стекла и восстановителя в фейерверках . [21]
Триоксид селена может быть синтезирован путем дегидратации селеновой кислоты H 2 SeO 4 , которая сама получается окислением диоксида селена перекисью водорода : [23]
Горячая концентрированная селеновая кислота реагирует с золотом с образованием селената золота (III). [24]
Галогенные соединения
[ редактировать ]Селен реагирует с фтором с образованием гексафторида селена :
По сравнению со своим серным аналогом ( гексафторидом серы ) гексафторид селена (SeF 6 ) более реактивен и является токсичным раздражителем легких . [25] Элементы с разной стехиометрией вместо этого образуют тетрафторид селена лабораторного масштаба , фторирующий агент .
Единственными стабильными хлоридами являются тетрахлорид селена (SeCl 4 ) и монохлорид селена (Se 2 Cl 2 ), который может быть более известен как хлорид селена (I) и по структуре аналогичен дихлориду дисеры . Метастабильные растворы дихлорида селена могут быть приготовлены из сульфурилхлорида и селена (вместо этого в результате реакции элементов образуется тетрахлорид ) и представляют собой важный реагент при получении соединений селена (например, Se 7 ). Все соответствующие бромиды известны и имеют ту же стабильность и структуру, что и хлориды. [26]
Йодиды . селена малоизвестны, и долгое время считалось, что они не существуют [27] Имеются ограниченные спектроскопические доказательства того, что низшие иодиды могут образовываться в двухэлементных растворах с неполярными растворителями, такими как сероуглерод. [28] и четыреххлористый углерод ; [27] но даже они, по-видимому, разлагаются при освещении . [29]
Некоторые оксигалогениды селена — селенинилфторид (SeOF 2 ) и оксихлорид селена (SeOCl 2 ) — использовались в качестве специальных растворителей. [12]
Селениды металлов
[ редактировать ]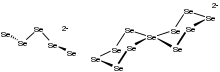
Аналогично поведению других халькогенов селен образует селеноводород H 2 Se. Это сильно пахучий , токсичный и бесцветный газ. Он более кислый, чем H 2 S. В растворе ионизируется до HSe. − . Селенид-дианион Se 2− образует множество соединений, включая минералы, из которых селен получают в промышленных масштабах. Иллюстративные селениды включают селенид ртути (HgSe), селенид свинца (PbSe), селенид цинка (ZnSe) и диселенид меди, индия-галлия (Cu(Ga,In)Se 2 ). Эти материалы являются полупроводниками . В случае металлов с высокими электроположительными свойствами, таких как алюминий , эти селениды склонны к гидролизу, который можно описать этим идеализированным уравнением: [12]
Селениды щелочных металлов реагируют с селеном с образованием полиселенидов Se . 2−
n , которые существуют в виде цепочек и колец.
Другие соединения
[ редактировать ]Тетраселен тетранитрид Se 4 N 4 представляет собой взрывчатое оранжевое соединение, аналогичное тетранитриду тетраселена (S 4 N 4 ). [12] [31] [32] Его можно синтезировать реакцией тетрахлорида селена (SeCl 4 ) с [((CH
3 )
3 Си)
2Н ]
2 Се . [33]
Селен реагирует с цианидами с образованием селеноцианатов : [12]
Селенорганические соединения
[ редактировать ]Селен, особенно во II степени окисления, образует множество органических производных. Структурно они аналогичны соответствующим сероорганическим соединениям . Особенно распространены селениды (R 2 Se, аналоги тиоэфиров ), диселениды (R 2 Se 2 , аналоги дисульфидов ) и селенолы (RSeH, аналоги тиолов ). Представители селенидов, диселенидов и селенолов включают соответственно селенометионин , дифенилдиселенид и бензолселенол . Сульфоксид реакция в химии серы представлен в химии селена селеноксидами (формула RSe(O)R), которые являются промежуточными продуктами органического синтеза, о чем свидетельствует удаления селеноксида . В соответствии с тенденциями, указанными правилом двойной связи , селенокетоны R(C=Se)R и селенальдегиды R(C=Se)H наблюдаются редко. [34]
История
[ редактировать ]
Селен ( греческое σελήνη selene означает «Луна») был открыт в 1817 году Йенсом Якобом Берцелиусом и Йоханом Готлибом Ганом . [35] Оба химика владели химическим заводом недалеко от Грипсхольма , Швеция, производящим серную кислоту методом в свинцовой камере . Образцы пирита из шахты Фалунь дали красный твердый осадок в свинцовых камерах, который предположительно был соединением мышьяка, поэтому использование пирита для производства кислоты было прекращено. Берцелиус и Ган, которые хотели использовать пирит, заметили, что красный осадок при сжигании издает запах хрена . Этот запах не был свойственен мышьяку, но аналогичный запах был известен и у соединений теллура . Следовательно, в первом письме Берцелиуса Александру Марсету говорилось, что это соединение теллура. Однако отсутствие соединений теллура в минералах шахты Фалун в конечном итоге заставило Берцелиуса повторно проанализировать красный осадок, и в 1818 году он написал Марсет второе письмо, описывая недавно обнаруженный элемент, похожий на серу и теллур. Из-за его сходства с теллуром, названным в честь Земли, Берцелиус назвал новый элемент в честь Луны . [36] [37]
В 1873 году Уиллоуби Смит обнаружил, что электропроводность серого селена. свет влияет на [38] [39] Это привело к его использованию в качестве ячейки для восприятия света. Первые коммерческие продукты с использованием селена были разработаны Вернером Сименсом в середине 1870-х годов. Селеновая ячейка использовалась в фотофоне, разработанном Александром Грэмом Беллом в 1879 году. Селен передает электрический ток, пропорциональный количеству света, падающего на его поверхность. Это явление было использовано при проектировании люксметров и подобных устройств. Полупроводниковые свойства селена нашли множество других применений в электронике. [40] [41] [42] Разработка селеновых выпрямителей началась в начале 1930-х годов, и они заменили медно-оксидные выпрямители, поскольку были более эффективными. [43] [44] [45] Они использовались в коммерческих целях до 1970-х годов, после чего были заменены менее дорогими и даже более эффективными кремниевыми выпрямителями .
Позднее медики обратили внимание на селен из-за его токсичности для промышленных рабочих. Селен также был признан важным ветеринарным токсином, который наблюдается у животных, которые ели растения с высоким содержанием селена. обнаружила первые намеки на специфические биологические функции селена в микроорганизмах В 1954 году биохимик Джейн Пинсент . [46] [47] В 1957 году было обнаружено, что он необходим для жизни млекопитающих. [48] [49] В 1970-х годах было показано, что он присутствует в двух независимых наборах ферментов . За этим последовало открытие селеноцистеина в белках. В 1980-х годах было показано, что селеноцистеин кодируется кодоном UGA . Механизм перекодирования был отработан сначала у бактерий , а затем у млекопитающих (см. элемент SECIS ). [50]
возникновение
[ редактировать ]
Самородный (т.е. элементарный) селен — редкий минерал, который обычно не образует хороших кристаллов, но когда это происходит, они представляют собой крутые ромбоэдры или крошечные игольчатые (волосообразные) кристаллы. [51] Выделение селена часто осложняется присутствием других соединений и элементов.
Селен встречается в природе в ряде неорганических форм, включая селенид , селенат и селенит , но эти минералы встречаются редко. Обычный минерал селенит не является минералом селена и не содержит ионов селенита , а представляет собой разновидность гипса (гидрат сульфата кальция), названного как селен в честь Луны задолго до открытия селена. Селен чаще всего встречается в виде примеси, заменяя небольшую часть серы в сульфидных рудах многих металлов. [52] [53]
В живых системах селен содержится в аминокислотах селенометионин , селеноцистеин и метилселеноцистеин . В этих соединениях селен играет роль, аналогичную роли серы. Другое встречающееся в природе селенорганическое соединение — диметилселенид . [54] [55]
Некоторые почвы богаты селеном, а могут биоконцентрировать некоторые растения селен. В почвах селен чаще всего встречается в растворимых формах, таких как селенат (аналог сульфата), которые очень легко вымываются в реки со стоками. [52] [53] Океанская вода содержит значительное количество селена. [56] [57]
Типичные фоновые концентрации селена не превышают 1 нг/м. 3 в атмосфере; 1 мг/кг в почве и растительности и 0,5 мкг/л в пресной и морской воде. [58]
Антропогенные источники селена включают сжигание угля, а также добычу и плавку сульфидных руд. [59]
Производство
[ редактировать ]Селен чаще всего производится из селенида во многих сульфидных рудах , таких как медь , никель или свинец . Электролитическое рафинирование металлов особенно продуктивно по селену как побочному продукту, получаемому из анодного шлама медеперерабатывающих заводов. Другим источником был шлам из свинцовых камер сернокислотных заводов - процесс, который больше не используется. Селен можно очистить из этих грязей несколькими методами. Однако большая часть элементарного селена является побочным продуктом переработки меди или производства серной кислоты . [60] [61] С момента изобретения производство меди с помощью экстракции растворителем и электролиза (SX/EW) обеспечивает все большую долю мировых поставок меди. [62] Это меняет доступность селена, поскольку лишь сравнительно небольшая часть селена в руде выщелачивается с медью. [63]
Промышленное производство селена обычно предполагает извлечение диоксида селена из остатков, полученных при очистке меди. Затем обычное производство из остатка начинается с окисления карбонатом натрия с образованием диоксида селена, который смешивается с водой и подкисляется с образованием селенистой кислоты ( окисления стадия ). Селенистую кислоту барботируют диоксидом серы ( этап восстановления ) с получением элементарного селена. [64] [65]
В 2011 году во всем мире было произведено около 2000 тонн селена, в основном в Германии (650 т), Японии (630 т), Бельгии (200 т) и России (140 т), а общие запасы оцениваются в 93 000 т. Эти данные не включают двух крупных производителей: США и Китай. Предыдущий резкий рост наблюдался в 2004 году с 4–5 долларов до 27 долларов за фунт. Цена была относительно стабильной в течение 2004–2010 годов и составляла около 30 долларов США за фунт (партиями по 100 фунтов), но в 2011 году выросла до 65 долларов США за фунт. Потребление в 2010 году распределялось следующим образом: металлургия – 30%, производство стекла – 30%, сельское хозяйство – 10%, химикаты и пигменты – 10% и электроника – 10%. Китай является доминирующим потребителем селена (1500–2000 тонн в год). [66]
Приложения
[ редактировать ]Электролиз марганца
[ редактировать ]При электровыделении марганца добавление диоксида селена снижает мощность, необходимую для работы электролизеров . Китай является крупнейшим потребителем диоксида селена для этих целей. На каждую тонну марганца используется в среднем 2 кг оксида селена. [66] [67]
Производство стекла
[ редактировать ]Наибольшее коммерческое использование селена, составляющее около 50% потребления, приходится на производство стекла. Соединения селена придают стеклу красный цвет. Этот цвет нейтрализует зеленые или желтые оттенки, возникающие из-за примесей железа, типичных для большинства стекол. Для этого добавляют различные соли селенита и селената. Для других применений может потребоваться красный цвет, получаемый смесями CdSe и CdS. [68]
Сплавы
[ редактировать ]Селен используется вместе с висмутом в латуни для замены более токсичного свинца . Регулирование содержания свинца в питьевой воде, например, в США, с помощью Закона о безопасной питьевой воде 1974 года, сделало необходимым сокращение содержания свинца в латуни. Новая латунь продается под названием EnviroBrass. [69] Подобно свинцу и сере, селен улучшает обрабатываемость стали в концентрациях около 0,15%. [70] [71] Селен обеспечивает такое же улучшение обрабатываемости медных сплавов. [72]
Литий-селеновые батареи
[ редактировать ]Литий-селеновая (Li-Se) батарея — одна из наиболее перспективных систем хранения энергии в семействе литиевых батарей. [73] Батарея Li-Se является альтернативой литий-серной батарее с преимуществом высокой электропроводности.
Солнечные батареи
[ редактировать ]Селен использовался в качестве фотопоглощающего слоя в первом твердотельном солнечном элементе, который был продемонстрирован английским физиком Уильямом Гриллсом Адамсом и его учеником Ричардом Эвансом Дэем в 1876 году. [74] Всего через несколько лет Чарльз Фриттс изготовил первый тонкопленочный солнечный элемент, также используя селен в качестве фотопоглотителя. Однако с появлением кремниевых солнечных элементов в 1950-х годах исследования тонкопленочных солнечных элементов из селена пошли на спад. В результате рекордная эффективность в 5,0%, продемонстрированная Токио Накада и Акио Куниока в 1985 году, оставалась неизменной более 30 лет. [75] В 2017 году исследователи из IBM достигли нового рекорда эффективности в 6,5% за счет перепроектирования структуры устройства. [76] После этого достижения селен вновь приобрел интерес как широкозонный фотопоглотитель с возможностью интеграции в тандеме с фотопоглотителями с более низкой запрещенной зоной. [77] В 2024 году был продемонстрирован первый тандемный солнечный элемент на основе селена, демонстрирующий селеновую верхнюю ячейку, монолитно интегрированную с кремниевой нижней ячейкой. [78] Однако значительный дефицит напряжения холостого хода в настоящее время является основным ограничивающим фактором для дальнейшего повышения эффективности, что требует разработки стратегий устранения дефектов в тонких пленках селена для увеличения срока службы носителей . [79] На данный момент единственная стратегия устранения дефектов, которая была исследована для тонкопленочных солнечных элементов из селена, включает кристаллизацию селена с помощью лазера . [80]
Фотопроводники
[ редактировать ]Тонкие пленки аморфного селена (α-Se) нашли применение в качестве фотопроводников в плоских детекторах рентгеновского излучения . В этих детекторах используется аморфный селен для захвата и преобразования падающих рентгеновских фотонов непосредственно в электрический заряд. Селен был выбран для этого применения среди других полупроводников благодаря сочетанию его благоприятных технологических и физических свойств: [81] [82]
- Аморфный селен имеет низкую температуру плавления, высокое давление паров и однородную структуру. Эти три свойства позволяют быстро и легко наносить однородные пленки большой площади толщиной до 1 мм со скоростью 1–5 мкм/мин. Их однородность и отсутствие границ зерен, свойственные поликристаллическим материалам, улучшают качество рентгеновского изображения. Между тем, большая площадь необходима для сканирования человеческого тела или предметов багажа.
- Селен менее токсичен, чем многие соединения полупроводников, содержащие мышьяк или тяжелые металлы, такие как ртуть или свинец.
- Подвижность в приложенном электрическом поле достаточно высока как для электронов, так и для дырок, так что в типичном устройстве толщиной 0,2 мм c. 98% электронов и дырок, создаваемых рентгеновскими лучами, собираются на электродах, не захватываясь различными дефектами. Следовательно, чувствительность устройства высока, а его поведение легко описать простыми уравнениями переноса.
Выпрямители
[ редактировать ]Селеновые выпрямители впервые были использованы в 1933 году. В основном их заменили устройства на основе кремния. Одним заметным исключением является защита от скачков напряжения постоянного тока , где превосходные энергетические возможности селеновых подавителей делают их более желательными, чем металлооксидные варисторы . [ нужна ссылка ]
Другое использование
[ редактировать ]Спрос на селен со стороны электронной промышленности снижается. [66] Его фотоэлектрические и фотопроводящие свойства до сих пор используются при фотокопировании . [83] [84] [85] [86] фотоэлементы , люксметры и солнечные элементы . Его использование в качестве фотопроводника в копировальных аппаратах для обычной бумаги когда-то было ведущим применением, но в 1980-х годах применение фотопроводника сократилось (хотя оно все еще было крупным конечным пользователем), поскольку все больше и больше копировальных аппаратов перешли на органические фотопроводники. [ нужна ссылка ]
Селенид цинка был первым материалом для изготовления синих светодиодов , но нитрид галлия . на этом рынке доминирует [87] Селенид кадмия был важным компонентом квантовых точек . [ нужна ссылка ] Листы аморфного селена преобразуют рентгеновские изображения в образцы заряда в ксерорадиографии и в твердотельных плоских рентгеновских камерах. [88] Ионизированный селен (Se+24, где 24 внешних орбитали D, S и P удаляются из-за высоких входных энергий. [ нужны разъяснения ] ) — одна из активных сред, используемых в рентгеновских лазерах. [89] 75 Se используется в качестве источника гамма-излучения в промышленной радиографии. [90]
Селен катализирует некоторые химические реакции, но широко не используется из-за проблем с токсичностью. [91] В рентгеновской кристаллографии включение одного или нескольких атомов селена вместо серы помогает при многоволновой аномальной дисперсии и одноволновой аномальной фазировке дисперсии. [92]
Селен используется при тонировании фотоотпечатков и продается в качестве тонера многими производителями фототехники. Селен усиливает и расширяет тональный диапазон черно-белых фотографических изображений и улучшает стойкость отпечатков. [93] [94] [95] Небольшие количества селенорганических соединений использовались для модификации катализаторов, используемых для вулканизации при производстве каучука. [63] Селен используется в некоторых шампунях против перхоти в форме дисульфида селена, таких как Selsun и Vichy Dereos. [96] бренды.
Загрязнение
[ редактировать ]Загрязнение селеном может повлиять на некоторые водные системы и быть вызвано антропогенными факторами, такими как стоки с сельскохозяйственных ферм и промышленные процессы. [97] Люди, которые едят больше рыбы, обычно более здоровы, чем те, кто ест меньше. [98] что предполагает отсутствие серьезных проблем со здоровьем человека из-за загрязнения селеном, хотя селен потенциально оказывает воздействие на человека. [99]
Отравление водных систем селеном может произойти всякий раз, когда новые сельскохозяйственные стоки проходят через засушливые земли. В результате этого процесса в воду выщелачиваются природные растворимые соединения селена (такие как селенаты), которые затем могут концентрироваться на водно-болотных угодьях по мере испарения воды. Загрязнение водоемов селеном также происходит при выщелачивании селена из золы угольных дымов, при горнодобывающей промышленности и выплавке металлов , переработке сырой нефти и на свалках. [100] Было обнаружено, что высокий уровень селена в водных путях вызывает врожденные заболевания у яйцекладущих видов, включая водно-болотных птиц. [101] и рыба. [102] Повышенные уровни метилртути в пище могут усилить вред токсичности селена для яйцекладущих видов. [103] [104]
Селен биоаккумулируется в водной среде обитания, что приводит к более высоким концентрациям в организмах, чем в окружающей воде. Селенорганические соединения могут концентрироваться зоопланктоном более чем в 200 000 раз , когда концентрация воды находится в диапазоне от 0,5 до 0,8 мкг Se/л. Неорганический селен легче биоаккумулируется в фитопланктоне, чем в зоопланктоне. Фитопланктон может концентрировать неорганический селен в 3000 раз. Дальнейшая концентрация за счет биоаккумуляции происходит вдоль пищевой цепи, поскольку хищники потребляют богатую селеном добычу. Рекомендуется считать концентрацию в воде 2 мкг Se/л крайне опасной для чувствительных рыб и водоплавающих птиц . Отравление селеном может передаваться от родителей потомству через яйцо, и отравление селеном может сохраняться на протяжении многих поколений. Размножение кряквы нарушается при концентрации в рационе 7 мкг Se/л. Многие донные беспозвоночные могут переносить концентрации селена в своем рационе до 300 мкг/л. [105]
Биоаккумуляция селена в водной среде приводит к гибели рыбы в зависимости от вида в пораженной зоне. Однако есть несколько видов, которые пережили эти события и перенесли повышенное содержание селена. Также было высказано предположение, что сезон может повлиять на вредное воздействие селена на рыбу. [106] Существенные физиологические изменения могут произойти у рыб с высоким содержанием селена в тканях. У рыб, подвергшихся воздействию селена, может наблюдаться отек жаберных пластинок , что препятствует диффузии кислорода через жабры и кровотоку внутри жабр. Дыхательная способность еще больше снижается из-за связывания селена с гемоглобином . Другие проблемы включают дегенерацию ткани печени, отек вокруг сердца, повреждение яйцеклеток в яичниках, катаракту и скопление жидкости в полости тела и голове. Селен часто вызывает уродство у плода рыбы, у которого могут возникнуть проблемы с питанием или дыханием; Также часто встречается деформация плавников или позвоночника. Взрослые рыбы могут выглядеть здоровыми, несмотря на их неспособность производить жизнеспособное потомство. [ нужна ссылка ]
Примеры
[ редактировать ]В озере Бельюс , штат Северная Каролина, 19 видов рыб были уничтожены из озера из-за сточных вод с содержанием 150–200 мкг Se/л, сброшенных с 1974 по 1986 год с Duke Energy угольной электростанции . В Национальном заповеднике дикой природы Кестерсон в Калифорнии тысячи рыб и водоплавающих птиц были отравлены селеном, содержащимся в ирригационных дренажных системах. [ нужна ссылка ]
Биологическая роль
[ редактировать ]| Опасности | |
|---|---|
| NFPA 704 (огненный алмаз) | |
Несмотря на то, что селен в больших дозах токсичен, он является важным микроэлементом для животных. В растениях он встречается как побочный минерал. [107] иногда в токсичных пропорциях в кормах (некоторые растения могут накапливать селен в качестве защиты от поедания животными, [108] но другие растения, такие как лосось , требуют селена, и их рост указывает на присутствие селена в почве). [109] Считается, что содержание селена в организме человека находится в пределах 13–20 мг. [110]
Селен является компонентом необычных аминокислот селеноцистеина и селенометионина . [ нужна ссылка ] У людей селен является питательным микроэлементом , который действует как кофактор для восстановления антиоксидантных . ферментов, таких как глутатионпероксидазы [111] и некоторые формы тиоредоксинредуктазы, обнаруженные у животных и некоторых растений (этот фермент встречается во всех живых организмах, но не все его формы в растениях требуют селена). [ нужна ссылка ] Семейство ферментов глутатионпероксидазы (GSH-Px) катализирует реакции, которые удаляют активные формы кислорода, такие как перекись водорода и органические гидропероксиды . [ нужна ссылка ]
Щитовидная железа и каждая клетка, которая использует гормон щитовидной железы, также используют селен. [112] который является кофактором трех из четырех известных типов дейодиназ гормонов щитовидной железы , которые активируют, а затем деактивируют различные гормоны щитовидной железы и их метаболиты; Йодтирониндейодиназы представляют собой подсемейство ферментов дейодиназ, которые используют селен в качестве редкой аминокислоты селеноцистеина. Только дейодиназа йодтирозиндейодиназа , которая воздействует на последние продукты распада гормона щитовидной железы, не использует селен. [113] Селен может также ингибировать болезнь Хашимото в щитовидной железе, при которой собственные клетки щитовидной железы подвергаются атаке как чужеродные. Сообщается о снижении антител к ТПО на 21% при употреблении с пищей 0,2 мг селена. [114]
Повышенное содержание селена в рационе снижает последствия токсичности ртути, [115] [116] [117] хотя он эффективен только при низких и умеренных дозах ртути. [118] Имеющиеся данные свидетельствуют о том, что молекулярные механизмы токсичности ртути включают необратимое ингибирование селеноферментов, которые необходимы для предотвращения и устранения окислительных повреждений в мозге и эндокринных тканях. [119] [120] Селенсодержащее соединение селенонеин присутствует в крови голубого тунца . [121] [122] Некоторые виды растений считаются индикаторами высокого содержания селена в почве, поскольку для их роста требуется высокий уровень селена. Основными растениями-индикаторами селена являются виды Astragalus (в том числе некоторые виды мушмоса ), шлейф принца ( Stanleya sp.), астры древесные ( Xylorhiza sp.) и золотарник ложный ( Oonopsis sp.). [123]
Эволюция в биологии
[ редактировать ]Примерно три миллиарда лет назад прокариотические семейства селенопротеинов стимулировали эволюцию селеноцистеина, аминокислоты. Селен включен в несколько семейств прокариотических селенопротеинов у бактерий, архей и эукариот в виде селеноцистеина, [124] где селенопротеиновые пероксиредоксины защищают бактериальные и эукариотические клетки от окислительного повреждения. Семейства селенопротеинов GSH-Px и дейодиназ эукариотических клеток, по-видимому, имеют бактериальное филогенетическое происхождение. Селеноцистеинсодержащая форма встречается у таких разнообразных видов, как зеленые водоросли, диатомовые водоросли, морские ежи, рыбы и куры. Ферменты селена участвуют в небольших восстанавливающих молекулах глутатиона и тиоредоксина . Одно семейство селенсодержащих молекул (глутатионпероксидазы ) разрушает перекись и восстанавливает поврежденные перекисные клеточные мембраны с помощью глутатиона. Другой селенсодержащий фермент у некоторых растений и животных ( тиоредоксинредуктаза ) генерирует восстановленный тиоредоксин, дитиол, который служит источником электронов для пероксидаз, а также важный восстанавливающий фермент рибонуклеотидредуктазу , который делает предшественники ДНК из предшественников РНК. [125]
Микроэлементы, участвующие в активности ферментов GSH-Px и супероксиддисмутазы, например, селен, ванадий , магний , медь и цинк , возможно, отсутствовали в некоторых земных районах с дефицитом минералов. [124] Морские организмы сохранили, а иногда и расширили свои селенопротеомы, тогда как у некоторых наземных организмов селенопротеомы были редуцированы или полностью утрачены. Эти результаты показывают, что, за исключением позвоночных , водная жизнь поддерживает использование селена, тогда как наземная среда обитания приводит к снижению использования этого микроэлемента. [126] Морские рыбы и щитовидная железа позвоночных имеют самую высокую концентрацию селена и йода. Примерно 500 миллионов лет назад пресноводные и наземные растения постепенно оптимизировали выработку «новых» эндогенных антиоксидантов, таких как аскорбиновая кислота (витамин С), полифенолы (включая флавоноиды), токоферолы и т. д. Некоторые из них появились в последние 50–50–150 лет. 200 миллионов лет, в плодах и цветках покрытосеменных растений. Фактически, покрытосеменные растения (доминирующий сегодня тип растений) и большая часть их антиоксидантных пигментов эволюционировали в конце юрского периода. [ нужна ссылка ]
дейодиназы Изоферменты составляют другое семейство эукариотических селеноферментов. Дейодиназы участвуют в регуляции тиреоидных гормонов, участвуя в защите тироцитов от повреждения H 2 O 2 , вырабатываемого для биосинтеза тиреоидных гормонов. [127] Около 200 миллионов лет назад были разработаны новые селенопротеины как ферменты GSH-Px млекопитающих. [128] [129] [130] [131]
Токсичность
[ редактировать ]
Хотя селен является важным микроэлементом , он токсичен, если принимать его в избытке. Превышение допустимого верхнего уровня потребления в 400 микрограммов в день может привести к селенозу. [133] Этот допустимый верхний уровень потребления в 400 мкг основан главным образом на исследовании 1986 года пяти китайских пациентов, у которых наблюдались явные признаки селеноза, и на последующем исследовании с участием тех же пяти человек в 1992 году. [134] Исследование 1992 года показало, что максимально безопасное потребление селена с пищей составляет примерно 800 микрограммов в день (15 микрограммов на килограмм массы тела), но предлагалось потреблять 400 микрограммов в день, чтобы избежать дисбаланса питательных веществ в рационе и согласовываться с данными других стран. . [135] В Китае люди, которые употребляли кукурузу, выращенную в каменном угле (углистом сланце ), чрезвычайно богатом селеном, страдали от токсичности селена. Было показано, что в этом угле содержание селена достигает 9,1%, что является самой высокой концентрацией в угле, когда-либо зарегистрированной. [136]
Признаки и симптомы селеноза включают запах чеснока изо рта, желудочно-кишечные расстройства, выпадение волос, шелушение ногтей, усталость, раздражительность и неврологические нарушения. Крайние случаи селеноза могут проявляться циррозом печени, отеком легких или смертью. [137] Элементарный селен и большинство селенидов металлов обладают относительно низкой токсичностью из-за низкой биодоступности . Напротив, селенаты и селениты обладают окислительным механизмом действия, аналогичным действию триоксида мышьяка , и очень токсичны. Хроническая токсическая доза селенита для человека составляет от 2400 до 3000 мкг селена в день. [138] Селеноводород — чрезвычайно токсичный и едкий газ. [139] Селен также встречается в органических соединениях, таких как диметилселенид, селенометионин , селеноцистеин и метилселеноцистеин , все из которых имеют высокую биодоступность и токсичны в больших дозах.
19 апреля 2009 года 21 пони для поло умерла незадолго до матча Открытого чемпионата США по поло. Три дня спустя аптека опубликовала заявление, в котором объяснялось, что лошади получили неправильную дозу одного из ингредиентов, используемых в составе витаминно-минеральной добавки, которая была неправильно приготовлена в аптеке . Анализ уровня неорганических соединений были в 10–15 раз выше нормы в добавке в крови показал, что концентрации селена в образцах крови , а в образцах печени – в 15–20 раз выше нормы. Позже было подтверждено, что селен является токсичным фактором. [140]

Рыбам и другим диким животным селен необходим для жизни, но в высоких дозах токсичен. Для лосося оптимальная концентрация селена составляет около 1 микрограмма селена на грамм массы всего тела. Гораздо ниже этого уровня молодь лосося умирает от дефицита; [142] намного выше, они умирают от избытка токсичных веществ. [141]
Управление по охране труда (OSHA) установило законный предел ( допустимый предел воздействия ) для селена на рабочем месте на уровне 0,2 мг/м. 3 более 8-часового рабочего дня. Национальный институт охраны труда (NIOSH) установил рекомендуемый предел воздействия (REL) 0,2 мг/м. 3 более 8-часового рабочего дня. На уровне 1 мг/м 3 селен сразу опасен для жизни и здоровья . [144]
Обнаружение в биологических жидкостях
[ редактировать ]Селен можно измерять в крови, плазме, сыворотке или моче для мониторинга чрезмерного воздействия окружающей среды или на рабочем месте, для подтверждения диагноза отравления у госпитализированных жертв или для расследования предполагаемого случая смертельной передозировки. Некоторые аналитические методы способны отличать органические формы элемента от неорганических. Как органические, так и неорганические формы селена в основном преобразуются в организме в конъюгаты моносахаридов (селеносахара) перед выведением с мочой. У онкологических больных, получающих ежедневные пероральные дозы селенотионина, могут достигаться очень высокие концентрации селена в плазме и моче. [145]
Дефицит
[ редактировать ]Дефицит селена может возникнуть у пациентов с тяжелыми нарушениями функции кишечника , у пациентов, находящихся на полном парентеральном питании , и у пациентов с тяжелыми нарушениями функции кишечника. [146] у лиц пожилого возраста (старше 90 лет). Кроме того, в зоне риска находятся люди, зависящие от продуктов питания, выращенных на почвах с дефицитом селена. Хотя в почве Новой Зеландии низкий уровень селена, у жителей не обнаружено вредных последствий для здоровья. [147]
Дефицит селена, определяемый низким (<60% от нормального) уровнем активности селеноферментов в мозге и эндокринных тканях, возникает только тогда, когда низкий уровень селена связан с дополнительным стрессом, например, с сильным воздействием ртути. [148] или повышенный окислительный стресс из-за дефицита витамина Е. [149]
Селен взаимодействует с другими питательными веществами, такими как йод и витамин Е. Влияние дефицита селена на здоровье остается неопределенным, особенно в отношении болезни Кашина-Бека . [150] Кроме того, селен взаимодействует с другими минералами, такими как цинк и медь . Высокие дозы добавок селена у беременных животных могут нарушить соотношение цинк:медь и привести к снижению содержания цинка; в таких случаях лечения следует контролировать уровень цинка. Для подтверждения этих взаимодействий необходимы дальнейшие исследования. [151]
В регионах (например, в различных регионах Северной Америки), где низкие уровни селена в почве приводят к низким концентрациям в растениях, у некоторых видов животных может возникнуть дефицит, если селен не дополняется с помощью диеты или инъекций. [152] жвачные животные Особенно восприимчивы . В целом всасывание пищевого селена у жвачных ниже, чем у других животных, и ниже из кормов, чем из зерна. [153] Жвачные животные, выпасающие определенные корма, например, некоторые белого клевера сорта , содержащие цианогенные гликозиды , могут иметь более высокие потребности в селене. [153] предположительно потому, что цианид высвобождается из агликона под действием глюкозидазы в рубце. [154] а глутатионпероксидаза дезактивируется цианидом, действующим на глутатионовый фрагмент . [155] Новорожденным жвачным животным с риском развития белой мышечной болезни можно вводить как селен, так и витамин Е путем инъекций; ОМП некоторые из миопатий реагируют только на селен, некоторые только на витамин Е, а некоторые и на то и на другое. [156]
Пищевые источники селена
[ редактировать ]Диетический селен поступает из мяса, орехов, круп и грибов. Бразильские орехи являются самым богатым пищевым источником (хотя это зависит от почвы, поскольку бразильскому ореху не требуется большое количество этого элемента для собственных нужд). [157] [158]
Рекомендуемая в США диетическая норма (RDA) селена для подростков и взрослых составляет 55 мкг /день. Селен в качестве пищевой добавки доступен во многих формах, включая мультивитаминные/минеральные добавки, которые обычно содержат 55 или 70 мкг на порцию. Добавки, содержащие селен, обычно содержат 100 или 200 мкг/порцию. [ нужна ссылка ] США В июне 2015 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) опубликовало окончательное правило, устанавливающее требования к минимальному и максимальному уровню содержания селена в детской смеси . [159]
Общие последствия для здоровья
[ редактировать ]Влияние потребления селена на рак изучалось в нескольких клинических и эпидемиологических исследованиях на людях. Селен может играть химиопрофилактическую роль в развития рака предотвращении риска в качестве антиоксиданта и может вызывать иммунный ответ. В низких концентрациях он используется в организме для создания антиоксидантных селенопротеинов , в более высоких дозах, чем обычно, он вызывает гибель клеток. [132]
Селен (в тесной взаимосвязи с йодом ) играет роль в здоровье щитовидной железы. Селен является кофактором трех дейодиназ гормонов щитовидной железы , помогая активировать, а затем деактивировать различные гормоны щитовидной железы и их метаболиты. Изолированный дефицит селена в настоящее время исследуется на предмет его роли в индукции аутоиммунных реакций в щитовидной железе при болезни Хашимото . [160] Показано, что при сочетанном дефиците йода и селена дефицит селена играет защитную роль для щитовидной железы. [161]
См. также
[ редактировать ]Примечания
[ редактировать ]- ^ Для всех практических целей, 82 Se стабилен.
Ссылки
[ редактировать ]- ^ «Стандартные атомные массы: селен» . ЦИАВ . 2013.
- ^ Прохаска, Томас; Ирргехер, Йоханна; Бенефилд, Жаклин; Бёлке, Джон К.; Чессон, Лесли А.; Коплен, Тайлер Б.; Дин, Типинг; Данн, Филип Дж. Х.; Грёнинг, Манфред; Холден, Норман Э.; Мейер, Харро Эй Джей (04 мая 2022 г.). «Стандартные атомные веса элементов 2021 (Технический отчет ИЮПАК)» . Чистая и прикладная химия . дои : 10.1515/pac-2019-0603 . ISSN 1365-3075 .
- ^ Атом Se(0) был идентифицирован с помощью DFT в [ReOSe(2-pySe) 3 ]; видеть Каргнелутти, Роберта; Ланг, Эрнесто С.; Пикини, Пауло; Абрам, Ульрих (2014). «Синтез и структура [ReOSe(2-Se-py)3]: комплекс рения (V) с селеном (0) в качестве лиганда». Неорганическая химия . 45 : 48–50. дои : 10.1016/j.inoche.2014.04.003 . ISSN 1387-7003 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Арбластер, Джон В. (2018). Некоторые значения кристаллографических свойств элементов . Парк материалов, Огайо: ASM International. ISBN 978-1-62708-155-9 .
- ^ Магнитная восприимчивость элементов и неорганических соединений , в Лиде, Д.Р., изд. (2005). Справочник CRC по химии и физике (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5 .
- ^ Уэст, Роберт (1984). CRC, Справочник по химии и физике . Бока-Ратон, Флорида: Издательство компании Chemical Rubber Company. стр. E110. ISBN 0-8493-0464-4 .
- ^ Jump up to: а б с Кондев, ФГ; Ван, М.; Хуанг, WJ; Наими, С.; Ауди, Г. (2021). «Оценка ядерных свойств NUBASE2020» (PDF) . Китайская физика C . 45 (3): 030001. doi : 10.1088/1674-1137/abddae .
- ^ Jump up to: а б с д Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . стр. 751–752. ISBN 978-0-08-037941-8 .
- ^ Фернандес-Баутиста, Тамара; Гомес-Гомес, Беатрис; Паласин-Гарсия, Роберто; Грасия-Лор, Эмма; Перес-Корона, Тереза; Мадрид, Иоланда (15 января 2022 г.). «Анализ распределения биомолекул Se и Hg и видообразования Se в малоизученных белковых фракциях мышечных тканей интенсивно потребляемых рыб методами SEC-UV-ICP-MS и HPLC-ESI-MS/MS» . Таланта . 237 : 122922. doi : 10.1016/j.talanta.2021.122922 . ISSN 0039-9140 . ПМИД 34736659 . S2CID 243761320 .
- ^ Руйл, Джордж. «Ядовитые растения на пастбищах Аризоны» (PDF) . Университет Аризоны. Архивировано из оригинала (PDF) 15 июля 2004 года . Проверено 5 января 2009 г.
- ^ Jump up to: а б с д и ж г час Хаус, Джеймс Э. (2008). Неорганическая химия . Академическая пресса. п. 524. ИСБН 978-0-12-356786-4 .
- ^ Олав Фосс и Виталиюс Яницкис (1980). «Кристаллическая структура γ-моноклинного селена». Журнал Химического общества, Dalton Transactions (4): 624–627. дои : 10.1039/DT9800000624 .
- ^ «Структура β –Se (Al): A_mP32_14_8e» . Энциклопедия кристаллографических прототипов .
- ^ «Се(Ак ) Структура: A_mP64_14_16e» . Энциклопедия кристаллографических прототипов .
- ^ «Структура γ–Se (A8): A_hP3_152_a» . Энциклопедия кристаллографических прототипов .
- ^ Видео нагревания селена на YouTube.
- ^ Ауди, Г.; Кондев, ФГ; Ван, М.; Хуанг, WJ; Наими, С. (2017). «Оценка ядерных свойств NUBASE2016» (PDF) . Китайская физика C . 41 (3): 030001. Бибкод : 2017ChPhC..41c0001A . дои : 10.1088/1674-1137/41/3/030001 .
- ^ «Период полураспада 79 Se" .Physikalisch-Technische Bundesanstalt. 23 сентября 2010. Архивировано из оригинала 27 сентября 2011 года. Проверено 29 мая 2012 года .
- ^ Йорг, Герхард; Бюнеманн, Рольф; Холлас, Саймон; и др. (2010). «Приготовление радиохимически чистых 79 Se и высокоточное определение периода его полураспада». Applied Radiation and Isotopes . 68 (12): 2339–2351. Bibcode : 2010AppRI..68.2339J . doi : 10.1016/j.apradiso.2010.05.006 . PMID 20627600 .
- ^ Jump up to: а б с Виберг, Эгон; Виберг, Нильс; Холлеман, Арнольд Фредерик (2001). Неорганическая химия . Сан-Диего: Академическая пресса. п. 583. ИСБН 978-0-12-352651-9 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 780. ИСБН 978-0-08-037941-8 .
- ^ Зеппельт, К.; Демарто, Дэррил Д. (1980). «Селенонилдифторид». Неорганические синтезы . Том. 20. С. 36–38. дои : 10.1002/9780470132517.ch9 . ISBN 978-0-471-07715-2 . В отчете описан синтез селеновой кислоты.
- ^ Ленхер, В. (апрель 1902 г.). «Действие селеновой кислоты на золото» . Журнал Американского химического общества . 24 (4): 354–355. дои : 10.1021/ja02018a005 .
- ^ Проктор, Ник Х.; Хэтэуэй, Глория Дж. (2004). Хьюз, Джеймс П. (ред.). Химические опасности на рабочем месте Проктора и Хьюза (5-е изд.). Вайли-IEEE. п. 625. ИСБН 978-0-471-26883-3 .
- ^ Сюй, Чжэнтао (2007). Девиланова, Франческо А. (ред.). Справочник по химии халькогенов: новые перспективы в области серы, селена и теллура . Королевское химическое общество. п. 460. ИСБН 978-0-85404-366-8 .
- ^ Jump up to: а б Гопал, Мадхубан; Милн, Джон (октябрь 1992 г.). «Спектроскопические данные о йодидах селена в растворе сероуглерода: Se3I2, Se2I2 и SeI2» . Неорганическая химия . 31 (22): 4530–4533. дои : 10.1021/ic00048a017 . ISSN 0020-1669 .
- ^ Маккалоу, Джеймс Д. (декабрь 1939 г.). «Доказательства существования йодида селена» . Журнал Американского химического общества . 61 (12): 3401–3402. дои : 10.1021/ja01267a052 . ISSN 0002-7863 .
- ^ Рао, MR Асватха Нараяна. «Йодид селена» . В Трудах Индийской академии наук, раздел А , том. 12, стр. 410-415. Спрингер, Индия, 1940 год.
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 763-765. ISBN 978-0-08-037941-8 .
- ^ Вулинз, Дерек; Келли, Пол Ф. (1993). «Реакционная способность Se 4 N 4 в жидком аммиаке». Многогранник . 12 (10): 1129–1133. дои : 10.1016/S0277-5387(00)88201-7 .
- ^ Келли, ПФ; Славин, АМЗ; Сориано-Рама, А. (1997). «Использование Se 4 N 4 и Se(NSO) 2 при получении палладиевых аддуктов динитрида диселена Se 2 N 2 ; кристаллическая структура [PPh
4 ]
2 [Пд
22 комн.
6 (Се
2 Н
2 )] ». Dalton Transactions (4): 559–562. doi : 10.1039/a606311j . - ^ Сиивари, Яри; Чиверс, Тристрам; Лайтинен, Ристо С. (1993). «Простой и эффективный синтез тетранитрида тетраселена». Неорганическая химия . 32 (8): 1519–1520. дои : 10.1021/ic00060a031 .
- ^ Эркер, Г.; Хок, Р.; Крюгер, К.; Вернер, С.; Кларнер, ФГ; Аршвагер-Перл, У. (1990). «Синтез и циклоприсоединения мономерного селенобензофенона». Международное издание «Прикладная химия» на английском языке . 29 (9): 1067–1068. дои : 10.1002/anie.199010671 .
- ^ Берцелиус, Дж. Дж. (1818 г.). «Письмо г-на Берцелиуса г-ну Бертолле о двух новых металлах» . Анналы химии и физики . 2-я серия (на французском языке). 7 : 199–206. Из стр. 203: «Однако, чтобы вспомнить связь последнего с теллуром, я назвал его селеном». (Однако, чтобы вспомнить отношения этого последнего [вещества (а именно, селена)] к теллуру, я назвал его «селеном».)
- ^ Уикс, Мария Эльвира (1932). «Открытие элементов. VI. Теллур и селен». Журнал химического образования . 9 (3): 474. Бибкод : 1932ЖЧЭд...9..474В . дои : 10.1021/ed009p474 .
- ^ Трофаст, Январь (2011). «Открытие Берцелиусом селена» . Химия Интернэшнл . 33 (5): 16–19. PDF
- ^ Смит, Уиллоби (1873). «Действие света на селен» . Журнал Общества инженеров-телеграфистов . 2 (4): 31–33. doi : 10.1049/jste-1.1873.0023 .
- ^ Смит, Уиллоби (20 февраля 1873 г.). «Влияние света на селен при прохождении электрического тока» . Природа . 7 (173): 303. Бибкод : 1873Natur...7R.303. . дои : 10.1038/007303e0 .
- ^ Боннье Корпорейшн (1876 г.). «Действие света на селен» . Популярная наука . 10 (1): 116.
- ^ Левинштейн, М.Э.; Симин Г.С. (1 декабря 1992 г.). Самый ранний полупроводниковый прибор . Знакомство с полупроводниками. стр. 77–79. ISBN 978-981-02-3516-1 .
- ^ Уинстон, Брайан (29 мая 1998 г.). Медиа-технологии и общество: история: от телеграфа к Интернету . Психология Пресс. п. 89. ИСБН 978-0-415-14229-8 .
- ^ Моррис, Питер Робин (1990). История мировой полупроводниковой промышленности . п. 18. ISBN 978-0-86341-227-1 .
- ^ Бергманн, Людвиг (1931). «О новом фотоэлементе с селеновым переходом». Физический журнал . 32 :286-288.
- ^ Уэйткинс, Греция; Беарс, А.Е.; Шатт, Р. (1942). «Промышленное использование селена и теллура». Промышленная и инженерная химия . 34 (8): 899–910. дои : 10.1021/ie50392a002 .
- ^ Пинсент, Джейн (1954). «Необходимость селенита и молибдата в образовании формиатдегидрогеназы представителями группы бактерий Coli-aerogenes» . Биохим. Дж . 57 (1): 10–16. дои : 10.1042/bj0570010 . ПМЦ 1269698 . ПМИД 13159942 .
- ^ Штадтман, Тресса К. (2002). «Некоторые функции незаменимого микроэлемента селена». Микроэлементы у человека и животных 10 . Том. 10. С. 831–836. дои : 10.1007/0-306-47466-2_267 . ISBN 978-0-306-46378-5 .
- ^ Шварц, Клаус; Фольц, Кэлвин М. (1957). «Селен как неотъемлемая часть фактора 3 против диетической некротической дегенерации печени». Журнал Американского химического общества . 79 (12): 3292–3293. дои : 10.1021/ja01569a087 .
- ^ Олдфилд, Джеймс Э. (2006). «Селен: историческая перспектива». Селен . стр. 1–6. дои : 10.1007/0-387-33827-6_1 . ISBN 978-0-387-33826-2 .
- ^ Хэтфилд, ДЛ; Гладышев В.Н. (2002). «Как селен изменил наше понимание генетического кода» . Молекулярная и клеточная биология . 22 (11): 3565–3576. дои : 10.1128/MCB.22.11.3565-3576.2002 . ПМЦ 133838 . ПМИД 11997494 .
- ^ «Родной селен» . Вебминералы . Проверено 6 июня 2009 г.
- ^ Jump up to: а б Кабата-Пендиас, А. (1998). «Геохимия селена». Журнал экологической патологии, токсикологии и онкологии . 17 (3–4): 173–177. ПМИД 9726787 .
- ^ Jump up to: а б Фордайс, Фиона (2007). «Геохимия селена и здоровье» (PDF) . Амбио: журнал о человеческой среде . 36 (1): 94–97. doi : 10.1579/0044-7447(2007)36[94:SGAH]2.0.CO;2 . ПМИД 17408199 . S2CID 18925825 .
- ^ Вессйоханн, Людгер А.; Шнайдер, Алекс; Аббас, Мухаммед; Брандт, Вольфганг (2007). «Селен в химии и биохимии по сравнению с серой». Биологическая химия . 388 (10): 997–1006. дои : 10.1515/BC.2007.138 . ПМИД 17937613 . S2CID 34918691 .
- ^ Бирринджер, Марк; Пилава, Сандра; Флоэ, Леопольд (2002). «Тенденции в биохимии селена». Отчеты о натуральных продуктах . 19 (6): 693–718. дои : 10.1039/B205802M . ПМИД 12521265 .
- ^ Амуру, Дэвид; Лисс, Питер С.; Тессье, Эммануэль; и др. (2001). «Роль океанов как биогенных источников селена». Письма о Земле и планетологии . 189 (3–4): 277–283. Бибкод : 2001E&PSL.189..277A . дои : 10.1016/S0012-821X(01)00370-3 .
- ^ Хауг, Анна; Грэм, Робин Д.; Кристоферсен, Олав А.; Лайонс, Грэм Х. (2007). «Как эффективно использовать скудные мировые ресурсы селена для повышения концентрации селена в продуктах питания» . Микробная экология в здоровье и болезнях . 19 (4): 209–228. дои : 10.1080/08910600701698986 . ПМК 2556185 . ПМИД 18833333 .
- ^ Риувертс, Джон (2015). Элементы загрязнения окружающей среды . Лондон и Нью-Йорк: Earthscan Routledge. п. 262. ИСБН 978-0-415-85919-6 . OCLC 886492996 .
- ^ «Заявление общественного здравоохранения: селен» (PDF) . Агентство по регистрации токсичных веществ и заболеваний . Проверено 5 января 2009 г.
- ^ «Заявление общественного здравоохранения: селен – производство, импорт/экспорт, использование и утилизация» (PDF) . Агентство по регистрации токсичных веществ и заболеваний . Проверено 5 января 2009 г.
- ^ «Химия: Таблица Менделеева: селен: ключевая информация» . веб-элементы . Проверено 6 января 2009 г.
- ^ Бартос, П.Дж. (2002). «Медь SX-EW и технологический цикл». Ресурсная политика . 28 (3–4): 85–94. Бибкод : 2002РеПол..28...85Б . дои : 10.1016/S0301-4207(03)00025-4 .
- ^ Jump up to: а б Наумов, А.В. (2010). «Селен и теллур: состояние рынков, кризис и его последствия». Металлург . 54 (3–4): 197–200. дои : 10.1007/s11015-010-9280-7 . S2CID 137066827 .
- ^ Хоффманн, Джеймс Э. (1989). «Извлечение селена и теллура из шламов медеперерабатывающих заводов». ДЖОМ . 41 (7): 33–38. Бибкод : 1989JOM....41g..33H . дои : 10.1007/BF03220269 . S2CID 138253358 .
- ^ Хюваринен, Олли; Линдроос, Лео; Юллё, Эркки (1989). «Извлечение селена из шламов медезаводов». ДЖОМ . 41 (7): 42–43. Бибкод : 1989JOM....41g..42H . дои : 10.1007/BF03220271 . S2CID 138555797 .
- ^ Jump up to: а б с «Селен и теллур: статистика и информация» . Геологическая служба США . Проверено 30 мая 2012 г.
- ^ Сунь, Ян; Тиан, Сике; Он, Бинбин; и др. (2011). «Исследование механизма восстановления диоксида селена и его влияния на микроструктуру электроосаждения марганца». Электрохимика Акта . 56 (24): 8305–8310. дои : 10.1016/j.electacta.2011.06.111 .
- ^ Бернд Э. Лангнер (2005), «Селен и соединения селена», Энциклопедия промышленной химии Ульмана , Wiley-VCH, Вайнхайм. два : 10.1002/14356007.a23_525 .
- ^ Дэвис, Джозеф Р. (2001). Медь и медные сплавы . АСМ Межд. п. 91. ИСБН 978-0-87170-726-0 .
- ^ Исаков, Эдмунд (31 октября 2008 г.). Режимы резания для токарной обработки стали . Промышленная пресса. п. 67. ИСБН 978-0-8311-3314-6 .
- ^ Гольдштейн, Я. Э.; Муштакова, Т.Л.; Комиссарова Т.А. (1979). «Влияние селена на структуру и свойства конструкционной стали». Металловедение и термическая обработка . 21 (10): 741–746. Бибкод : 1979МСТ...21..741Г . дои : 10.1007/BF00708374 . S2CID 135853965 .
- ^ Дэвис, Джозеф Р. (2001). Медь и медные сплавы . АСМ Интернешнл . п. 278. ИСБН 978-0-87170-726-0 .
- ^ Эфтехари, Али (2017). «Рост литий-селеновых батарей». Устойчивая энергетика и топливо . 1 : 14–29. дои : 10.1039/C6SE00094K .
- ^ Адамс, Уильям Гриллс; Дэй, Ричард Эванс. «Действие света на селен». Философские труды Лондонского королевского общества . 167 : 313–349.
- ^ Накада, Токио; Куниока, Акио (1 июля 1985 г.). «Поликристаллические тонкопленочные солнечные элементы TiO 2 /Se». Японский журнал прикладной физики . 24 (7А): Л536. Бибкод : 1985JaJAP..24L.536N . дои : 10.1143/JJAP.24.L536 . S2CID 118838432 .
- ^ Тодоров, Теодор К.; Сингх, Саураб; Бишоп, Дуглас М.; Гунаван, Оки; Ли, Юн Сог; Гершон, Талия С.; Брю, Кевин В.; Антунес, Присцилла Д.; Хейт, Ричард (25 сентября 2017 г.). «Ультратонкие солнечные элементы с широкой запрещенной зоной и повышенной эффективностью из старейшего в мире фотоэлектрического материала» . Природные коммуникации . 8 (1): 682. Бибкод : 2017NatCo...8..682T . дои : 10.1038/s41467-017-00582-9 . ПМК 5613033 . ПМИД 28947765 .
- ^ Янгман, Томас Х.; Нильсен, Расмус; Кроветто, Андреа; Сегер, Брайан; Хансен, Оле; Чоркендорф, Иб; Весборг, Питер К.К. (июль 2021 г.). «Полупрозрачные селеновые солнечные элементы как верхний элемент для тандемной фотогальваники». Солнечная РРЛ . 5 (7). дои : 10.1002/solr.202100111 . S2CID 235575161 .
- ^ Нильсен, Расмус; Кроветто, Андреа; Ассар, Алиреза; Хансен, Оле; Чоркендорф, Иб; Весборг, Питер К.К. (12 марта 2024 г.). «Монолитные тандемные селено-кремниевые солнечные элементы». PRX Energy . 3 (1): 013013. arXiv : 2307.05996 . Бибкод : 2024PRXE....3a3013N . дои : 10.1103/PRXEnergy.3.013013 .
- ^ Нильсен, Расмус; Янгман, Томас Х.; Мустафа, Хадил; Левченко, Сергей; Хемпель, Ханнес; Кроветто, Андреа; Олсен, Томас; Хансен, Оле; Чоркендорф, Иб; Анолд, Томас; Весборг, Питер К.К. (2022). «Происхождение фотоэлектрических потерь в селеновых солнечных элементах с напряжением холостого хода, приближающимся к 1 В». Журнал химии материалов А. 10 (45): 24199–24207. дои : 10.1039/D2TA07729A . S2CID 253315416 .
- ^ Нильсен, Расмус; Хеммингсен, Тобиас Х.; Бончик, Тобиас Г.; Хансен, Оле; Чоркендорф, Иб; Весборг, Питер К.К. (11 сентября 2023 г.). «Лазерный отжиг и твердофазная эпитаксия селеновых тонкопленочных солнечных элементов». ACS Прикладные энергетические материалы . 6 (17): 8849–8856. arXiv : 2306.11311 . дои : 10.1021/acsaem.3c01464 . S2CID 259203956 .
- ^ Хуан, Хэюань; Аббасзаде, Шива (2020). «Последние разработки детекторов рентгеновского излучения на основе аморфного селена: обзор» . Журнал датчиков IEEE . 20 (4): 1694–1704. Бибкод : 2020ISenJ..20.1694H . дои : 10.1109/JSEN.2019.2950319 . S2CID 208833373 .
- ^ Касап, Сафа; Фрей, Джоэл Б.; Белев, Георгий; Тузиньян, Оливье; Мани, Хабиб; Лаперьер, Люк; Резник Алла; Роулендс, Джон А. (2009). «Аморфный селен и его сплавы от ранней ксерорадиографии до детекторов рентгеновских изображений высокого разрешения и сверхчувствительных трубок для визуализации». Физический статус Solidi B. 246 (8): 1794–1805. Бибкод : 2009ПССБР.246.1794К . дои : 10.1002/pssb.200982007 . S2CID 122848842 .
- ^ Спрингетт, Бельгия (1988). «Применение селен-теллуровых фотопроводников в процессах ксерографического копирования и печати». Фосфор и сера и родственные им элементы . 38 (3–4): 341–350. дои : 10.1080/03086648808079729 .
- ^ Уильямс, Роб (2006). Архитектура компьютерных систем: сетевой подход . Прентис Холл. стр. 547–548. ISBN 978-0-321-34079-5 .
- ^ Дильс, Жан-Клод; Арисян, Ладан (2011). «Лазерный принтер» . Лазеры . Вайли-ВЧ. стр. 81–83. ISBN 978-3-527-64005-8 .
- ^ Меллер, Грегор и Грассер, Тибор (2009). Органическая электроника . Спрингер. стр. 3–5. ISBN 978-3-642-04537-0 .
- ^ Нормил, Деннис (2000). «Рождение блюза» . Популярная наука . п. 57.
- ^ Касап, Сафа; Фрей, Джоэл Б.; Белев, Георгий; и др. (2009). «Аморфный селен и его сплавы от ранней ксерорадиографии до детекторов рентгеновских изображений высокого разрешения и сверхчувствительных трубок для визуализации». Физический статус Solidi B. 246 (8): 1794–1805. Бибкод : 2009ПССБР.246.1794К . дои : 10.1002/pssb.200982007 . S2CID 122848842 .
- ^ Свелто, Орацио (1998). Принципы ЛАЗЕРОВ, четвертое изд . Пленум. п. 457. ИСБН 978-0-306-45748-7 .
- ^ Хейворд, Питер; Карри, Дин. «Рентгенография сварных швов с использованием селена 75, Ir 192 и рентгеновских лучей» (PDF) .
- ^ Сингх, Фатех В.; Вирт, Томас (2019). «Селеновые реагенты как катализаторы» . Катализная наука и технология . 9 (5): 1073–1091. дои : 10.1039/C8CY02274G . S2CID 104468775 .
- ^ Хай-Фу, Ф.; Вульфсон, ММ; Цзя-Син, Ю. (1993). «Новые методы применения данных многоволнового аномального рассеяния». Труды Королевского общества A: Математические, физические и технические науки . 442 (1914): 13–32. Бибкод : 1993RSPSA.442...13H . дои : 10.1098/rspa.1993.0087 . S2CID 122722520 .
- ^ Маклин, Мэрион Э. (1937). «Проект для студентов-химиков: Цветное тонирование фотоотпечатков». Журнал химического образования . 14 (1): 31. Бибкод : 1937ЖЧЭд..14...31М . дои : 10.1021/ed014p31 .
- ^ Пенишон, Сильви (1999). «Различия в тональности изображения, создаваемые разными протоколами тонирования для матовых коллодионных фотографий». Журнал Американского института охраны природы . 38 (2): 124–143. дои : 10.2307/3180042 . JSTOR 3180042 .
- ^ Маккензи, Джой (2003). Знакомство с основами черно-белой фотографии . Дельмар. п. 176 . ISBN 978-1-4018-1556-1 .
- ^ «Что такое перхоть?» (PDF) . Виши Великобритания . Проверено 3 октября 2023 г.
- ^ Лемли, А. Деннис (1 сентября 2004 г.). «Загрязнение водного селена является глобальной проблемой экологической безопасности» . Экотоксикология и экологическая безопасность . 59 (1): 44–56. Бибкод : 2004ЭкоЭС..59...44Л . дои : 10.1016/S0147-6513(03)00095-2 . ISSN 0147-6513 . ПМИД 15261722 .
- ^ Эструх, Рамон; Саканелла, Эмилио; Рос, Эмилио (4 января 2021 г.). «Должны ли мы все стать песко-вегетарианцами?» . Европейский кардиологический журнал . 42 (12): 1144–1146. дои : 10.1093/eurheartj/ehaa1088 . ISSN 0195-668X . ПМИД 33393612 .
- ^ Гриббл, Мэтью; Карими, Роксана; Файнголд, Бет; Ниланд, Дженнифер; О'Хара, Тодд; Гладышев Михаил; Чен, Селия (8 сентября 2015 г.). «Ртуть, селен и рыбий жир в морских пищевых цепях и последствия для здоровья человека» . Журнал Морской биологической ассоциации Соединенного Королевства . 1 (96): 43–59. дои : 10.1017/S0025315415001356 . ПМК 4720108 . ПМИД 26834292 .
в более высоких дозах селен может быть токсичным для ряда животных, включая человека.
- ^ Лемли, Д. (2004). «Загрязнение водного селена является глобальной проблемой экологической безопасности» . Экотоксикология и экологическая безопасность . 59 (1): 44–56. Бибкод : 2004ЭкоЭС..59...44Л . дои : 10.1016/S0147-6513(03)00095-2 . ПМИД 15261722 .
- ^ Олендорф, HM (2003). Экотоксикология селена . Справочник по экотоксикологии. Бока-Ратон: Издательство Льюиса. стр. 466–491. ISBN 978-1-56670-546-2 .
- ^ Лемли, AD (1997). «Индекс тератогенной деформации для оценки воздействия селена на популяции рыб» . Экотоксикология и экологическая безопасность . 37 (3): 259–266. Бибкод : 1997ЭкоЭС..37..259Л . дои : 10.1006/eesa.1997.1554 . ПМИД 9378093 .
- ^ Пенглас, С.; Хамре, К.; Эллингсен, С. (2014). «Селен и ртуть оказывают синергетическое негативное воздействие на воспроизводство рыб». Водная токсикология . 149 : 16–24. Бибкод : 2014AqTox.149...16P . дои : 10.1016/j.aquatox.2014.01.020 . ПМИД 24555955 .
- ^ Хайнц, Г.Х.; Хоффман, диджей (1998). «Взаимодействие хлорида метилртути и селенометионина на здоровье и воспроизводство кряквы». Экологическая токсикология и химия . 17 (2): 139–145. дои : 10.1002/etc.5620170202 . S2CID 95466655 .
- ^ Лемли, Деннис (1998). Оценка содержания селена в водных экосистемах: руководство по оценке опасностей и критериям качества воды . Спрингер. ISBN 0-387-95346-9 .
- ^ Гамильтон, Стивен Дж. (29 июня 2004 г.). «Обзор токсичности селена в водной пищевой цепи» . Наука об общей окружающей среде . 326 (1): 1–31. Бибкод : 2004ScTEn.326....1H . doi : 10.1016/j.scitotenv.2004.01.019 . ISSN 0048-9697 . ПМИД 15142762 .
- ^ Атроши, Фаик (28 мая 2014 г.). Фармакология и диетическое вмешательство при лечении заболеваний . Совет директоров – Книги по запросу. ISBN 978-953-51-1383-6 .
- ^ Фриман, Джон Л.; Линдблом, «Грозовый рассвет»; Куинн, Колин Ф.; Факра, Сирин; Маркус, Мэтью А.; Пилон-Смитс, Элизабет АХ (2007). «Накопление селена защищает растения от травоядных прямокрылых посредством токсичности и сдерживания» . Новый фитолог . 175 (3): 490–500. дои : 10.1111/j.1469-8137.2007.02119.x . ISSN 0028-646X . ПМИД 17635224 . S2CID 2330947 .
- ^ Концентрации селена в листовом материале Astragalus Oxyphysus (дьяволовник диабло) и Atriplex Lentiformis (перепелиный куст) во внутренних прибрежных хребтах и западной части долины Сан-Хоакин, Калифорния (Отчет). Геологическая служба США. 1986. Отчет об исследованиях водных ресурсов 86-4066.
- ^ Общая ссылка на это: Шредер, ХА; Мороз, Д.В.; Баласса, Джей-Джей (1970). «Незаменимые микроэлементы для человека: селен». Журнал хронических болезней . 23 (4): 227–243. дои : 10.1016/0021-9681(70)90003-2 . ОСТИ 6424964 . ПМИД 4926392 .
- ^ Институт Лайнуса Полинга при Университете штата Орегон lpi.oregonstate.edu
- ^ Пакдель, Фарзад; Газави, Рогайе; Хейдари, Рогайе; Незамабади, Афины; Парвизи, Марьям; Хаджи Сафар Али Мемар, Махса; Гаребаги, Реза; Хейдари, Фатема (2019). «Влияние селена на заболевания щитовидной железы: наукометрический анализ» . Иранский журнал общественного здравоохранения . 48 (3): 410–420. ISSN 2251-6085 . ПМК 6570790 . ПМИД 31223567 .
- ^ «Селен» . Институт Лайнуса Полинга при Университете штата Орегон . Проверено 5 января 2009 г.
- ^ Мазокопакис, Э.Э.; Пападакис, Дж. А.; Пападоманолаки, МГ; и др. (2007). «Влияние 12-месячного лечения L-селенометионином на уровни анти-ТПО в сыворотке крови у пациентов с тиреоидитом Хашимото». Щитовидная железа . 17 (7): 609–612. дои : 10.1089/thy.2007.0040 . ПМИД 17696828 .
- ^ Ралстон, Невада; Ралстон, Чехия; Блэквелл, JL III; Раймонд, ЖЖ (2008). «Диетический и тканевой селен в связи с токсичностью метилртути» (PDF) . Нейротоксикология . 29 (5): 802–811. Бибкод : 2008NeuTx..29..802R . CiteSeerX 10.1.1.549.3878 . дои : 10.1016/j.neuro.2008.07.007 . ПМИД 18761370 . Архивировано из оригинала (PDF) 24 июля 2012 г. Проверено 28 сентября 2012 г.
- ^ Пенглас, С.; Хамре, К.; Эллингсен, С. (2014). «Селен предотвращает подавление генов антиоксидантных селенопротеинов метилртутью». Свободнорадикальная биология и медицина . 75 : 95–104. doi : 10.1016/j.freeradbiomed.2014.07.019 . HDL : 1956/8708 . ПМИД 25064324 .
- ^ Усуки, Ф.; Ямасита, А.; Фудзимура, М. (2011). «Посттранскрипционные дефекты антиоксидантных селеноферментов вызывают окислительный стресс при воздействии метилртути» . Журнал биологической химии . 286 (8): 6641–6649. дои : 10.1074/jbc.M110.168872 . ПМК 3057802 . ПМИД 21106535 .
- ^ Охи, Г.; Секи, Х.; Маэда, Х.; Ягю, Х. (1975). «Защитный эффект селенита от токсичности метилртути: наблюдения относительно факторов времени, дозы и пути развития ослабления селена» . Промышленное здоровье . 13 (3): 93–99. дои : 10.2486/indhealth.13.93 .
- ^ Ралстон, NVC; Раймонд, ЖЖ (2010). «Защитное действие диетического селена против токсичности метилртути». Токсикология . 278 (1): 112–123. Бибкод : 2010Toxgy.278..112R . дои : 10.1016/j.tox.2010.06.004 . ПМИД 20561558 .
- ^ Карвалью, ХМЛ; Чу, Хашеми С.И.; Хашеми, Дж.; и др. (2008). «Ингибирование тиоредоксиновой системы человека: молекулярный механизм ртутной токсичности» . Журнал биологической химии . 283 (18): 11913–11923. дои : 10.1074/jbc.M710133200 . ПМИД 18321861 .
- ^ Кен Тухата, Такеши Ябу и Юмико Ямасита, «Высокая антиоксидантная активность нового селенсодержащего имидазольного соединения «селенонеина » Мичиаки Ямасита, Синтаро Имамура, доктор медицинских наук Анвар Хоссейн , , The FASEB Journal , vol. 26 нет. 1, приложение 969.13, апрель 2012 г.
- ^ Ямасита, Ю.; Ябу, Т.; Ямасита, М. (2010). «Открытие сильного антиоксиданта селенонеина в тунце и окислительно-восстановительного метаболизма селена» . Всемирный журнал биологической химии . 1 (5): 144–150. дои : 10.4331/wjbc.v1.i5.144 . ПМК 3083957 . ПМИД 21540999 .
- ^ Зейн Дэвис, Т. (27 марта 2008 г.). «Селен в растениях» (PDF) . п. 8 . Проверено 5 декабря 2008 г.
- ^ Jump up to: а б Гладышев Вадим Н.; Хэтфилд, Дольф Л. (1999). «Селеноцистеинсодержащие белки млекопитающих» . Журнал биомедицинской науки . 6 (3): 151–160. дои : 10.1007/BF02255899 . ПМИД 10343164 .
- ^ Штадтман, ТК (1996). «Селеноцистеин». Ежегодный обзор биохимии . 65 (1): 83–100. дои : 10.1146/annurev.bi.65.070196.000503 . ПМИД 8811175 .
- ^ Лобанов Алексей Владимирович; Фоменко Дмитрий Евгеньевич; Чжан, Ян; и др. (2007). «Эволюционная динамика эукариотических селенопротеомов: большие селенопротеомы могут ассоциироваться с водной жизнью, а маленькие - с наземной жизнью» . Геномная биология . 8 (9): 198 рандов. дои : 10.1186/gb-2007-8-9-r198 . ПМК 2375036 . ПМИД 17880704 .
- ^ Вентури, Себастьяно; Вентури, Маттиа (2007). «Эволюция диетической антиоксидантной защиты» . Европейский эпимаркер . 11 (3): 1–11.
- ^ Кастеллано, Серджи; Новоселов Сергей Владимирович; Крюков Григорий Васильевич; и др. (2004). «Пересмотр эволюции эукариотических селенопротеинов: новое семейство немлекопитающих с разбросанным филогенетическим распределением» . Отчеты ЭМБО . 5 (1): 71–7. дои : 10.1038/sj.embor.7400036 . ПМЦ 1298953 . ПМИД 14710190 .
- ^ Kryukov, Gregory V.; Gladyshev, Vadim N. (2004). "The prokaryotic selenoproteome" . EMBO Reports . 5 (5): 538–43. doi : 10.1038/sj.embor.7400126 . PMC 1299047 . PMID 15105824 .
- ^ Уилтинг, Р.; Шерлинг, С.; Перссон, Британская Колумбия; Бёк, А. (1997). «Синтез селенопротеина у архей: идентификация элемента мРНК Methanococcus jannaschii , вероятно, управляющего вставкой селеноцистеина». Журнал молекулярной биологии . 266 (4): 637–41. дои : 10.1006/jmbi.1996.0812 . ПМИД 9102456 .
- ^ Чжан, Ян; Фоменко Дмитрий Евгеньевич; Гладышев, Вадим Н. (2005). «Микробный селенопротеом Саргассова моря» . Геномная биология . 6 (4): С37. дои : 10.1186/gb-2005-6-4-r37 . ПМЦ 1088965 . ПМИД 15833124 .
- ^ Jump up to: а б Разаги, Али; Пуребрагим, Мансур; Сархан, Дифаф; Бьёрнштедт, Микаэль (01 сентября 2021 г.). «Селен стимулирует противоопухолевый иммунитет: перспективы будущих исследований» . Европейский журнал рака . 155 : 256–267. дои : 10.1016/j.ejca.2021.07.013 . ISSN 0959-8049 . ПМИД 34392068 .
- ^ «Информационный бюллетень о пищевых добавках: селен» . Национальные институты здравоохранения; Офис пищевых добавок . Проверено 5 января 2009 г.
- ^ Группа по диетическим антиоксидантам и родственным соединениям, подкомитеты по верхним референтным уровням питательных веществ, а также интерпретации и использованию DRI, Постоянный комитет по научной оценке эталонного потребления с пищей, Совет по продовольствию и питанию, Институт медицины (15 августа 2000 г.). Рекомендуемая диетическая норма витамина С, витамина Е, селена и каротиноидов . Институт медицины. стр. 314–315. дои : 10.17226/9810 . ISBN 978-0-309-06949-6 . ПМИД 25077263 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Ян, Г.; Чжоу, Р. (1994). «Дальнейшие наблюдения за максимально безопасным потреблением селена с пищей человеком в селеноносном районе Китая». Журнал микроэлементов и электролитов в здоровье и болезнях . 8 (3–4): 159–165. ПМИД 7599506 .
- ^ Ян, Гуан-Ци; Ся, И-Мин (1995). «Исследования пищевых потребностей человека и безопасного диапазона потребления селена с пищей в Китае и их применение для профилактики связанных с ними эндемических заболеваний». Биомедицинские и экологические науки . 8 (3): 187–201. ПМИД 8561918 .
- ^ «Заявление об общественном здравоохранении: последствия для здоровья» (PDF) . Агентство по регистрации токсичных веществ и заболеваний . Проверено 5 января 2009 г.
- ^ Уилбер, CG (1980). «Токсикология селена». Клиническая токсикология . 17 (2): 171–230. дои : 10.3109/15563658008985076 . ПМИД 6998645 .
- ^ Олсон, О.Э. (1986). «Токсичность селена у животных с акцентом на человека» . Международный журнал токсикологии . 5 : 45–70. дои : 10.3109/10915818609140736 . S2CID 74619246 .
- ^ «Уровень селена в поло-пони в 20 раз выше обычного» . 06.05.2009. Архивировано из оригинала 19 августа 2016 г. Проверено 5 мая 2009 г.
- ^ Jump up to: а б Гамильтон, Стивен Дж.; Буль, Кевин Дж.; Фаербер, Нил Л.; и др. (1990). «Токсичность органического селена в рационе чавычи». Окружающая среда. Токсикол. Хим . 9 (3): 347–358. дои : 10.1002/etc.5620090310 .
- ^ Jump up to: а б Постон, штат Ха; Комбс, Г. Ф. младший; Лейбовиц, Л. (1976). «Взаимоотношения витамина Е и селена в рационе атлантического лосося ( Salmo salar ): валовые, гистологические и биохимические признаки». Журнал питания . 106 (7): 892–904. дои : 10.1093/jn/106.7.892 . ПМИД 932827 .
- ^ Брэйн, П.; Казенс, Р. (1989). «Уравнение для описания реакции на дозу при стимуляции роста при низких дозах». Исследования сорняков . 29 (2): 93–96. Бибкод : 1989WeedR..29...93B . дои : 10.1111/j.1365-3180.1989.tb00845.x .
- ^ «Карманный справочник NIOSH по химическим опасностям – селен» . США: Национальный институт безопасности и гигиены труда . Проверено 21 ноября 2015 г.
- ^ Базелт, Р. (2008). Утилизация токсичных лекарств и химикатов в организме человека (8-е изд.). Фостер-Сити, Калифорния: Биомедицинские публикации. стр. 1416–1420. ISBN 978-0-9626523-5-6 .
- ^ Равалья, Г.; Форти, П.; Майоли, Ф.; и др. (2000). «Влияние статуса микроэлементов на иммунную функцию естественных киллеров у здоровых людей, живущих на свободе в возрасте ≥90 лет» . Американский журнал клинического питания . 71 (2): 590–598. дои : 10.1093/ajcn/71.2.590 . ПМИД 10648276 .
- ^ Редакционная коллегия МедСейф. «Селен» . Обновленные статьи для врачей . Управление по безопасности лекарственных средств и медицинского оборудования Новой Зеландии . Проверено 13 июля 2009 г.
- ^ Ралстон, NVC; Раймонд, ЖЖ (2010). «Защитное действие диетического селена против токсичности метилртути». Токсикология . 278 (1): 112–123. Бибкод : 2010Toxgy.278..112R . дои : 10.1016/j.tox.2010.06.004 . ПМИД 20561558 .
- ^ Манн, Джим; Трусвелл, А. Стюарт (2002). Основы питания человека (2-е изд.). Издательство Оксфордского университета. ISBN 978-0-19-262756-8 .
- ^ Морено-Рейес, Р.; Матье, Ф.; Боэлерт, М.; и др. (2003). «Добавка селена и йода сельским тибетским детям, страдающим остеоартропатией Кашина-Бека» . Американский журнал клинического питания . 78 (1): 137–144. дои : 10.1093/ajcn/78.1.137 . ПМИД 12816783 .
- ^ Качуи, Р.; Мойни, М.; Суори, М. (2013). «Влияние пищевых добавок органического и неорганического селена на статус Se, Cu, Fe и Zn в сыворотке крови на поздних сроках беременности у мергхозских коз и их козлят». Исследования мелких жвачных животных . 110 (1): 20–27. doi : 10.1016/j.smallrumres.2012.08.010 .
- ^ Национальный исследовательский совет, Подкомитет по питанию овец (1985). Потребность овец в питательных веществах . 6-е изд., National Academy Press, Вашингтон, ISBN 0309035961 .
- ^ Jump up to: а б Национальный исследовательский совет, Комитет по потребностям мелких жвачных животных в питательных веществах (2007). Потребность мелких жвачных животных в питательных веществах . Издательство национальных академий, Вашингтон, ISBN 0-309-10213-8 .
- ^ Куп, IE; Блейкли, Р.Л. (1949). «Метаболизм и токсичность цианидов и цианогенных гликозидов у овец». Новозеландский журнал науки и технологий . 30 : 277–291.
- ^ Краус, Р.Дж.; Прохаска, младший; Гантер, HE (1980). «Окисленные формы глутатионпероксидазы эритроцитов овец. Цианидное ингибирование 4-глутатион:4-селенофермента». Biochimica et Biophysical Acta (BBA) - Энзимология . 615 (1): 19–26. дои : 10.1016/0005-2744(80)90004-2 . ПМИД 7426660 .
- ^ Кан, CM (редактор) (2005). Ветеринарное руководство Merck . 9-е изд. Merck & Co., Inc., станция Уайтхаус, ISBN 0911910506 .
- ^ Барклай, Маргарет Н.И.; Макферсон, Аллан; Диксон, Джеймс (1995). «Содержание селена в ряде продуктов питания Великобритании». Журнал пищевого состава и анализа . 8 (4): 307–318. дои : 10.1006/jfca.1995.1025 .
- ^ «Информационный бюллетень по селену» . США: Управление пищевых добавок, Национальные институты здравоохранения . Включает список продуктов, богатых селеном.
- ^ «FDA выпустило окончательное правило о добавлении селена в список необходимых питательных веществ для детского питания» . Управление по контролю за продуктами и лекарствами. Архивировано из оригинала 14 ноября 2017 года . Проверено 10 сентября 2015 г.
- ^ Ростами, Рахим; Нуруз-Заде, Сармад; Мохаммади, Афшин; Халхали, Хамид Реза; Папоротники, Гордон; Нуруз-Заде, Джафар (31 октября 2020 г.). «Статус селена в сыворотке и его взаимосвязь с сывороточными биомаркерами функции щитовидной железы и антиоксидантной защиты при тиреоидите Хашимото» . Антиоксиданты . 9 (11): Е1070. дои : 10.3390/antiox9111070 . ISSN 2076-3921 . ПМЦ 7692168 . ПМИД 33142736 .
- ^ Вандерпас, Дж.Б.; Контемпре, Б.; Дуале, Нидерланды; Декс, Х.; Бебе, Н.; Лонгомбе, АО; Тилли, CH; Диплок, АТ; Дюмон, JE (февраль 1993 г.). «Дефицит селена смягчает гипотироксинемию у людей с дефицитом йода» . Американский журнал клинического питания . 57 (2 доп.): 271S–275S. дои : 10.1093/ajcn/57.2.271S . ISSN 0002-9165 . ПМИД 8427203 .
Внешние ссылки
[ редактировать ]- Селен в Периодической таблице видео (Ноттингемский университет)
- Страница Национального института здравоохранения о селене
- Анализ. Архивировано 26 февраля 2012 г. в Wayback Machine.
- ATSDR – Токсикологический профиль: Селен
- CDC - Карманный справочник NIOSH по химическим опасностям
- Сайт элементов Питера ван дер Крогта




