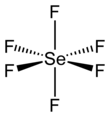
Гексафторид селена
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Гексафторид селена | |||
| Другие имена Фторид селена(VI), Фторид селена | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.149.506 | ||
ПабХим CID | |||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| СеФ 6 | |||
| Молярная масса | 192.9534 g/mol | ||
| Появление | бесцветный газ | ||
| Плотность | 0,007887 г/см 3 [1] | ||
| Температура плавления | -39 ° C (-38 ° F; 234 К) | ||
| Точка кипения | -34,5 ° C (-30,1 ° F; 238,7 К) возвышенное | ||
| нерастворимый | |||
| Давление пара | >1 атм (20°C) [2] | ||
| −51.0·10 −6 см 3 /моль | |||
Показатель преломления ( n D ) | 1.895 | ||
| Структура | |||
| Орторомбический , oP28 | |||
| Пнма, нет. 62 | |||
| октаэдрический ( о ч ) | |||
| 0 | |||
| Термохимия | |||
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | -1030 кДж/моль [3] | ||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | токсичный, коррозионный | ||
| NFPA 704 (огненный алмаз) | |||
| Летальная доза или концентрация (LD, LC): | |||
LC Lo ( самый низкий из опубликованных ) | 10 частей на миллион (крыса, 1 час) 10 частей на миллион (мышь, 1 час) 10 частей на миллион (морская свинка, 1 час) [4] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
МЕХ (Допускается) | TWA 0,05 частей на миллион (0,4 мг/м 3 ) [2] | ||
РЕЛ (рекомендуется) | СВВ 0,05 частей на миллион [2] | ||
IDLH (Непосредственная опасность) | 2 частей на миллион [2] | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
селена – неорганическое соединение формулы 6 SeF Гексафторид . Это очень токсичный бесцветный газ, имеющий «отталкивающий» запах. [5] Он не получил широкого распространения и не имеет коммерческого применения. [6]
Структура, получение и реакции
[ редактировать ]SeF 6 имеет октаэдрическую молекулярную геометрию с длиной связи Se-F 168,8 мкм . С точки зрения связи он гипервалентен .
SeF 6 можно получить из элементов. [7] Он также образуется при реакции трифторида брома (BrF 3 ) с диоксидом селена . Неочищенный продукт можно очистить сублимацией.
Относительная реакционная способность гексафторидов S, Se и Te находится в ряду TeF 6 > SeF 6 > SF 6 , причем последний полностью инертен к гидролизу вплоть до высоких температур. SeF 6 также устойчив к гидролизу. [3] Газ можно без изменений пропускать через 10% раствор NaOH или КОН, но он реагирует с газообразным аммиаком при 200 °C. [8]
Безопасность
[ редактировать ]Хотя гексафторид селена довольно инертен и медленно гидролизуется, он токсичен даже в низких концентрациях. [9] особенно при более длительном воздействии. В США стандарты OSHA и ACGIH для воздействия гексафторида селена устанавливают верхний предел в 0,05 частей на миллион в воздухе в среднем за восьмичасовую рабочую смену. Кроме того, гексафторид селена обозначен как химическое вещество IDLH с максимально допустимым пределом воздействия 2 частей на миллион. [10]
Ссылки
[ редактировать ]- ^ Лиде, Д.Р., изд. (2005). Справочник CRC по химии и физике (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5 .
- ^ Jump up to: а б с д Карманный справочник NIOSH по химическим опасностям. «#0551» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Jump up to: а б Виберг, Э.; Холлеман, А.Ф. (2001). Неорганическая химия . Эльзевир. ISBN 0-12-352651-5 .
- ^ «Гексафторид селена» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Материальная безопасность» (PDF) . Проверено 24 июля 2010 г.
- ^ Лангнер, Б.Е. «Селен и соединения селена». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a23_525 . ISBN 978-3527306732 .
- ^ Йост, Д.М.; Саймонс, Дж. Х. (1939). «Гексафториды серы, селена и теллура». Неорганические синтезы . Том. 1. С. 121–122. дои : 10.1002/9780470132326.ch44 . ISBN 9780470132326 .
- ^ Кребс, Б.; Бонманн, С.; Эйденшинк, И. (1994). «Селен-неорганическая химия». В Кинге, РБ (ред.). Энциклопедия неорганической химии . Джон Уайли и сыновья. ISBN 0-471-93620-0 .
- ^ «Руководство по медицинскому применению гексафторида селена (SeF 6 )» . CDC АТСДР. Архивировано из оригинала 28 мая 2010 года . Проверено 24 июля 2010 г.
- ^ Документация по концентрациям, непосредственно опасным для жизни или здоровья (IDLH).