Фторбензол
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК Фторбензол | |||
| Другие имена Фенилфторид Монофторбензол | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| 1236623 | |||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.006.657 | ||
| Номер ЕС |
| ||
| 49856 | |||
| КЕГГ | |||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
| Число | 2387 | ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 6 Ч 5 Ж | |||
| Молярная масса | 96.103 | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 1,025 г/мл, жидкость | ||
| Температура плавления | -44 ° C (-47 ° F; 229 К) | ||
| Точка кипения | От 84 до 85 ° C (от 183 до 185 ° F; от 357 до 358 К) | ||
| низкий | |||
| -58.4·10 −6 см 3 /моль | |||
Показатель преломления ( n D ) | 1.46553 | ||
| Структура | |||
| Планарный | |||
| Опасности | |||
| СГС Маркировка : | |||
   | |||
| Предупреждение | |||
| Х225 , Х318 , Х411 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P264 , P280 , P273 , P303+P361+P353 , P305+P351+P338 , P310 , P337+P313 , P370+P378 , P391 , 3+П235 , П501 | |||
| NFPA 704 (огненный алмаз) | |||
| Родственные соединения | |||
Родственные галогенбензолы | хлорбензол Бромбензол Йодобензол | ||
Родственные соединения | Бензол 1,2-дифторбензол | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Фторбензол представляет собой арилфторид и простейший из фторбензолов с формулой C 6 H 5 F, часто сокращенно Ph F. Бесцветная жидкость является предшественником многих фторфенильных соединений.
Подготовка
[ редактировать ]Впервые о PhF сообщил в 1886 году О. Уоллах из Боннского университета , который приготовил соединение в два этапа. Хлорид фенилдиазония сначала превратили в триазен с помощью пиперидина:
- [PhN 2 ]Cl + 2 (CH 2 ) 5 NH → PhN=NN(CH 2 ) 5 + [(CH 2 ) 5 NH 2 ]Cl
Затем триазин расщепляли плавиковой кислотой :
- PhN=NN(CH 2 ) 5 + 2 HF → PhF + N 2 + [(CH 2 ) 5 NH 2 ]F
Историческая справка: в эпоху Уоллаха элемент фтор обозначался буквой «Fl». Таким образом, его процедура имеет подзаголовок «Фторбензол, C 6 H 5 Fl». [1]
масштабах PhF получают термическим разложением тетрафторбората бензолдиазония В лабораторных :
- ФН 2 ДФ 4 → ФН + ДФ 3 + Н 2
Согласно методике, твердый [PhN 2 ]BF 4 нагревается пламенем для инициирования экзотермической реакции , в результате которой также образуется трифторид бора и газообразный азот. Продукты PhF и BF 3 легко разделяются из-за разной температуры кипения . [2]
Технический синтез осуществляется реакцией циклопентадиена с дифторкарбеном . Первоначально образовавшийся циклопропан подвергается расширению кольца и последующему отщеплению фторида водорода .
Реакции
[ редактировать ]PhF ведет себя иначе, чем другие производные галогенбензола, из-за пи-донорных свойств фторида. Например, пара-положение более активируется по отношению к электрофилам, чем бензол. По этой причине его можно преобразовать в 1-бром-4-фторбензол с относительно высокой эффективностью. [3]
Свойства растворителя
[ редактировать ]PhF является полезным растворителем для высокореактивных веществ. Его температура плавления при -44 °C ниже, чем у бензола. Напротив, температуры кипения PhF и бензола очень похожи и различаются всего на 4 °C. Он значительно более полярен, чем бензол, с диэлектрической проницаемостью 5,42 по сравнению с 2,28 у бензола при 298 К. [4] Фторбензол — относительно инертное соединение, что отражает силу связи C–F.
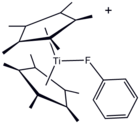
Хотя его обычно считают некоординирующим растворителем, металлокомплекс PhF кристаллизовался. [5]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Уоллах, О. «О методе легкого получения фторорганических соединений» «Анналы химии» Юстуса Либиха, 1886, том 235, стр. 255-271; два : 10.1002/jlac.18862350303
- ^ Наводнение, DT (1933). «Фторбензол». Орг. Синтез . 13:46 . дои : 10.15227/orgsyn.013.0046 . .
- ^ Розенталь, Джоэл; Шустер, Дэвид И. (2003). «Аномальная реакционная способность фторбензола при электрофильном ароматическом замещении и связанные с ним явления». Дж. Хим. Образование . 80 (6): 679. Бибкод : 2003JChEd..80..679R . дои : 10.1021/ed080p679 .
- ^ Таблица диэлектрических проницаемостей чистых жидкостей . Национальное бюро стандартов. 1951.
- ^ Р. Н. Перуц и Т. Браун «Активация связи C – F, опосредованная переходными металлами», Комплексная металлоорганическая химия III, 2007, Том 1, стр. 725–758; два : 10.1016/B0-08-045047-4/00028-5 .