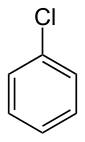
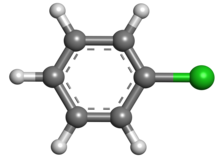
хлорбензол
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК хлорбензол | |||
| Другие имена Фенилхлорид, монохлорбензол [1] | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| 3DMeet | |||
| Сокращения | PhCl | ||
| 605632 | |||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.003.299 | ||
| Номер ЕС |
| ||
| 26704 | |||
| КЕГГ | |||
ПабХим CID | |||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
| Число | 1134 | ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 6 Н 5 Cl | |||
| Молярная масса | 112.56 g/mol | ||
| Появление | бесцветная жидкость | ||
| Запах | миндалевидный [2] | ||
| Плотность | 1,11 г/см 3 , жидкость | ||
| Температура плавления | -45,58 ° C (-50,04 ° F; 227,57 К) | ||
| Точка кипения | 131,70 ° С (269,06 ° F; 404,85 К) | ||
| 0,5 гл −1 в воде при 20 °C | |||
| Растворимость в других растворителях | растворим в большинстве органических растворителей | ||
| Давление пара | 9 мм рт.ст. [2] | ||
| −69.97·10 −6 см 3 /моль | |||
Показатель преломления ( n D ) | 1.52138 | ||
| Вязкость | 0.7232 | ||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | Низкая и умеренная опасность [3] | ||
| СГС Маркировка : | |||
   | |||
| Предупреждение | |||
| Х226 , Х302 , Х305 , Х315 , Х332 , Х411 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P271 , P273 , P280 , P302+P352 , P303+P361+P353 , P304+P312 , P304+P340 , P312 , П332 21 , +П313 , П362 , П370+П378 , П391 , П403+П235 , П501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 29 ° C (84 ° F; 302 К) | ||
| Взрывоопасные пределы | 1.3%-9.6% [2] | ||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза ) | 2290 мг/кг (крыса, перорально) 590 мг/кг (мыши, перорально) [4] | ||
LC Lo ( самый низкий из опубликованных ) | 8000 частей на миллион (кошка, 3 часа) [5] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
ПЭЛ (допустимо) | СВВ 75 частей на миллион (350 мг/м 3 ) [2] | ||
РЕЛ (рекомендуется) | никто [2] | ||
IDLH (Непосредственная опасность) | 1000 частей на миллион [2] | ||
| Родственные соединения | |||
Родственные галогенбензолы | Фторбензол Бромбензол Йодобензол | ||
Родственные соединения | бензол 1,4-дихлорбензол | ||
| Страница дополнительных данных | |||
| Хлорбензол (страница данных) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Хлорбензол (сокращенно PhCl ) представляет собой арилхлорид и простейший из хлорбензолов , состоящий из бензольного кольца, замещенного одним атомом хлора . Его химическая формула C 6 H 5 Cl. Эта бесцветная легковоспламеняющаяся жидкость является распространенным растворителем и широко используемым промежуточным продуктом при производстве других химикатов. [6]
Использование
[ редактировать ]В основном хлорбензол используется в качестве прекурсора для других промежуточных продуктов, таких как нитрофенолы , нитроанизол , хлоранилин и фенилендиамины , которые используются в производстве гербицидов, красителей, химикатов для резины и фармацевтических препаратов. [7]
Он также используется в качестве высококипящего растворителя в промышленных и лабораторных условиях для таких материалов, как масла, воски, смолы и каучук. [7] [8]
Хлорбензол нитруют в больших масштабах с образованием смеси 2-нитрохлорбензола и 4-нитрохлорбензола , которые разделяют и используют в качестве промежуточных продуктов при производстве других химикатов. Эти мононитрохлорбензолы превращаются в родственные 2-нитрофенол , 2-нитроанизол, бис(2-нитрофенил)дисульфид и 2-нитроанилин путем нуклеофильного замещения хлорида соответственно гидроксидом натрия , метоксидом натрия , дисульфидом натрия и аммиаком . Превращения 4-нитропроизводного аналогичны. [9]
Ниша и прежнее использование
[ редактировать ]Хлорбензол когда-то использовался при производстве пестицидов , особенно ДДТ , путем реакции с хлоралем (трихлорацетальдегидом), но это применение сократилось с уменьшением использования ДДТ. В свое время хлорбензол был основным предшественником для производства фенола : [10]
- C 6 H 5 Cl + NaOH → C 6 H 5 OH + NaCl
Реакция известна как процесс Доу , при этом реакция проводится при 350 ° C с использованием конденсированного гидроксида натрия без растворителя. Эксперименты по маркировке показывают, что реакция протекает путем отщепления/присоединения с использованием бензона в качестве промежуточного продукта.
Производство
[ редактировать ]Впервые он был описан в 1851 году. Хлорбензол получают путем хлорирования бензола такой в присутствии каталитического количества кислоты Льюиса, как хлорид железа , дихлорид серы и хлорид алюминия : [6]
В промышленности реакцию проводят как непрерывный процесс, чтобы свести к минимуму образование дихлорбензолов . Поскольку хлор электроотрицательен, C 6 H 5 Cl несколько снижает восприимчивость к дальнейшему хлорированию.
Лабораторные маршруты
[ редактировать ]Хлорбензол можно получить из анилина посредством хлорида бензолдиазония , иначе известного как реакция Зандмейера .
Безопасность
[ редактировать ]Хлорбензол проявляет токсичность от низкой до умеренной, о чем свидетельствует его ЛД 50, равная 2,9 г/кг. [8] Управление по охране труда установило допустимый предел воздействия на уровне 75 частей на миллион (350 мг/м2). 3 ) более восьмичасового средневзвешенного по времени времени для работников, работающих с хлорбензолом. [11]
Токсикология и биоразложение
[ редактировать ]Хлорбензол может сохраняться в почве несколько месяцев, на воздухе около 3,5 суток и в воде менее суток. Люди могут подвергнуться воздействию этого агента при вдыхании загрязненного воздуха (в основном в результате профессионального воздействия), при употреблении зараженной пищи или воды или при контакте с загрязненной почвой (обычно вблизи мест опасных отходов). Однако, поскольку он был обнаружен только на 97 из 1177 свалок опасных отходов NPL, он не считается широко распространенным загрязнителем окружающей среды. Бактерия Rhodococcusphenolicus разлагает хлорбензол, дихлорбензол и фенол как единственные источники углерода. [12]
При попадании в организм, обычно через загрязненный воздух, хлорбензол выводится как через легкие, так и через мочевыделительную систему.
На других планетах
[ редактировать ]Хлорбензол был обнаружен в осадочной породе на Марсе . [13] Было высказано предположение, что хлорбензол мог образоваться при нагревании образца в камере для отбора проб прибора. Нагревание вызвало бы реакцию органических веществ в марсианской почве, которая, как известно, содержит перхлорат.
Ссылки
[ редактировать ]- ^ Пубхим. «Хлорбензол» . pubchem.ncbi.nlm.nih.gov . Проверено 21 августа 2022 г.
- ^ Jump up to: а б с д и ж Карманный справочник NIOSH по химическим опасностям. «#0121» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Токсичность хлорбензола
- ^ Хлорбензол: LD50
- ^ Jump up to: а б «Хлорбензол» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Jump up to: а б Бек, Уве; Лёзер, Экхард (2011). «Хлорированные бензолы и другие хлорированные ароматические углеводороды». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.o06_o03 . ISBN 978-3-527-30385-4 .
- ^ Jump up to: а б Уве Бек; Экхард Лёзер (2012). «Хлорированные бензолы и другие хлорированные ароматические углеводороды». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. ISBN 978-3527306732 .
- ^ Jump up to: а б Россберг, Манфред; Лендл, Вильгельм; Пфляйдерер, Герхард; Тёгель, Адольф; Дреер, Эберхард-Людвиг; Лангер, Эрнст; Рассартс, Хайнц; Кляйншмидт, Питер; Страк, Хайнц; Кук, Ричард; Бек, Уве; Липпер, Карл-Август; Торкельсон, Теодор Р.; Лёзер, Экхард; Бэг, Клаус К.; Манн, Тревор (2006). «Хлорированные углеводороды». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a06_233.pub2 . ISBN 3527306730 .
- ^ Джеральд Бут (2007). «Нитросоединения ароматические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a17_411 . ISBN 978-3527306732 .
- ^ Вебер, Манфред; Вебер, Маркус; Кляйне-Бойманн, Майкл (2004). "Фенол". Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a19_299.pub2 . ISBN 3527306730 .
- ^ CDC - Карманный справочник NIOSH по химическим опасностям
- ^ Рефусс, М.; Урбан, Дж. (2005). « Rhodococcusphenolicus sp. nov., новый биопроцессор, выделил актиномицеты, способные разлагать хлорбензол, дихлорбензол и фенол как единственные источники углерода». Систематическая и прикладная микробиология . 28 (8): 695–701. дои : 10.1016/j.syapm.2005.05.011 . ПМИД 16261859 . Ошибка: Рефусс, М. (2006). «Ошибка в» Rhodococcusphenolicus sp. nov., новый биопроцессор выделил актиномицеты, способные разлагать хлорбензол, дихлорбензол и фенол как единственные источники углерода» [Systematic and Applied Microbiology 28 (2005) 695–701]» . Систематическая и прикладная микробиология . 29 (2): 182. doi : 10.1016/j.syapm.2005.11.005 .
- ^ Фрессине, К.; и др. (2015). «Органические молекулы в аргиллите Sheepbed, кратер Гейла, Марс» . Журнал геофизических исследований: Планеты . 120 (3): 495–514. Бибкод : 2015JGRE..120..495F . дои : 10.1002/2014JE004737 . ISSN 2169-9097 . ПМЦ 4672966 . ПМИД 26690960 .
Внешние ссылки
[ редактировать ] СМИ, связанные с хлорбензолом, на Викискладе?
СМИ, связанные с хлорбензолом, на Викискладе?