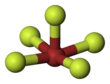
Пентафторид брома
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Пентафторид брома | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.029.234 | ||
| Номер ЕС |
| ||
ПабХим CID | |||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
| Число | 1745 | ||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| БрФ 5 | |||
| Молярная масса | 174.894 g.mol −1 | ||
| Появление | Бледно-желтая жидкость | ||
| Плотность | 2,466 г/см 3 | ||
| Температура плавления | -61,30 ° C (-78,34 ° F; 211,85 К) | ||
| Точка кипения | 40,25 ° С (104,45 ° F; 313,40 К) | ||
| Реагирует с водой | |||
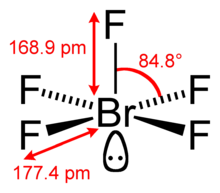
| Структура | |||
| Квадратно-пирамидальный | |||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | Мощный окислитель, коррозионный, высокотоксичный, бурно реагирует с водой с выделением HF. [1] | ||
| СГС Маркировка : | |||
    | |||
| Опасность | |||
| Х271 , Х300+Х310+Х330 , Х314 , Х372 | |||
| P210 , P220 , P221 , P260 , P264 , P270 , P271 , P280 , P283 , P284 , P301+P310 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351 +P338 , P306+P360 , P307+P311 , P309+P311 , P310 , P314 , P320 , P321 , P331 , P363 , P370+P378 , P371+P380+P375 , P403+P233 , P405 , P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | Невоспламеняющийся | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
МЕХ (Допускается) | никто [1] | ||
РЕЛ (рекомендуется) | TWA 0,1 ppm (0,7 мг/м 3 ) [1] | ||
IDLH (Непосредственная опасность) | без даты [1] | ||
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов [ мертвая ссылка ] | ||
| Родственные соединения | |||
Другие анионы | Бром монохлорид | ||
Другие катионы | Пентафторид хлора Пентафторид йода | ||
Родственные соединения | монофторид брома трифторид брома | ||
| Страница дополнительных данных | |||
| Пентафторид брома (страница данных) | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
брома Пентафторид Br F 5 представляет собой соединение и фторид брома межгалогенное . Это сильный фторирующий агент .
BrF 5 находит применение в кислорода анализе изотопов . Лазерная абляция твердых силикатов в присутствии BrF 5 выделяет O 2 для последующего анализа. [2] Он также был испытан в качестве окислителя в жидком ракетном топливе и используется в качестве фторирующего агента при переработке урана .
Подготовка [ править ]
BrF 5 был впервые получен в 1931 году прямой реакцией брома и фтора. [3] Эта реакция подходит для получения больших количеств, [ нужна ссылка ] и проводится при температуре выше 150 °C (302 °F) с избытком фтора:
- Бр 2 + 5 Ж 2 → 2 БрФ 5
Для приготовления меньших количеств бромид калия применяют: [3]
- КБр + 3 Ф 2 → КФ + БрФ 5
Этот путь дает BrF 5, практически полностью свободный от трифторидов и других примесей. [3]
Реакция [ править ]
BrF 5 реагирует с водой с образованием бромистой кислоты и плавиковой кислоты : [4]
- BrF 5 + 3 H 2 O → HBrO 3 + 5 HF
Это чрезвычайно эффективный фторирующий агент, способный превращать большинство металлов в их самые высокие фториды даже при комнатной температуре. Вместе с ураном и соединениями урана его можно использовать для получения гексафторида урана :
- 5 У + 6 БрФ 5 → 5 УФ 6 + 3 Бр 2
Опасности [ править ]
BrF 5 бурно реагирует с водой, оказывает сильное коррозионное и токсичное действие. Его пары также чрезвычайно раздражают все части тела человека, особенно кожу, глаза и другие слизистые оболочки . Как и многие другие интергалогенные соединения, он выделяет «дым», содержащий кислотные пары, при воздействии влажного воздуха, который возникает в результате его реакции с водой в воздухе. Воздействие 100 ppm или более в течение более одной минуты смертельно для большинства экспериментальных животных. Хроническое воздействие может вызвать повреждение почек и печеночную недостаточность . [5]
Кроме того, BrF 5 является сильным окислителем и может самопроизвольно воспламениться или взорваться при контакте с легковоспламеняющимися веществами, такими как органические материалы и металлическая пыль. [5]
Ссылки [ править ]
- ^ Jump up to: Перейти обратно: а б с д Карманный справочник NIOSH по химическим опасностям. «#0065» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Клейтон, Р.; Майеда, ТК (1963). «Применение пентафторида брома при извлечении кислорода из оксидов и силикатов для изотопного анализа». Geochimica et Cosmochimica Acta . 27 (1): 43–48. Бибкод : 1963GeCoA..27...43C . дои : 10.1016/0016-7037(63)90071-1 .
- ^ Jump up to: Перейти обратно: а б с Хайд, Джорджия; Будакян, М.М. (1968). «Пути синтеза пентафторидов хлора и брома». Неорганическая химия . 7 (12): 2648–2649. дои : 10.1021/ic50070a039 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 834. ИСБН 978-0-08-037941-8 .
- ^ Jump up to: Перейти обратно: а б Патнаик, Прадьот (2007). Комплексное руководство по опасным свойствам химических веществ (3-е изд.). Уайли-Интерсайенс. п. 480. ИСБН 978-0-471-71458-3 .
Внешние ссылки [ править ]
- Страница веб-книги для БрФ 5
- Международная карта химической безопасности 0974
- Карманный справочник NIOSH по химическим опасностям. «#0065» . Национальный институт охраны труда и здоровья (NIOSH).
- Национальный реестр загрязнителей - информационный бюллетень по фторидам и соединениям