Гексафторид технеция
 | |
| Идентификаторы | |
|---|---|
3D model ( JSmol ) | |
| ХимическийПаук | |
ПабХим CID | |
| Характеристики | |
| ТКФ 6 | |
| Молярная масса | 212 g/mol ( 98 Тс) |
| Появление | золотисто-желтые кристаллы [1] |
| Плотность | 3,58 г/см 3 (-140 °С), твердый [2] |
| Температура плавления | 37,4 ° C (99,3 ° F; 310,5 К) [1] |
| Точка кипения | 55,3 ° C (131,5 ° F; 328,4 К) [1] |
| Структура | |
| кубический | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Гексафторид технеция или фторид технеция(VI) ( Tc F 6 ) представляет собой желтое неорганическое соединение с низкой температурой плавления . Впервые он был идентифицирован в 1961 году. [3] В этом соединении технеций имеет степень окисления технеция +6, самую высокую степень окисления, обнаруженную у галогенидов . В этом отношении технеций отличается от рения, который образует гептафторид ReF 7 . [4] Гексафторид технеция встречается в виде примеси в гексафториде урана , поскольку технеций является продуктом деления урана , ( спонтанное деление природного урана возможное загрязнение от индуцированного деления внутри реактора в переработанном уране ). Тот факт, что температуры кипения гексафторидов урана и технеция очень близки друг к другу, представляет проблему при использовании летучести фторидов в ядерной переработке .
Подготовка
[ редактировать ]Гексафторид технеция получают нагреванием металлического технеция с избытком F 2 при 400°С. [3]
- Тс + 3 Ф
2 → ТкФ
6
Описание
[ редактировать ]Гексафторид технеция представляет собой твердое вещество золотисто-желтого цвета при комнатной температуре. Его температура плавления составляет 37,4 °С, а температура кипения — 55,3 °С. [1]
Гексафторид технеция претерпевает твердофазный переход при -4,54 ° C. Выше этой температуры (измеренной при 10 °C) твердая структура имеет кубическую форму . решетки Параметры a = 6,16 Å. приходится две формульные единицы (в данном случае дискретные молекулы) На элементарную ячейку , что дает плотность 3,02 г·см. −3 . Ниже этой температуры (измеренной при -19 ° C) твердая структура представляет собой ромбическую пространственную группу Pnma . Параметры решетки a = 9,55 Å , b = 8,74 Å и c = 5,02 Å. приходится четыре формульные единицы (в данном случае дискретные молекулы) На элементарную ячейку , что дает плотность 3,38 г·см. −3 . При -140 °C твердая структура по-прежнему является ортотомической, но параметры решетки теперь составляют a = 9,360 Å , b = 8,517 Å и c = 4,934 Å, что дает плотность 3,58 г·см. −3 . [2]
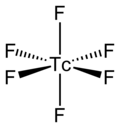
Сама молекула TcF 6 (форма, важная для жидкой или газовой фазы) имеет геометрию молекулы , имеющую точечную группу ( OH октаэдрическую ). Tc–F Длина связи составляет 1,812 Å. [2] Его магнитный момент был измерен и составил мкБ . 0,45 [5]
Характеристики
[ редактировать ]Физический
[ редактировать ]TcF 6 имеет октаэдрическую форму , как показывают инфракрасные и рамановские спектры . [6] [7] Его низкотемпературная ромбическая форма превращается в объемноцентрированную кубическую форму с более высокой симметрией при комнатной температуре, как и другие гексафториды металлов, такие как RhF 6 и OsF 6 . [8] Предварительные измерения магнитного момента дают значение 0,45 мкБ , что ниже ожидаемого для ad 1 октаэдрическое соединение. [9]
Химическая
[ редактировать ]TcF 6 реагирует с хлоридами щелочных металлов в растворе пентафторида йода (IF 5 ) с образованием гексафтортехнетатов. [10] [11] TcF 6 диспропорционируется при гидролизе водным раствором NaOH с образованием черного осадка TcO 2 . [3] В фтороводорода растворе TcF 6 реагирует с фторидом гидразина с образованием N 2 H 6 TcF 6 или N 2 H 6 (TcF 6 ) 2 . [12]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д Справочник CRC по химии и физике , 90-е издание, CRC Press, Бока-Ратон, Флорида, 2009 г., ISBN 978-1-4200-9084-0 , Раздел 4, Физические константы неорганических соединений , с. 4-93.
- ^ Перейти обратно: а б с Дрюс, Т.; Супел, Ю.; Хагенбах, А.; Зеппельт, К. (2006). «Твердотельные молекулярные структуры гексафторидов переходных металлов». Неорганическая химия . 45 (9): 3782–3788. дои : 10.1021/ic052029f . ПМИД 16634614 .
- ^ Перейти обратно: а б с Селиг, Х.; Черник, CL; Мальм, Дж. Г. (1961). «Получение и свойства TcF 6 ». Журнал неорганической и ядерной химии . 19 (3–4): 377–381. дои : 10.1016/0022-1902(61)80132-2 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Селиг, Х.; Кафассо, ФА; Грюн, DM ; Мальм, Дж. Г. (1962). «Магнитная восприимчивость ReF 6 ». Журнал химической физики . 36 (12): 3440. Бибкод : 1962ЖЧФ..36.3440С . дои : 10.1063/1.1732477 .
- ^ Говард Х. Клаассен; Генри Селиг и Джон Г. Мальм (1962). «Колебательные спектры MoF 6 и TcF 6 ». Журнал химической физики . 36 (11): 2888–2890. Бибкод : 1962JChPh..36.2888C . дои : 10.1063/1.1732396 .
- ^ Говард Х. Клаассен; Гордон Л. Гудман; Джон Х. Холлоуэй и Генри Селиг (1970). «Спектры комбинационного рассеяния MoF 6 , TcF 6 , ReF 6 , UF 6 , SF 6 , SeF 6 и TeF 6 в парообразном состоянии». Журнал химической физики . 53 (1): 341–348. Бибкод : 1970ЖЧФ..53..341С . дои : 10.1063/1.1673786 .
- ^ Сигел С., Нортроп Д.А. (1966). «Рентгеноструктурные исследования некоторых гексафторидов переходных металлов». Неорганическая химия . 5 (12): 2187–2188. дои : 10.1021/ic50046a025 .
- ^ Селиг, Х; Кафассо, Ф.А.; Грюн, Д.М.; Мальм, Дж. Г. (1962). «Магнитная восприимчивость ReF 6 ». Журнал химической физики . 36 (12): 3440–3444. Бибкод : 1962ЖЧФ..36.3440С . дои : 10.1063/1.1732477 .
- ^ Эдвардс, Эй Джей; Хьюгилл, Д.; Пикок, РД (1963). «Новые фтористые соединения технеция» . Природа . 200 (4907): 672. Бибкод : 1963Natur.200..672E . дои : 10.1038/200672a0 . S2CID 4259399 .
- ^ Д. Хагилл и Р.Д. Пикок (1966). «Некоторые пятивалентные фтортехнетаты». Журнал Химического общества А : 1339–1341. дои : 10.1039/J19660001339 .
- ^ Фрлек Б; Селиг Х. и Хайман Х.Х. (1967). «Гексафторметаллаты гидразиния (+2) (IV) и -(V) в переходных рядах 4d и 5d». Неорганическая химия . 6 (10): 1775–1783. дои : 10.1021/ic50056a004 .