Технеций
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Технеций | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | / t ɛ k ˈ n iː ʃ ( i ) ə m / | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Появление | блестящий серый металл | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Массовое число | [97] (данные не являются решающими) [а] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Технеций в таблице Менделеева | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный номер ( Z ) | 43 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа | группа 7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Период | период 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Блокировать | d-блок | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [ Кр ]4д 5 5 с 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроны на оболочку | 2, 8, 18, 13, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза в СТП | твердый | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 2430 К (2157 °С, 3915 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка кипения | 4538 К (4265 °С, 7709 °F) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность (при 20°С) | 98 Тс: 11,359 г/см 3 99 Тс: 11,475 г/см 3 [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота плавления | 33,29 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота испарения | 585,2 кДж/моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная теплоемкость | 24,27 Дж/(моль·К) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
Давление пара (экстраполировано)
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомные свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стадии окисления | −1, 0, +1, [3] [ нужна ссылка ] +2, +3, +4 , +5, +6, +7 (сильнокислотный оксид ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 1,9. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Энергии ионизации |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный радиус | эмпирический: 136 вечера | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 147±19:00 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Радиус Ван-дер-Ваальса | 205 вечера | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Другие объекты недвижимости | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Естественное явление | от распада | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кристаллическая структура | гексагональная плотноупакованная (ГПУ) ( hP2 ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Константы решетки | а = 274,12 вечера c = 439,90 вечера (при 20 ° C) [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Тепловое расширение | 8.175 × 10 −6 /К (при 20 °С) [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплопроводность | 50,6 Вт/(м⋅К) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электрическое сопротивление | 200 нОм⋅м (при 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнитный заказ | Парамагнетик | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная магнитная восприимчивость | +270.0 × 10 −6 см 3 /моль (298 К) [5] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Скорость звука тонкого стержня | 16 200 м/с (при 20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Номер CAS | 7440-26-8 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| История | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Прогноз | Дмитрий Менделеев (1871) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Открытие и первая изоляция | Эмилио Сегре и Карло Перье (1937) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изотопы технеция | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Технеций — химический элемент ; он имеет символ Tc и атомный номер 43. Это самый легкий элемент, изотопы все которого радиоактивны . Технеций и прометий — единственные радиоактивные элементы, соседи которых по атомному номеру оба стабильны. Весь доступный технеций производится как синтетический элемент . Встречающийся в природе технеций представляет собой продукт спонтанного деления урановой руд и ториевой (наиболее распространенный источник) или продукт захвата нейтронов в молибденовых рудах. Этот серебристо-серый кристаллический переходный металл находится между марганцем и рением в 7-й группе периодической таблицы , а его химические свойства занимают промежуточное положение между свойствами обоих соседних элементов. Наиболее распространенным природным изотопом является 99 Тс, только в следах.
Многие свойства технеция были предсказаны Дмитрием Менделеевым еще до его открытия; Менделеев заметил пробел в своей таблице Менделеева и дал неоткрытому элементу условное название экамарганец ( Эм ). В 1937 году технеций стал первым произведенным преимущественно искусственным элементом, отсюда и его название (от греческого technetos , «искусственный», + -ий ).
Один короткоживущий гамма-излучения , ядерный изомер технеций -99m , используется в ядерной медицине для широкого спектра тестов, таких как диагностика рака костей. Основное состояние нуклида технеций-99 используется в качестве источника бета-частиц , свободного от гамма-лучей . Долгоживущие изотопы технеция, производимые в промышленных масштабах, являются побочными продуктами деления урана -235 в ядерных реакторах и извлекаются из ядерных топливных стержней . Поскольку даже самый долгоживущий изотоп технеция имеет относительно короткий период полураспада (4,21 миллиона лет), обнаружение технеция в красных гигантах в 1952 году помогло доказать, что звезды могут производить более тяжелые элементы .
История [ править ]
Ранние предположения
С 1860-х по 1871 год ранние формы таблицы Менделеева, предложенные Дмитрием Менделеевым, содержали пробел между молибденом (элемент 42) и рутением (элемент 44). В 1871 году Менделеев предсказал, что этот недостающий элемент займет пустое место под марганцем и будет иметь аналогичные химические свойства. Менделеев дал ему предварительное название экамарганец (от эка — санскритское слово, обозначающее один ), потому что предсказанный элемент находился на одну позицию ниже известного элемента марганца. [6]
Ранние ошибочные идентификации
Многие ранние исследователи, как до, так и после публикации таблицы Менделеева, стремились первыми обнаружить и назвать недостающий элемент. Его расположение в таблице предполагало, что его будет легче найти, чем другие неоткрытые элементы.
| Год | Истец | Предлагаемое имя | Фактический материал |
|---|---|---|---|
| 1828 | Готфрид Осанн | Полиний | Иридий |
| 1845 | Генрих Роуз | Пелопий [7] | Сплав ниобий-тантал |
| 1847 | Р. Германн | Ильмениум [8] | Ниобий - танталовый сплав |
| 1877 | Серж Керн | Давиум | иридий - родий - железо Сплав |
| 1896 | Проспер Барьер | Люциус | Иттрий |
| 1908 | Масатака Огава | Ниппониум | Рений , который представлял собой неизвестный дви -марганец. [9] [10] |
Невоспроизводимые результаты [ править ]

Немецкие химики Вальтер Ноддак , Отто Берг и Ида Таке сообщили об открытии элемента 75 и элемента 43 в 1925 году и назвали элемент 43 мазурием (в честь Мазурии в восточной Пруссии , ныне в Польше , регионе, где возникла семья Уолтера Ноддака). [11] Это название вызвало значительное негодование в научном сообществе, поскольку интерпретировалось как относящееся к серии побед ; немецкой армии над русской армией в Мазурском крае во время Первой мировой войны Поскольку Ноддаки оставались на своих академических позициях, пока нацисты были у власти, подозрения и враждебность в отношении их заявлений об открытии элемента 43 продолжались. [12] Группа бомбардировала колумбит пучком электронов и пришла к выводу, что элемент 43 присутствовал в нем, исследуя рентгеновского излучения спектрограммы . [13] Длина волны производимых рентгеновских лучей связана с атомным номером по формуле, выведенной Генри Мозли в 1913 году. Команда заявила, что обнаружила слабый рентгеновский сигнал на длине волны, создаваемой элементом 43. Более поздние экспериментаторы не смогли повторить это открытие. , и это было отклонено как ошибка. [14] [15] Тем не менее, в 1933 году в серии статей об открытии элементов приводилось название «мазурий» . для элемента 43 [16] Были предприняты и некоторые более поздние попытки реабилитировать утверждения Ноддаков, но они опровергнуты исследованием Пола Курода о количестве технеция, которое могло присутствовать в изученных ими рудах: оно не могло превышать 3 × 10 −11 мкг/кг руды, и поэтому его нельзя было обнаружить методами Ноддака. [12] [17]
Официальное открытие и история более поздняя
Открытие 43- го элемента было окончательно подтверждено в эксперименте 1937 года в Университете Палермо на Сицилии Карло Перье и Эмилио Сегре . [18] В середине 1936 года Сегре посетил Соединенные Штаты, сначала Колумбийский университет в Нью-Йорке, а затем Национальную лабораторию Лоуренса Беркли в Калифорнии. Он убедил циклотрона изобретателя Эрнеста Лоуренса позволить ему забрать некоторые выброшенные детали циклотрона, которые стали радиоактивными . Лоуренс отправил ему по почте молибденовую фольгу, которая была частью дефлектора циклотрона. [19]
Сегре привлек своего коллегу Перье, чтобы попытаться доказать с помощью сравнительной химии, что активность молибдена действительно принадлежит элементу с атомным номером 43. В 1937 году им удалось выделить изотопы технеций-95m и технеций-97 . [20] [21] [ оспаривается – обсуждаем ] Представители Университета Палермо хотели, чтобы они назвали свое открытие «панормиум» , в честь латинского названия Палермо , Panormus . В 1947 году [20] Элемент 43 был назван в честь греческого слова технетос ( τεχνητός ), что означает «искусственный», поскольку это был первый элемент, полученный искусственно. [7] [11] Сегре вернулся в Беркли и встретил Гленна Т. Сиборга . Они выделили метастабильный изотоп технеций-99m , который сейчас используется примерно в десяти миллионах медицинских диагностических процедур ежегодно. [22]
В 1952 году астроном Пол У. Меррилл из Калифорнии обнаружил спектральную подпись технеция (в частности, длины волн 403,1 нм , 423,8 нм, 426,2 нм и 429,7 нм) в свете S-типа красных гигантов . [23] Жизнь звезд приближалась к концу, но они были богаты короткоживущим элементом, что указывало на то, что он вырабатывался в звездах в результате ядерных реакций . Эти данные подтвердили гипотезу о том, что более тяжелые элементы являются продуктом нуклеосинтеза в звездах. [21] Совсем недавно такие наблюдения предоставили доказательства того, что элементы образуются путем захвата нейтронов в s-процессе . [24]
После этого открытия в земных материалах было проведено множество поисков природных источников технеция. В 1962 году технеций-99 был выделен и идентифицирован в настуране из Бельгийского Конго в очень небольших количествах (около 0,2 нг/кг). [24] где он возникает как спонтанного деления продукт урана-238 . Окло Природный ядерный реактор деления содержит доказательства того, что значительные количества технеция-99 были произведены и с тех пор распались на рутений-99 . [24]
Характеристики [ править ]
Физические свойства [ править ]
Технеций — серебристо-серый радиоактивный металл , внешне похожий на платину , обычно получаемый в виде серого порошка. [25] Кристаллическая структура объемного чистого металла гексагональная плотноупакованная , а кристаллическая структура нанодисперсного чистого металла кубическая . Нанодисперсный технеций не имеет расщепленного спектра ЯМР, тогда как объемный гексагональный технеций имеет спектр ЯМР Tc-99, разделенный на 9 сателлитов. [25] [26] Атомный технеций имеет характерные линии излучения на длинах волн , 363,3 403,1, 426,2, 429,7 и 485,3 нм. [27] Параметры элементарной ячейки ромбического металлического Tc были указаны, когда Tc загрязнен углеродом (a = 0,2805(4), b = 0,4958(8), c = 0,4474(5)·нм для Tc-C с 1,38% масс. C и a = 0,2815(4), b = 0,4963(8), c = 0,4482(5)·нм для Tc-C с 1,96 мас.% C). [28] Металлическая форма слегка парамагнитна , то есть ее магнитные диполи выравниваются по внешним магнитным полям , но после прекращения действия поля принимают случайную ориентацию. [29] монокристаллический технеций становится сверхпроводником второго рода при температуре ниже 7,46 К. Чистый металлический [30] [б] Ниже этой температуры технеций имеет очень высокую глубину магнитного проникновения , большую, чем любой другой элемент, кроме ниобия . [31]
Химические свойства [ править ]
Технеций располагается в седьмой группе таблицы Менделеева, между рением и марганцем . Как и предсказывает периодический закон , его химические свойства находятся между этими двумя элементами. Из этих двух технеций больше напоминает рений, особенно по своей химической инертности и склонности к образованию ковалентных связей . [32] Это согласуется с тенденцией элементов периода 5 напоминать свои аналоги в периоде 6 больше, чем в периоде 4, из-за сокращения лантаноидов . В отличие от марганца, технеций с трудом образует катионы ( ионы с суммарным положительным зарядом). Технеций имеет девять степеней окисления от -1 до +7, наиболее распространенными из которых являются +4, +5 и +7. [33] Технеций растворяется в царской водке , азотной кислоте и концентрированной серной кислоте , но не растворяется в соляной кислоте любой концентрации. [25]
Металлический технеций медленно тускнеет во влажном воздухе. [33] и в виде порошка горит в кислороде . При реакции с водородом при высоком давлении образует гидрид TcH 1,3. [34] при реакции с углеродом образует Tc 6 C, [35] с параметром ячейки 3,98 Å, а также нанодисперсный низкоуглеродистый карбид с параметром 4,02 Å. [36]
Технеций может катализировать разрушение гидразина азотной , кислотой и это свойство обусловлено его множественностью валентностей. [37] Это вызвало проблему отделения плутония от урана при переработке ядерного топлива , где гидразин используется в качестве защитного восстановителя, удерживающего плутоний в трехвалентном, а не в более стабильном четырехвалентном состоянии. Проблема усугублялась взаимно усиленной экстракцией технеция и циркония растворителем на предыдущем этапе. [38] и потребовалось изменение процесса.
Соединения [ править ]
Пертехнетат и производные [ править ]
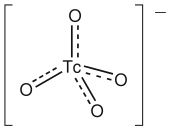
Наиболее распространенной и легкодоступной формой технеция является пертехнетат натрия Na[TcO 4 ]. Большая часть этого материала образуется в результате радиоактивного распада [ 99 МоО 4 ] 2− : [39] [40]
Пертехнетат ( TcO −
4 ) слабо гидратируется в водных растворах, [41] и он ведет себя аналогично перхлорат-аниону, оба из которых являются тетраэдрическими . В отличие от перманганата ( MnO −
4 ), это лишь слабый окислитель .
Родственным пертехнетату является гептоксид технеция . Это бледно-желтое летучее твердое вещество образуется в результате окисления металла Tc и родственных ему предшественников:
Это молекулярный оксид металла, аналог гептоксида марганца . Он имеет центросимметричную структуру с двумя типами связей Tc-O с длиной связи 167 и 184 мкм. [42]
Гептоксид технеция гидролизуется до пертехнетата и пертехнетовой кислоты в зависимости от pH: [43] [44]
HTcO 4 – сильная кислота. В концентрированной серной кислоте [TcO 4 ] − превращается в октаэдрическую форму TcO 3 (OH)(H 2 O) 2 , сопряженное основание гипотетического триаквокомплекса [ TcO 3 (H 2 O) 3 ] + . [45]
Другие халькогенидов производные
Технеций образует диоксид , [46] дисульфид , диселенид и дителлурид . Неопределенный Tc 2 S 7 образуется при обработке пертехната сероводородом. Термически разлагается на дисульфид и элементарную серу. [47] Аналогичным образом диоксид можно получить восстановлением Tc 2 O 7 .
В отличие от рения, для технеция триоксид не выделен. Однако TcO 3 был идентифицирован в газовой фазе с помощью масс-спектрометрии . [48]
Простые гидридные и галогенидные комплексы [ править ]
Технеций образует простой комплекс TcH. 2−
9 . Калийная соль изоструктурна ReH . 2−
9 . [49] Сообщалось также об образовании TcH1,3 из элементов при высоком давлении. [34]

Известны следующие бинарные (содержащие всего два элемента) галогениды технеция: TcF 6 , TcF 5 , TcCl 4 , TcBr 4 , TcBr 3 , α-TcCl 3 , β-TcCl 3 , TcI 3 , α-TcCl 2 и β-. ТсСl 2 . Степени окисления варьируются от Tc(VI) до Tc(II). Галогениды технеция имеют различные типы структуры, такие как молекулярные октаэдрические комплексы, вытянутые цепи, слоистые листы и металлические кластеры, расположенные в трехмерной сетке. [50] [51] Эти соединения получаются путем объединения металла и галогена или менее прямыми реакциями.
TcCl 4 получают хлорированием металлического Tc или Tc 2 O 7. при нагревании TcCl 4 дает соответствующие хлориды Tc(III) и Tc(II). [51]
Структура TcCl 4 состоит из бесконечных зигзагообразных цепочек октаэдров TcCl 6, имеющих общие ребра . Он изоморфен тетрахлоридам переходных металлов циркония , гафния и платины . [51]

Существуют две полиморфные модификации трихлорида технеция : α- и β-TcCl 3 . Полиморф α также обозначается как Tc 3 Cl 9 . Он принимает конфациальную биооктаэдрическую структуру . [52] Его получают обработкой хлорацетата Tc 2 (O 2 CCH 3 ) 4 Cl 2 HCl. Как и Re 3 Cl 9 , структура α-полиморфа состоит из треугольников с короткими ММ-расстояниями. β-TcCl 3 имеет октаэдрические центры Tc, которые организованы парами, как это видно также для трихлорида молибдена . TcBr 3 не принимает структуру ни одной трихлоридной фазы. Вместо этого он имеет структуру трибромида молибдена , состоящую из цепочек конфациальных октаэдров с чередующимися короткими и длинными контактами Tc—Tc. TcI 3 имеет ту же структуру, что и высокотемпературная фаза TiI 3 , и представляет собой цепочки конфациальных октаэдров с равными контактами Tc—Tc. [51]
Известно несколько анионных галогенидов технеция. Бинарные тетрагалогениды можно преобразовать в гексагалогениды [TcX 6 ] 2− (X = F, Cl, Br, I), которые принимают октаэдрическую молекулярную геометрию . [24] Более восстановленные галогениды образуют анионные кластеры со связями Tc–Tc. Аналогичная ситуация и для родственных элементов Mo, W, Re. Эти кластеры имеют ядерность Tc 4 , Tc 6 , Tc 8 и Tc 13 . Более стабильные кластеры Tc 6 и Tc 8 имеют форму призмы, в которой вертикальные пары атомов Tc соединены тройными связями, а плоские атомы - одинарными. Каждый атом технеция образует шесть связей, а оставшиеся валентные электроны могут быть насыщены одним аксиальным и двумя мостиковыми атомами галогена лиганда, такими как хлор или бром . [53]
Координационные и металлоорганические комплексы [ править ]

Технеций образует разнообразные координационные комплексы с органическими лигандами. Многие из них были хорошо исследованы из-за их значимости для ядерной медицины . [54]
Технеций образует разнообразные соединения со связями Tc–C, т. е. технецийорганические комплексы. Выдающимися представителями этого класса являются комплексы с CO, ареном и циклопентадиенильными лигандами. [55] Бинарный карбонил Tc 2 (CO) 10 представляет собой белое летучее твердое вещество. [56] В этой молекуле два атома технеция связаны друг с другом; каждый атом окружен октаэдрами из пяти карбонильных лигандов. Длина связи между атомами технеция 303 пм, [57] [58] значительно больше, чем расстояние между двумя атомами металлического технеция (272 пм). Подобные карбонилы образуются родственными технецию марганцем и рением. [59] Интерес к технецийорганическим соединениям обусловлен также применением их в ядерной медицине . [55] Технеций также образует аквакарбонильные комплексы, одним из которых является [Tc(CO) 3 (H 2 O) 3 ] + , что необычно по сравнению с карбонилами других металлов. [55]
Изотопы [ править ]
Технеций с атомным номером Z = 43 — элемент с наименьшим номером в периодической таблице, все изотопы которого радиоактивны . Второй по легкости исключительно радиоактивный элемент, прометий , имеет атомный номер 61. [33] Атомные ядра с нечетным числом протонов менее стабильны, чем ядра с четным числом, даже если общее количество нуклонов (протонов + нейтронов ) четно, [60] и элементы с нечетными номерами имеют меньше стабильных изотопов .
Наиболее стабильными радиоактивными изотопами являются технеций-97 с периодом 4,21 полураспада ± 0,16 миллиона лет и технеций-98 с периодом полураспада 4,2 ± 0,3 миллиона лет; текущие измерения их периодов полураспада дают перекрывающиеся доверительные интервалы, соответствующие одному стандартному отклонению , и, следовательно, не позволяют однозначно определить наиболее стабильный изотоп технеция. Следующим по стабильности изотопом является технеций-99, период полураспада которого составляет 211 100 лет. [1] Тридцать других радиоизотопов характеризуются массовыми числами от 85 до 118. [61] Период полураспада большинства из них составляет менее часа, за исключением технеция-93 (2,73 часа), технеция-94 (4,88 часа), технеция-95 (20 часов) и технеция-96 (4,3 дня). [62]
Первичный режим распада изотопов легче технеция-98 ( 98 Tc) — захват электронов с образованием молибдена ( Z = 42). [61] Для технеция-98 и более тяжелых изотопов основным режимом является бета-эмиссия (испускание электрона или позитрона ) с образованием рутения ( Z = 44), за исключением того, что технеций-100 может распадаться как за счет бета-излучения, так и за счет захвата электронов. [61] [63]
Технеций также имеет множество ядерных изомеров , которые представляют собой изотопы с одним или несколькими возбужденными нуклонами. Технеций-97м ( 97 м Тс; «м» означает метастабильность ) является наиболее стабильным, с периодом полураспада 91 день и энергией возбуждения 0,0965 МэВ. [62] Далее следуют технеций-95m (61 день, 0,03 МэВ) и технеций-99m (6,01 часа, 0,142 МэВ). [62]
Технеций-99 ( 99 Tc) — основной продукт деления урана-235 ( 235 U), что делает его наиболее распространенным и наиболее доступным изотопом технеция. Один грамм технеция-99 дает 6,2×10 8 распадов в секунду (иными словами, активность удельная 99 Tc составляет 0,62 Г Бк /г). [29]
и Возникновение производство
Технеций естественным образом встречается в земной коре в минимальных концентрациях около 0,003 частей на триллион. Технеций настолько редок, потому что полураспада период 97 Тс и 98 Tc составляет всего 4,2 миллиона лет. прошло более тысячи таких периодов С момента образования Земли , поэтому вероятность выживания даже одного атома первичного технеция фактически равна нулю. Однако небольшие количества существуют в виде продуктов спонтанного деления в урановых рудах . Килограмм урана содержит примерно 1 нанограмм (10 −9 г) эквивалент десяти триллионам атомов технеция. [21] [64] [65] Некоторые звезды красных гигантов спектральных классов S-, M- и N содержат спектральную линию поглощения, указывающую на присутствие технеция. [25] [66] Эти красные гиганты неофициально известны как звезды технеция .
Отходы деления [ править ]
В отличие от редкого природного явления, большие количества технеция-99 производятся каждый год из отработавших ядерных топливных стержней , которые содержат различные продукты деления. Деление грамма урана-235 в ядерных реакторах дает 27 мг технеция-99, в результате чего выход продукта деления технеция составляет 6,1%. [29] Другие делящиеся изотопы производят аналогичные выходы технеция, например, 4,9% из урана-233 и 6,21% из плутония-239 . [67] По оценкам, в период с 1983 по 1994 год в ядерных реакторах было произведено около 49 000 Т Бк (78 метрических тонн ) технеция, который на сегодняшний день является доминирующим источником земного технеция. [68] [69] Лишь часть продукции используется в коммерческих целях. [с]
Технеций-99 производится в результате ядерного деления урана-235 и плутония-239. Поэтому он присутствует в радиоактивных отходах и ядерных осадках в результате взрывов ядерных бомб . Его распад, измеряемый в беккерелях на количество отработавшего топлива, вносит основной вклад в радиоактивность ядерных отходов примерно через 10 лет. 4 до 10 6 лет после образования ядерных отходов. [68] С 1945 по 1994 год примерно 160 Т Бк (около 250 кг) технеция-99 было выброшено в окружающую среду во время атмосферных ядерных испытаний . [68] [70] Количество технеция-99 из ядерных реакторов, выброшенного в окружающую среду до 1986 г., составляет порядка 1000 ТБк (около 1600 кг), преимущественно при переработке ядерного топлива ; большая часть этого была сброшена в море. С тех пор методы переработки позволили сократить выбросы, но по состоянию на 2005 год основной выброс технеция-99 в окружающую среду приходится на завод в Селлафилде около 550 ТБк (около 900 кг) , который с 1995 по 1999 год выбросил в Ирландское море . [69] С 2000 года эта сумма была ограничена постановлением до 90 ТБк (около 140 кг) в год. [71] Сброс технеция в море привел к загрязнению некоторых морепродуктов незначительными количествами этого элемента. Например, европейские омары и рыба из западной Камбрии содержат около 1 Бк/кг технеция. [72] [73] [д]
для коммерческого использования деления Продукт
Метастабильный изотоп технеций-99m непрерывно производится как продукт деления урана или плутония в ядерных реакторах :
Поскольку отработанное топливо выдерживается в течение нескольких лет перед переработкой, весь молибден-99 и технеций-99m распадаются к тому времени, когда продукты деления отделяются от основных актинидов при обычной ядерной переработке . Жидкость, оставшаяся после плутоний-урановой экстракции ( PUREX ), содержит высокую концентрацию технеция в виде TcO. −
4 но почти всё это технеций-99, а не технеций-99м. [75]
Подавляющее большинство технеция-99м, используемого в медицинской работе, производится путем облучения специальных мишеней из высокообогащенного урана в реакторе, извлечения молибдена-99 из мишеней на перерабатывающих предприятиях, [40] и восстановление в диагностическом центре технеция-99м, образующегося при распаде молибдена-99. [76] [77] Молибден-99 в форме молибдата МоО. 2−
4 адсорбируется ( на кислом оксиде алюминия Al
22О
3 ) в экранированном колоночном хроматографе внутри генератора технеция-99m («технетиевая корова», также иногда называемая «молибденовой коровой»). Молибден-99 имеет период полураспада 67 часов, поэтому короткоживущий технеций-99m (период полураспада: 6 часов), образующийся в результате его распада, образуется постоянно. [21] Растворимый пертехнетат TcO −
4 затем может быть химически экстрагирован путем элюирования соляным раствором . Недостатком этого процесса является то, что для него требуются мишени, содержащие уран-235, на которые распространяются меры безопасности, связанные с делящимися материалами. [78] [79]

Почти две трети мировых поставок приходится на два реактора; Национальный исследовательский универсальный реактор в лабораториях Чок-Ривер в Онтарио, Канада, и высокопоточный реактор в Группе ядерных исследований и консультирования в Петтене, Нидерланды. Все основные реакторы, производящие технеций-99m, были построены в 1960-х годах, и их срок эксплуатации близок к концу . Два новых канадских многоцелевых реактора прикладной физики с решетчатым экспериментом, запланированные и построенные для производства 200% потребности в технеции-99m, освободили всех других производителей от строительства собственных реакторов. После отмены уже испытанных реакторов в 2008 году будущие поставки технеция-99m стали проблематичными. [80]
Утилизация отходов [ править ]
Длительный период полураспада технеция-99 и его способность образовывать анионные соединения создают серьезную проблему для долгосрочного захоронения радиоактивных отходов . Многие из процессов, предназначенных для удаления продуктов деления на заводах по переработке, нацелены на катионные соединения, такие как цезий (например, цезий-137 ) и стронций (например, стронций-90 ). Следовательно, пертехнетат ускользает в результате этих процессов. Текущие варианты захоронения отдают предпочтение захоронению в континентальных, геологически стабильных породах. Основная опасность такой практики заключается в вероятности контакта отходов с водой, которая может привести к попаданию радиоактивного загрязнения в окружающую среду. Анионный пертехнетат и йодид имеют тенденцию не адсорбироваться на поверхности минералов и, вероятно, будут вымыты. Для сравнения: плутоний , уран и цезий имеют тенденцию связываться с частицами почвы. Технеций может быть иммобилизован некоторыми средами, такими как микробная активность в донных отложениях озер, [81] а экологическая химия технеция является областью активных исследований. [82]
Альтернативный метод утилизации — трансмутация — был продемонстрирован в ЦЕРН для технеция-99. В этом процессе технеций (технеций-99 в качестве металлической мишени) бомбардируется нейтронами с образованием короткоживущего технеция-100 (период полураспада = 16 секунд), который распадается в результате бета-распада до стабильного рутения -100. Если целью является извлечение пригодного для использования рутения, то необходим чрезвычайно чистый мишень из технеция; небольшие следы второстепенных актинидов, таких как америций и кюрий если в мишени присутствуют , они, вероятно, подвергнутся делению и образуют больше продуктов деления , которые увеличивают радиоактивность облученной мишени. Образование рутения-106 (период полураспада 374 дня) в результате «свежего деления», вероятно, увеличит активность конечного металлического рутения, которому затем потребуется более длительное время охлаждения после облучения, прежде чем рутений можно будет использовать. [83]
Фактическое отделение технеция-99 от отработавшего ядерного топлива — длительный процесс. При переработке топлива оно выделяется в составе высокорадиоактивных жидких отходов. После нескольких лет простоя радиоактивность снижается до уровня, при котором извлечение долгоживущих изотопов, включая технеций-99, становится возможным. В результате серии химических процессов получается металл технеций-99 высокой чистоты. [84]
Нейтронная активация [ править ]
Молибден-99 , который распадается с образованием технеция-99m, может образовываться путем нейтронной активации молибдена-98. [85] При необходимости другие изотопы технеция не производятся в значительных количествах путем деления, а производятся нейтронным облучением исходных изотопов (например, технеций-97 может быть получен нейтронным облучением рутения-96 ). [86]
Ускорители частиц [ править ]
Возможность получения технеция-99m при бомбардировке протонами с энергией 22 МэВ мишени из молибдена-100 в медицинских циклотронах по реакции 100 Мо(п,2n) 99 м Тс был продемонстрирован в 1971 году. [87] Недавний дефицит медицинского технеция-99m возобновил интерес к его производству путем протонной бомбардировки изотопно-обогащенных (>99,5%) мишеней из молибдена-100. [88] [89] Исследуются другие методы получения молибдена-99 из молибдена-100 посредством реакций (n,2n) или (γ,n) в ускорителях частиц. [90] [91] [92]
Приложения [ править ]
медицина Ядерная и биология
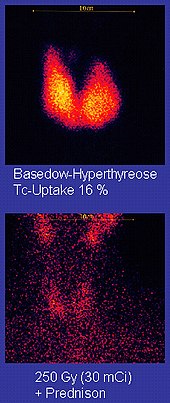
Технеций-99m («м» указывает на то, что это метастабильный ядерный изомер) используется в медицинских испытаниях радиоактивных изотопов . Например, технеций-99m — это радиоактивный индикатор , который отслеживает медицинское оборудование для визуализации в организме человека. [21] [88] Он хорошо подходит для этой роли, поскольку излучает легко обнаруживаемые 140 кэВ гамма-лучи с энергией , а его период полураспада составляет 6,01 часа (это означает, что около 94% его распадается до технеция-99 за 24 часа). [29] Химия технеция позволяет связывать его с множеством биохимических соединений, каждое из которых определяет, как он метаболизируется и откладывается в организме, и этот единственный изотоп можно использовать для множества диагностических тестов. более 50 распространенных радиофармпрепаратов На основе технеция-99m создано , предназначенных для визуализации и функциональных исследований головного мозга , сердечной мышцы, щитовидной железы , легких , печени , желчного пузыря , почек , скелета , крови и опухолей . [93]
Долгоживущий изотоп технеций-95m с периодом полураспада 61 день используется в качестве радиоактивного индикатора для изучения движения технеция в окружающей среде, а также в растительных и животных системах. [94]
Промышленно-химическая [ править ]
Технеций-99 почти полностью распадается в результате бета-распада, испуская бета-частицы с постоянными низкими энергиями и без сопутствующих гамма-лучей. Более того, его длительный период полураспада означает, что это выделение со временем уменьшается очень медленно. Его также можно извлечь до высокой химической и изотопной чистоты из радиоактивных отходов. По этим причинам это стандартный бета-излучатель Национального института стандартов и технологий (NIST) и используется для калибровки оборудования. [95] Технеций-99 также был предложен для использования в оптоэлектронных устройствах и наноразмерных ядерных батареях . [96]
Подобно рению и палладию , технеций может служить катализатором . В таких процессах, как дегидрирование изопропилового спирта , он является гораздо более эффективным катализатором, чем рений или палладий. Однако его радиоактивность является серьезной проблемой при безопасном каталитическом применении. [97]
Когда сталь погружают в воду, добавление в воду небольшой концентрации (55 частей на миллион ) пертехнетата калия (VII) защищает сталь от коррозии. [98] даже если температура повышается до 250 °C (523 К). [99] По этой причине пертехнетат использовался в качестве ингибитора анодной коррозии стали, хотя радиоактивность технеция создает проблемы, которые ограничивают его применение автономными системами. [100] В то время как (например) CrO 2−
4 также может ингибировать коррозию, для этого требуется концентрация в десять раз выше. В одном эксперименте образец углеродистой стали выдерживался в водном растворе пертехнетата в течение 20 лет и до сих пор не подвергся коррозии. [99] Механизм, с помощью которого пертехнетат предотвращает коррозию, не совсем понятен, но, по-видимому, включает обратимое образование тонкого поверхностного слоя ( пассивацию ). Одна теория утверждает, что пертехнетат реагирует с поверхностью стали, образуя слой диоксида технеция , который предотвращает дальнейшую коррозию; тот же эффект объясняет, как можно использовать порошок железа для удаления пертехнетата из воды. Эффект быстро исчезает, если концентрация пертехнетата падает ниже минимальной концентрации или если добавляется слишком высокая концентрация других ионов. [101]
Как уже отмечалось, радиоактивная природа технеция (3 МБк/л в необходимых концентрациях) делает такую защиту от коррозии практически во всех ситуациях непрактичной. [98] Тем не менее, защита от коррозии пертехнетат-ионами была предложена (но так и не была принята) для использования в реакторах с кипящей водой . [101]
Меры предосторожности [ править ]
Технеций не играет естественной биологической роли и обычно не встречается в организме человека. [25] Технеций производится в больших количествах в результате ядерного деления и распространяется легче, чем многие радионуклиды. Похоже, что он имеет низкую химическую токсичность. Например, у крыс, которые потребляли до 15 мкг технеция-99 на грамм пищи в течение нескольких недель, не было обнаружено существенных изменений в формуле крови, массе тела и органов, а также в потреблении пищи. [102] В организме технеций быстро превращается в стабильный TcO. −
Ион 4 , который хорошо растворим в воде и быстро выводится из организма. Радиологическая токсичность технеция (на единицу массы) зависит от соединения, типа излучения рассматриваемого изотопа и периода полураспада изотопа. [103]
Со всеми изотопами технеция необходимо обращаться осторожно. Самый распространенный изотоп, технеций-99, является слабым бета-излучателем; такое излучение останавливают стенки лабораторной посуды. Основная опасность при работе с технецием — вдыхание пыли; такое радиоактивное загрязнение легких может представлять значительный риск развития рака. Для большинства работ осторожного обращения в вытяжном шкафу достаточно , перчаточный ящик не требуется. [104]
Примечания [ править ]
- ^ Самый стабильный изотоп технеция не может быть определен на основе существующих данных из-за перекрывающихся неопределенностей измерения периодов полураспада двух самых долгоживущих изотопов. Период полураспада 97 Tc с неопределенностью, соответствующей одному стандартному отклонению, составляет 4,21 ± 0,16 млн лет, тогда как для 98 Тс составляет 4,2 ± 0,3 млн лет; эти измерения имеют перекрывающиеся доверительные интервалы . [1]
- ^ Кристаллы неправильной формы и следы примесей повышают температуру перехода до 11,2 К для порошка технеция с чистотой 99,9%. [30]
- ^ По состоянию на 2005 г. [update]Технеций-99 в форме пертехнетата аммония доступен обладателям разрешения Национальной лаборатории Ок-Ридж . [25]
- ^ Анаэробные . спорообразующие IV бактерии Clostridium рода ( ) способны восстанавливать Tc(VII) до Tc Бактерии Clostridia играют роль в восстановлении железа, марганца и урана, тем самым влияя на растворимость этих элементов в почве и отложениях. Их способность восстанавливать технеций может во многом определять подвижность технеция в промышленных отходах и других подземных средах. [74]
Ссылки [ править ]
- ↑ Перейти обратно: Перейти обратно: а б с Кондев, ФГ; Ван, М.; Хуанг, WJ; Наими, С.; Ауди, Г. (2021). «Оценка ядерных свойств NUBASE2020» (PDF) . Китайская физика C . 45 (3): 030001. doi : 10.1088/1674-1137/abddae .
- ↑ Перейти обратно: Перейти обратно: а б с Арбластер, Джон В. (2018). Некоторые значения кристаллографических свойств элементов . Парк материалов, Огайо: ASM International. ISBN 978-1-62708-155-9 .
- ^ «Технеций: данные о соединении йодида технеция (III)» . OpenMOPAC.net . Проверено 10 декабря 2007 г.
- ^ Маттолат, К.; Готвальд, Т.; Редер, С.; Роте, С.; Швеллнус, Ф.; Вендт, К.; Тёрле-Поспих, П.; Траутманн, Н. (24 мая 2010 г.). «Определение первого потенциала ионизации технеция». Физический обзор А. 81 : 052513. doi : 10.1103/PhysRevA.81.052513 .
- ^ Уэст, Роберт (1984). CRC, Справочник по химии и физике . Бока-Ратон, Флорида: Издательство компании Chemical Rubber Company. стр. E110. ISBN 0-8493-0464-4 .
- ^ Йонге; Паувелс, ЭК (1996). «Технеций, недостающий элемент». Европейский журнал ядерной медицины . 23 (3): 336–44. дои : 10.1007/BF00837634 . ПМИД 8599967 . S2CID 24026249 .
- ↑ Перейти обратно: Перейти обратно: а б Холден, Н. Е. «История происхождения химических элементов и их первооткрыватели» . Брукхейвенская национальная лаборатория . Проверено 5 мая 2009 г.
- ^ Германн, Р. (1847). «Исследования Ильмениума» . Журнал практической химии . 40 : 457-480. дои : 10.1002/prac.184704001110 .
- ^ Ёшихара, Гонконг (2004). «Открытие нового элемента «ниппоний»: переоценка новаторских работ Масатаки Огавы и его сына Эйджиро Огавы». Spectrochimica Acta Часть B. 59 (8): 1305–1310. Бибкод : 2004AcSpe..59.1305Y . дои : 10.1016/j.sab.2003.12.027 .
- ^ Хисамацу, Ёдзи; Эгашира, Казухиро; Маэно, Ёситеру (2022). «Ниппоний Огавы и его переприсвоение рению» . Основы химии . 24 : 15–57. дои : 10.1007/s10698-021-09410-x .
- ↑ Перейти обратно: Перейти обратно: а б ван дер Крогт, П. «Технеций» . Элентимолгия и элементы Multidict . Проверено 5 мая 2009 г.
- ↑ Перейти обратно: Перейти обратно: а б Шерри, Эрик (2013). Сказка о семи стихиях . Издательство Оксфордского университета. стр. 109–114, 125–131. ISBN 978-0-19-539131-2 .
- ^ Эмсли 2001 , с. 423.
- ^ Армстронг, Джей Ти (2003). «Технеций» . Новости химии и техники . 81 (36): 110. doi : 10.1021/cen-v081n036.p110 . Проверено 11 ноября 2009 г.
- ^ Нис, К.А. (2001). «Ида Таке и война за открытие деления» . Архивировано из оригинала 9 августа 2009 г. Проверено 5 мая 2009 г.
- ^ Уикс, Мэн (1933). «Открытие элементов. XX. Недавно открытые элементы». Журнал химического образования . 10 (3): 161–170. Бибкод : 1933JChEd..10..161W . дои : 10.1021/ed010p161 .
- ^ Хабаши, Фатхи (2006). «История элемента 43 — технеция» . Журнал химического образования . 83 (2): 213. Бибкод : 2006JChEd..83..213H . дои : 10.1021/ed083p213.1 . Проверено 2 января 2023 г.
- ^ Хейзерман, Д.Л. (1992). «Элемент 43: Технеций» . Изучение химических элементов и их соединений . Нью-Йорк: TAB Books. п. 164. ИСБН 978-0-8306-3018-9 .
- ^ Сегре, Эмилио (1993). Разум всегда в движении: автобиография Эмилио Сегре . Беркли, Калифорния: Издательство Калифорнийского университета. стр. 115–118 . ISBN 978-0520076273 .
- ↑ Перейти обратно: Перейти обратно: а б Перье, К.; Сегре, Э. (1947). «Технеций: элемент с атомным номером 43». Природа . 159 (4027): 24. Бибкод : 1947Natur.159...24P . дои : 10.1038/159024a0 . ПМИД 20279068 . S2CID 4136886 .
- ↑ Перейти обратно: Перейти обратно: а б с д и Эмсли 2001 , стр. 422–425 .
- ^ Хоффман, Дарлин К.; Гиорсо, Альберт; Сиборг, Гленн Т. (2000). «Глава 1.2: Первые дни работы в радиационной лаборатории Беркли» . Трансурановые люди: история изнутри . Калифорнийский университет, Беркли и Национальная лаборатория Лоуренса Беркли. п. 15. ISBN 978-1-86094-087-3 . Архивировано из оригинала 24 января 2007 г. Проверено 31 марта 2007 г.
- ^ Меррилл, PW (1952). «Технеций в звездах». Наука . 115 (2992): 479–489 [484]. Бибкод : 1952Sci...115..479. . дои : 10.1126/science.115.2992.479 . ПМИД 17792758 .
- ↑ Перейти обратно: Перейти обратно: а б с д Швохау, 2000 , стр. 7–9.
- ↑ Перейти обратно: Перейти обратно: а б с д и ж Хаммонд 2004 , с. [ нужна страница ] .
- ^ Tarasov, V.P.; Muravlev, Yu. B.; German, K. E.; Popova, N. N. (2001). " 99 Tc ЯМР нанесенных наночастиц технеция» . Доклады физической химии . 377 (1–3): 71–76. doi : 10.1023/A:1018872000032 . S2CID 91522281 .
- ^ Лиде, Дэвид Р. (2004–2005). «Линейчатые спектры элементов» . Справочник CRC . ЦРК Пресс. стр. 10–70 (1672). ISBN 978-0-8493-0595-5 .
- ^ German, K. E.; Peretrukhin, V. F.; Gedgovd, K. N.; Grigoriev, M. S.; Tarasov, A. V.; Plekhanov, Yu V.; Maslennikov, A. G.; Bulatov, G. S.; Tarasov, V. P.; Lecomte, M. (2005). "Tc Carbide and New Orthorhombic Tc Metal Phase" . Journal of Nuclear and Radiochemical Sciences . 6 (3): 211–214. doi : 10.14494/jnrs2000.6.3_211 .
- ↑ Перейти обратно: Перейти обратно: а б с д Римшоу, SJ (1968). Хэмпель, Калифорния (ред.). Энциклопедия химических элементов . Нью-Йорк: Книжная корпорация Рейнхолда. стр. 689–693 .
- ↑ Перейти обратно: Перейти обратно: а б Швохау 2000 , с. 96.
- ^ Аутлер, С.Х. (1968). «Технеций как материал для применения в сверхпроводимости переменного тока» (PDF) . Материалы летнего исследования сверхпроводников и ускорителей 1968 года . Проверено 5 мая 2009 г.
- ^ Гринвуд и Эрншоу 1997 , с. 1044.
- ↑ Перейти обратно: Перейти обратно: а б с Хастед, Р. (15 декабря 2003 г.). «Технеций» . Периодическая таблица элементов . Лос-Аламосская национальная лаборатория . Проверено 11 октября 2009 г.
- ↑ Перейти обратно: Перейти обратно: а б Zhou, Di; Semenok, Dmitrii V.; Volkov, Mikhail A.; Troyan, Ivan A.; Seregin, Alexey Yu.; Chepkasov, Ilya V.; Sannikov, Denis A.; Lagoudakis, Pavlos G.; Oganov, Artem R.; German, Konstantin E. (2023-02-06). "Synthesis of technetium hydride TcH 1.3 at 27 GPa" . Physical Review B . 107 (6): 064102. arXiv : 2210.01518 . doi : 10.1103/PhysRevB.107.064102 .
- ^ German, K. E.; Peretrukhin, V. F.; Gedgovd, K. N.; Grigoriev, M. S.; Tarasov, A. V.; Plekhanov, Yu V.; Maslennikov, A. G.; Bulatov, G. S.; Tarasov, V. P.; Lecomte, M. (2005). "Tc Carbide and New Orthorhombic Tc Metal Phase" . Journal of Nuclear and Radiochemical Sciences . 6 (3): 211–214. doi : 10.14494/jnrs2000.6.3_211 .
- ^ Кузнецов Виталий Владимирович; Герман Константин Евгеньевич; Наговицына Ольга А.; Филатова Елена Александровна; Волков Михаил А.; Ситанская Анастасия Владимировна; Пшеничкина Татьяна В. (31 октября 2023 г.). «Путь к стабилизации нанотехнеция в аморфной углеродной матрице: препаративные методы, данные XAFS и электрохимические исследования» . Неорганическая химия . 62 (45): 18660–18669. doi : 10.1021/acs.inorgchem.3c03001 . ISSN 0020-1669 . ПМИД 37908073 .
- ^ Гарравэй, Джон (1984). «Катализируемое технецием окисление гидразина азотной кислотой». Журнал менее распространенных металлов . 97 : 191–203. дои : 10.1016/0022-5088(84)90023-7 .
- ^ Гарравэй, Дж. (1985). «Совместная экстракция пертехнетата и циркония три-н-бутилфосфатом». Журнал менее распространенных металлов . 106 (1): 183–192. дои : 10.1016/0022-5088(85)90379-0 .
- ^ Швохау 2000 , стр. 127–136.
- ↑ Перейти обратно: Перейти обратно: а б Мур, PW (апрель 1984 г.). «Технеций-99 в генераторных системах» (PDF) . Журнал ядерной медицины . 25 (4): 499–502. ПМИД 6100549 . Проверено 11 мая 2012 г.
- ^ Устынюк Юрий А.; Глориозов Игорь П.; Жохова Нелли И.; Герман Константин Евгеньевич; Калмыков, Степан Н. (15 ноября 2021 г.). «Гидратация пертехнетат-аниона. ТФП-исследование» . Журнал молекулярных жидкостей . 342 : 117404. doi : 10.1016/j.molliq.2021.117404 . ISSN 0167-7322 .
- ^ Кребс, Б. (1969). «Оксид технеция (VII) — оксид переходного металла с молекулярной структурой в твердом состоянии». Прикладная химия (на немецком языке). 81 (9): 328–329. дои : 10.1002/anie.19690810905 .
- ^ Швохау 2000 , с. 127.
- ^ Херрелл, AY; Бьюзи, Р.Х.; Гейер, К.Х. (1977). Оксид технеция (VII) в неорганическом синтезе . Том. XVII. стр. 155–158. ISBN 978-0-07-044327-3 .
- ^ Пуано Ф., Век П.Ф., Герман К., Марук А., Киракосян Г., Люкенс В., Рего Д.Б. и др. (2010). «Вид семивалентного технеция в серной кислоте: структурные и спектроскопические исследования» (PDF) . Транзакции Далтона . 39 (37): 8616–8619. дои : 10.1039/C0DT00695E . ПМИД 20730190 . S2CID 9419843 . Архивировано из оригинала (PDF) 5 марта 2017 г. Проверено 14 ноября 2011 г.
- ^ Швохау 2000 , с. 108.
- ^ Швохау 2000 , стр. 112–113.
- ^ Гибсон, Джон К. (1993). «Высокотемпературные оксидные и гидроксидные пары технеция». Радиохимика Акта . 60 (2–3): 121–126. дои : 10.1524/ract.1993.60.23.121 . S2CID 99795348 .
- ^ Швохау 2000 , с. 146.
- ^ Джонстон, EV (май 2014 г.). Бинарные галогениды технеция . Диссертации, диссертации, профессиональные статьи и основные положения UNLV (тезисы). Университет Невады, Лас-Вегас. дои : 10.34917/5836118 .
- ↑ Перейти обратно: Перейти обратно: а б с д Пуано, Фредерик; Джонстон, Эрик В.; Червински, Кеннет Р.; Саттельбергер, Альфред П. (2014). «Последние достижения в химии галогенидов технеция». Отчеты о химических исследованиях . 47 (2): 624–632. дои : 10.1021/ar400225b . ПМИД 24393028 .
- ^ Пуано, Фредерик; Джонстон, Эрик В.; Век, Филипп Ф.; Ким, Ынджа; Форстер, Пол М.; Скотт, Брайан Л.; Саттельбергер, Альфред П.; Червински, Кеннет Р. (2010). «Синтез и структура трихлорида технеция». Журнал Американского химического общества . 132 (45): 15864–5. дои : 10.1021/ja105730e . ПМИД 20977207 .
- ^ немецкий, КЭ; Крючков, С.В. (2002). «Полиядерные кластеры галогенидов технеция» . Российский журнал неорганической химии . 47 (4): 578–583. Архивировано из оригинала 22 декабря 2015 г.
- ^ Бартоломя, Марк Д.; Луи, Аника С.; Вэллиант, Джон Ф.; Зубиета, Джон (2010). «Радиофармацевтические препараты, полученные из технеция и галлия: сравнение и сопоставление химического состава двух важных радиометаллов для эпохи молекулярной визуализации». Химические обзоры . 110 (5): 2903–20. дои : 10.1021/cr1000755 . ПМИД 20415476 .
- ↑ Перейти обратно: Перейти обратно: а б с Альберто, Роджер (2010). «Металлоорганические радиофармпрепараты». Медицинская металлоорганическая химия . Темы металлоорганической химии. Том. 32. С. 219–246. дои : 10.1007/978-3-642-13185-1_9 . ISBN 978-3-642-13184-4 .
- ^ Хилман, Дж. К.; Хаггинс, ДК; Каес, HD (1961). «Карбонил технеция». Журнал Американского химического общества . 83 (13): 2953–2954. дои : 10.1021/ja01474a038 .
- ^ Бейли, МФ; Даль, Лоуренс Ф. (1965). «Кристаллическая структура декакарбонила дитехнеция». Неорганическая химия . 4 (8): 1140–1145. дои : 10.1021/ic50030a011 .
- ^ Уоллах, Д. (1962). «Элементарная ячейка и пространственная группа карбонила технеция, Tc2 (CO) 10». Акта Кристаллографика . 15 (10): 1058. Бибкод : 1962AcCry..15.1058W . дои : 10.1107/S0365110X62002789 .
- ^ Швохау 2000 , стр. 286, 328.
- ^ Клейтон, Д.Д. (1983). Принципы звездной эволюции и нуклеосинтеза: с новым предисловием . Издательство Чикагского университета. п. 547 . ISBN 978-0-226-10953-4 .
- ↑ Перейти обратно: Перейти обратно: а б с Сонцогни, А.А. (ред.). «Таблица нуклидов» . Нью-Йорк: Национальный центр ядерных данных, Брукхейвенская национальная лаборатория. Архивировано из оригинала 25 августа 2009 г. Проверено 11 ноября 2009 г.
- ↑ Перейти обратно: Перейти обратно: а б с Холден, Нью-Йорк (2006). Лиде. ДР (ред.). Справочник по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press. стр. 11-88–11-89. ISBN 978-0-8493-0487-3 .
- ^ Лиде, Дэвид Р., изд. (2004–2005). «Таблица изотопов». Справочник CRC по химии и физике . ЦРК Пресс.
- ^ Диксон, П.; Кертис, Дэвид Б.; Масгрейв, Джон; Ренш, Фред; Роуч, Джефф; Рокоп, Дон (1997). «Анализ естественно произведенного технеция и плутония в геологических материалах». Аналитическая химия . 69 (9): 1692–1699. дои : 10.1021/ac961159q . ПМИД 21639292 .
- ^ Кертис, Д.; Фабрика-Мартин, июнь; Диксон, Пол; Крамер, Ян (1999). «Необычные элементы природы: плутоний и технеций» . Geochimica et Cosmochimica Acta . 63 (2): 275. Бибкод : 1999GeCoA..63..275C . дои : 10.1016/S0016-7037(98)00282-8 .
- ^ Мур, CE (1951). «Технеций на Солнце». Наука . 114 (2951): 59–61. Бибкод : 1951Sci...114...59M . дои : 10.1126/science.114.2951.59 . ПМИД 17782983 .
- ^ Швохау 2000 , стр. 374–404.
- ↑ Перейти обратно: Перейти обратно: а б с Ёшихара, К. (1996). «Технеций в окружающей среде». Ин Ёсихара, К.; Омори, Т. (ред.). Технеций и рений: их химия и применение . Темы современной химии. Том. 176. Берлин, Гейдельберг: Springer-Verlag. стр. 17–35. дои : 10.1007/3-540-59469-8_2 . ISBN 978-3-540-59469-7 .
- ↑ Перейти обратно: Перейти обратно: а б Гарсиа-Леон, М. (2005). «99Tc в окружающей среде: источники, распространение и методы» (PDF) . Журнал ядерных и радиохимических наук . 6 (3): 253–259. дои : 10.14494/jnrs2000.6.3_253 .
- ^ Десмет, Г.; Миттенар, К. (1986). Технеций в окружающей среде . Спрингер. п. 69. ИСБН 978-0-85334-421-6 .
- ^ Тагами, К. (2003). «Поведение технеция-99 в земной среде — полевые наблюдения и эксперименты с радиоиндикаторами» . Журнал ядерных и радиохимических наук . 4 : А1–А8. дои : 10.14494/jnrs2000.4.a1 .
- ^ Сефер, П.; Нриагу, ДЖО (2006). Минеральные компоненты в продуктах питания . ЦРК Пресс. п. 403. ИСБН 978-0-8493-2234-1 .
- ^ Харрисон, доктор юридических наук; Фиппс, А. (2001). «Кишечный перенос и дозы технеция из окружающей среды». Журнал радиологической защиты . 21 (1): 9–11. Бибкод : 2001JRP....21....9H . дои : 10.1088/0952-4746/21/1/004 . ПМИД 11281541 . S2CID 250752077 .
- ^ Фрэнсис, AJ; Додж, CJ; Мейнкен, GE (2002). «Биотрансформация пертехнетата клостридиями » . Радиохимика Акта . 90 (9–11): 791–797. дои : 10.1524/ract.2002.90.9-11_2002.791 . S2CID 83759112 .
- ^ Швохау 2000 , с. 39.
- ^ США 3799883 , Хирофуми Арино, «Ступенька из древесного угля с серебряным покрытием», выдан 26 марта 1974 г., передан Union Carbide Corporation.
- ^ Комитет по производству медицинских изотопов без высокообогащенного урана (2009). Производство медицинских изотопов без высокообогащенного урана . Пресса национальных академий. п. VII. ISBN 978-0-309-13040-0 .
- ^ Люценкирхен, К.-Р. «Сыщики-ядерщики-криминалисты выявляют происхождение незаконно перевезенных материалов» . Лос-Аламосская национальная лаборатория. Архивировано из оригинала 16 февраля 2013 г. Проверено 11 ноября 2009 г.
- ^ Снелгроув, JL; Хофман, Г.Л. (1995). Разработка и обработка целевых показателей НОУ для производства Mo-99 (PDF) . 1995 г. Международное совещание по пониженному обогащению исследовательских и испытательных реакторов, 18–21 сентября 1994 г., Париж, Франция. ANL.gov . Проверено 5 мая 2009 г.
- ^ Томас, Грегори С.; Маддахи, Джамшид (2010). «Дефицит технеция». Журнал ядерной кардиологии . 17 (6): 993–8. дои : 10.1007/s12350-010-9281-8 . ПМИД 20717761 . S2CID 2397919 .
- ^ Герман Константин Евгеньевич; Фирсова Е.В.; Перетрухин В.Ф.; Хижняк, ТВ; Симонов, М. (2003). «Биоаккумуляция Tc, Pu и Np на донных отложениях двух типов пресноводных озер Московской области». Радиохимия . 45 (6): 250–256. дои : 10.1023/А:1026008108860 . S2CID 55030255 .
- ^ Шоу, Г. (2007). Радиоактивность в земной среде . Эльзевир. п. 147. ИСБН 978-0-08-043872-6 .
- ^ Альтомаре, П; Бернарди (1979). Альтернативные концепции захоронения высокоактивных и трансурановых радиоактивных отходов . Агентство по охране окружающей среды США.
- ^ Швохау 2000 , стр. 87–96.
- ^ «Руководство по радиоизотопам, производимым в реакторах» (PDF) . МАГАТЭ. Январь 2003 года . Проверено 27 августа 2009 г.
- ^ Келли, Джей-Джей (1980). Радиационный надзор за стоками и окружающей средой: симпозиум . АСТМ Интернешнл. п. 91.
- ^ Бивер, Дж. Э.; Хупф, HB (ноябрь 1971 г.). «Производство 99 м Tc на медицинском циклотроне: технико-экономическое обоснование» (PDF) . Журнал ядерной медицины . 12 (11): 739–741. PMID 5113635 .
- ↑ Перейти обратно: Перейти обратно: а б Лоуренс Найт (30 мая 2015 г.). «Элемент, который может заставить кости светиться» . Новости Би-би-си . Проверено 30 мая 2015 г.
- ^ Герен Б., Трембле С., Родриг С., Руссо Ж.А. и др. (2010). «Циклотронное производство 99 м Tc: подход к кризису медицинских изотопов» (PDF) . Journal of Nuclear Medicine . 51 (4): 13N–6N. PMID 20351346 .
- ^ Шолтен, Бернхард; Ламбрехт, Ричард М.; Коньо, Мишель; Вера Руис, Эрнан; Каим, Сайед М. (25 мая 1999 г.). «Функции возбуждения для циклотронного производства 99 м Тс и 99 Mo». Applied Radiation and Isotopes . 51 (1): 69–80. Bibcode : 1999AppRI..51...69S . doi : 10.1016/S0969-8043(98)00153-5 .
- ^ Такач, С.; Шуч, З.; Тарканьи, Ф.; Германн, А.; Сонк, М. (1 января 2003 г.). «Оценка протон-индуцированных реакций на 100 Мо: Новые сечения для производства 99 м Тс и 99 Мо». Журнал радиоаналитической и ядерной химии . 257 (1): 195–201. doi : 10.1023/A:1024790520036 . S2CID 93040978 .
- ^ Селлер, А.; Хоу, X.; Бенар, Ф.; Рут, Т. (2011). «Теоретическое моделирование выходов протонно-индуцированных реакций на природных и обогащенных молибденовых мишенях». Физика в медицине и биологии . 56 (17): 5469–5484. Бибкод : 2011PMB....56.5469C . дои : 10.1088/0031-9155/56/17/002 . ПМИД 21813960 . S2CID 24231457 .
- ^ Швохау 2000 , с. 414.
- ^ Швохау 2000 , стр. 12–27.
- ^ Швохау 2000 , с. 87.
- ^ Джеймс С. Туленко; Дин Шенфельд; Дэвид Хинтенланг; Карл Крейн; Шеннон Риджуэй; Хосе Сантьяго; Чарльз Шир (30 ноября 2006 г.). Университетская исследовательская программа в области робототехники ОТЧЕТ (PDF) (Отчет). Университет Флориды. дои : 10.2172/895620 . Проверено 12 октября 2007 г.
- ^ Швохау 2000 , стр. 87–90.
- ↑ Перейти обратно: Перейти обратно: а б «Технеций (Тс)» . Американские элементы: Компания по науке о материалах . Проверено 24 мая 2024 г.
- ↑ Перейти обратно: Перейти обратно: а б Эмсли 2001 , с. 425.
- ^ «Глава 14, методы разделения» (PDF) . Агентство по охране окружающей среды: 402-b-04-001b-14-final . Агентство по охране окружающей среды США. Июль 2004 г. Архивировано (PDF) из оригинала 8 марта 2014 г. Проверено 4 августа 2008 г.
- ↑ Перейти обратно: Перейти обратно: а б Швохау 2000 , с. 91.
- ^ Десмет, Г.; Миттенар, К. (1986). Технеций в окружающей среде . Спрингер. стр. 392–395. ISBN 978-0-85334-421-6 .
- ^ Швохау 2000 , стр. 371–381.
- ^ Швохау 2000 , с. 40.
Библиография [ править ]
- Эмсли, Дж. (2001). Строительные блоки природы: Путеводитель по элементам от Аризоны . Оксфорд, Англия, Великобритания: Издательство Оксфордского университета. ISBN 978-0-19-850340-8 .
- Гринвуд, штат Нью-Йорк; Эрншоу, А. (1997). Химия элементов (2-е изд.). Оксфорд: Баттерворт-Хайнеманн. ISBN 978-0-7506-3365-9 .
- Хаммонд, ЧР (2004). «Элементы» . Справочник по химии и физике (81-е изд.). ЦРК Пресс. ISBN 978-0-8493-0485-9 .
- Шерри, Эрик (2013). Сказка о семи стихиях . Издательство Оксфордского университета, ISBN 9780195391312.
- Швохау, К. (2000). Технеций: химия и радиофармацевтические применения . Вайнхайм, Германия: Wiley-VCH. ISBN 978-3-527-29496-1 .
Дальнейшее чтение [ править ]
- Чоппин, Г.; Лильензин, Ж.-О. ; Ридберг, Дж. (2002). «Ядерная масса и стабильность» . Радиохимия и ядерная химия (3-е изд.). Баттерворт-Хайнеманн. стр. 41–57. ISBN 978-0-7506-7463-8 .
- Коттон, ФА; Уилкинсон, Г.; Мурильо, Калифорния; Бохманн, М. (1999). Продвинутая неорганическая химия (6-е изд.). John Wiley & Sons, Inc. Нью-Йорк: ISBN 978-0-471-19957-1 .
- Шерри, ER (2007). Таблица Менделеева, ее история и значение . Издательство Оксфордского университета. ISBN 978-0-19-530573-9 .
- Уилсон, Б.Дж., изд. (1966). Радиохимическое руководство (2-е изд.). Технология АЭА. ISBN 978-0-7058-1768-4 .
- EnvironmentalChemistry.com – Технеций
- Нудат 2. Архивировано 28 апреля 2021 г. на диаграмме нуклидов Wayback Machine из Национального центра ядерных данных, Брукхейвенская национальная лаборатория.
Внешние ссылки [ править ]
- Технеций в Периодической таблице видео (Ноттингемский университет)

![{\displaystyle {\ce {^{238}_{92}U ->[{\ce {sf}}] ^{137}_{53}I + ^{99}_{39}Y + 2^{ 1}_{0}н}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/69e432873016029d0ca91cbd92c76fc15631fd66)
![{\displaystyle {\ce {^{99}_{39}Y ->[\beta^-][1.47\,{\ce {s}}] ^{99}_{40}Zr ->[\beta ^-][2.1\,{\ce {s}}] ^{99}_{41}Nb ->[\beta^-][15.0\,{\ce {s}}] ^{99}_{ 42}Mo ->[\beta^-][65.94\,{\ce {h}}] ^{99}_{43}Tc ->[\beta^-][211,100\,{\ce {y} }] ^{99}_{44}Ру}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/33a9d13cb741fa5c8efce11540847d7deac9654b)