Элемент группы 7
| Группа 7 в таблице Менделеева | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| ↓ Период | |||||||||
| 4 | Марганец (Mn) 25 Переходный металл | ||||||||
| 5 | Технеций (Tc) 43 Переходный металл | ||||||||
| 6 | Рений (Ре) 75 Переходный металл | ||||||||
| 7 | Борий (Bh) 107 Переходный металл | ||||||||
Легенда
| |||||||||
Группа 7 , пронумерованная по номенклатуре ИЮПАК , представляет собой группу элементов периодической таблицы . Он содержит марганец (Mn), технеций (Tc), рений (Re) и борий (Bh). Эта группа находится в d-блоке периодической таблицы и, следовательно, является переходными металлами . Эту группу иногда называют группой марганца или семейством марганца по имени ее самого легкого члена; однако сама группа не получила тривиального названия , поскольку принадлежит к более широкой группе переходных металлов.
Элементы группы 7 имеют тенденцию иметь степень окисления основной группы (+7), хотя эта тенденция заметно менее последовательная, чем в предыдущих группах. Как и другие группы, члены этого семейства демонстрируют закономерности в электронных конфигурациях , особенно на внешних оболочках, что приводит к тенденциям в химическом поведении. В природе марганец — довольно распространенный элемент, тогда как рений встречается редко, технеций встречается лишь в следовых количествах, а борий — полностью синтетический материал .
Физические свойства
[ редактировать ]Тенденции в группе 7 следуют, хотя и менее заметно, тенденциям других ранних групп d-блоков и отражают добавление заполненной f-оболочки в ядро при переходе от пятого к шестому периоду. Все элементы группы 7 кристаллизуются в гексагональной плотноупакованной (ГПУ) структуре, за исключением марганца, который кристаллизуется в объемноцентрированной кубической (ОЦК) структуре. Ожидается также, что борий будет кристаллизоваться в структуре ГПУ. [1]
В таблице ниже представлена краткая информация об основных физических свойствах элементов группы 7. Значение, отмеченное вопросительным знаком, является прогнозируемым. [2]
| Имя | Мн, марганец | Тс, технеций | Ре, рений | Бх, борий |
|---|---|---|---|---|
| Температура плавления | 1519 К (1246 °С) | 2430 К (2157 °С) | 3459 К (3186 °С) | Unknown |
| Точка кипения | 2334 К (2061 °С) | 4538 К (4265 °С) | 5903 К (5630 °С) | Unknown |
| Плотность | 7,21 г·см −3 | 11 г·см −3 | 21,02 г·см −3 | 26-27 г·см −3 ? [3] [4] |
| Появление | серебристый металлик | серебристо-серый | серебристо-серый | Unknown |
| Атомный радиус | 127 вечера | 136 вечера | 137 вечера | 128 вечера? [2] |
Химические свойства
[ редактировать ]Как и другие группы, члены этого семейства демонстрируют закономерности в электронной конфигурации , особенно на внешних оболочках:
| С | Элемент | Количество электронов/оболочка |
|---|---|---|
| 25 | марганец | 2, 8, 13, 2 |
| 43 | технеций | 2, 8, 18, 13, 2 |
| 75 | рений | 2, 8, 18, 32, 13, 2 |
| 107 | борий | 2, 8, 18, 32, 32, 13, 2 |
Все члены группы с готовностью изображают степень окисления своей группы +7, и это состояние становится более стабильным по мере нисхождения группы. Технеций также демонстрирует стабильное состояние +4, тогда как рений демонстрирует стабильные состояния +4 и +3.
Таким образом, Борий также может проявлять и эти низшие состояния. Более высокая степень окисления +7 с большей вероятностью существует в оксианионах, таких как перборат, BhO 4 − , аналог более легкого перманганата , пертехнетата и перрената . Тем не менее, борий(VII), вероятно, нестабилен в водном растворе и, вероятно, будет легко восстановлен до более стабильного бория(IV). [5]
Соединения
[ редактировать ]Оксиды
[ редактировать ]Марганец
[ редактировать ]
разнообразные MnO , Mn3O4 , Mn2O3 и Mn2O7 , MnO2 , MnO3 образует оксиды . : Марганец Оксид марганца(II) представляет собой неорганическое соединение, образующее зеленые кристаллы. Как и многие монооксиды, MnO имеет структуру каменной соли , в которой катионы и анионы координированы октаэдрически. Также, как и многие оксиды, оксид марганца(II) часто нестехиометричен : его состав может варьироваться от MnO до MnO 1,045 . [6] Оксид марганца (II, III) образуется при нагревании любого оксида марганца на воздухе выше 1000 ° C. [6] Значительные исследования были сосредоточены на производстве нанокристаллического Mn 3 O 4 и различных синтезах, включающих окисление Mn. II или уменьшение Mn МЫ . [7] [8] [9] Оксид марганца(III) отличается от многих других оксидов переходных металлов тем, что он не имеет структуры корунда ( Al 2 O 3 ). [6] Обычно выделяют две формы: α-Mn 2 O 3 и γ-Mn 2 O 3 . [10] о форме высокого давления со структурой CaIrO 3 . хотя сообщалось также [11] Оксид марганца (IV) представляет собой черноватое или коричневое твердое вещество, встречающееся в природе в виде минерала пиролюзита , который является основной марганцевой рудой и компонентом марганцевых конкреций . Основное применение MnO 2 — это сухие батареи , такие как щелочные батареи и углеродно-цинковые батареи . [6] Оксид марганца (VII) в кристаллической форме имеет темно-зеленый цвет. Жидкость имеет зеленый цвет в отраженном свете и красный в проходящем свете. [12] Он растворим в четыреххлористом углероде и разлагается при контакте с водой.
Технеций
[ редактировать ]
Основными оксидами технеция являются оксид технеция (IV) и оксид технеция (VII) . Оксид технеция(IV) был впервые получен в 1949 году путем электролиза раствора пертехнетата аммония под гидроксидом аммония . Его часто использовали для отделения технеция от молибдена и рения. [13] [14] [15] Более эффективными способами являются восстановление пертехнетата аммония металлическим цинком и соляной кислотой , хлоридом олова , гидразином , гидроксиламином , аскорбиновой кислотой , [14] гидролизом гексахлортехнетата калия [16] или разложением пертехнетата аммония при 700 °C в инертной атмосфере. [13] [17] [18] Он реагирует с кислородом с образованием оксида технеция (VII) при 450 ° C.
Оксид технеция(VII) можно получить непосредственно окислением технеция при 450-500 °С. [19] Это редкий пример молекулярного бинарного оксида металла. Другими примерами являются оксид рутения (VIII) и оксид осмия (VIII) . Он принимает центросимметричную битетраэдрическую структуру с общими углами, в которой концевые и мостиковые связи Tc-O составляют 167 пм и 184 пм соответственно, а угол Tc-O-Tc составляет 180 °. [20]
Рений
[ редактировать ]Основными оксидами рения являются оксид рения (IV) и оксид рения (VII) . Оксид рения(IV) представляет собой кристаллическое твердое вещество от серого до черного цвета, которое можно получить путем сопропорционирования . [21] При высоких температурах он подвергается диспропорции . Это лабораторный реагент, который можно использовать в качестве катализатора . Он принимает рутиловую структуру . образует перренаты С щелочной перекисью водорода и кислотами-окислителями . [22] В расплавленном гидроксиде натрия образуется ренат натрия: [23]
- 2 NaOH + ReO 2 → Na 2 ReO 3 + H 2 O
Оксид рения(VII) может образовываться при окислении рения, его оксидов или сульфидов при температуре 500–700 °C на воздухе. [24] Растворяется в воде с образованием перреновой кислоты . При нагревании Re 2 O 7 образуется оксид рения(IV), о чем свидетельствует появление темно-синего окрашивания. [25] В твердой форме Re 2 O 7 состоит из чередующихся октаэдрических и тетраэдрических центров Re. Он является сырьем для всех соединений рения, поскольку представляет собой летучую фракцию, получаемую при обжиге вмещающей руды. [26]
Рений, помимо степеней окисления +4 и +7, образует еще и триоксид . Его можно получить восстановлением оксида рения(VII) монооксидом углерода при 200°С или элементарным рением при 4000°С. [27] Его также можно восстановить диоксаном . [28] Это красное твердое вещество с металлическим блеском, внешне напоминающее медь , и является единственным стабильным триоксидом элементов 7-й группы.
Галиды
[ редактировать ]Марганец
[ редактировать ]Марганец может образовывать соединения в степенях окисления +2, +3 и +4. Соединения марганца(II) часто представляют собой твердые вещества светло-розового цвета. Как и некоторые другие дифториды металлов, MnF 2 кристаллизуется в рутильной структуре, имеющей октаэдрические центры Mn. [29] его используют при производстве специальных видов стекла и лазеров . [30] Скакхит — это природная безводная форма хлорида марганца (II). [31] Единственным другим известным в настоящее время минералом, систематизированным как хлорид марганца, является кемпит — представитель группы атакамитов, группы гидроксид-хлоридов. [32] Его можно использовать вместо палладия в реакции Стилле , в которой два атома углерода соединяются с использованием оловоорганического соединения . [33] Его можно использовать в качестве розового пигмента или в качестве источника ионов марганца или йодида. Его часто используют в светотехнической промышленности. [33]
Технеций
[ редактировать ]Известны следующие бинарные (содержащие всего два элемента) галогениды технеция: TcF 6 , TcF 5 , TcCl 4 , TcBr 4 , TcBr 3 , α-TcCl 3 , β-TcCl 3 , TcI 3 , α-TcCl 2 и β-. ТсСl 2 . Степени окисления варьируются от Tc(VI) до Tc(II). Галогениды технеция имеют различные типы структуры, такие как молекулярные октаэдрические комплексы, вытянутые цепи, слоистые листы и металлические кластеры, расположенные в трехмерной сетке. [34] [35] Эти соединения получаются путем объединения металла и галогена или менее прямыми реакциями.
TcCl 4 получают хлорированием металлического Tc или Tc 2 O 7. при нагревании TcCl 4 дает соответствующие хлориды Tc(III) и Tc(II). [35]
- TcCl 4 → α-TcCl 3 + 1/2 Cl 2
- TcCl 3 → β-TcCl 2 + 1/2 Cl 2
Структура TcCl 4 состоит из бесконечных зигзагообразных цепочек октаэдров TcCl 6, имеющих общие ребра . Он изоморфен тетрахлоридам переходных металлов циркония , гафния и платины . [35]

Существуют две полиморфные модификации трихлорида технеция : α- и β-TcCl 3 . Полиморф α также обозначается как Tc 3 Cl 9 . Он принимает конфациальную биооктаэдрическую структуру . [36] Его получают обработкой хлорацетата Tc 2 (O 2 CCH 3 ) 4 Cl 2 HCl. Как и Re 3 Cl 9 , структура α-полиморфа состоит из треугольников с короткими ММ-расстояниями. β-TcCl 3 имеет октаэдрические центры Tc, которые организованы парами, как это видно также для трихлорида молибдена . TcBr 3 не принимает структуру ни одной трихлоридной фазы. Вместо этого он имеет структуру трибромида молибдена , состоящую из цепочек конфациальных октаэдров с чередующимися короткими и длинными контактами Tc—Tc. TcI 3 имеет ту же структуру, что и высокотемпературная фаза TiI 3 , и представляет собой цепочки конфациальных октаэдров с равными контактами Tc—Tc. [35]
Известно несколько анионных галогенидов технеция. Бинарные тетрагалогениды можно преобразовать в гексагалогениды [TcX 6 ] 2− (X = F, Cl, Br, I), которые принимают октаэдрическую молекулярную геометрию . [37] Более восстановленные галогениды образуют анионные кластеры со связями Tc–Tc. Аналогичная ситуация и для родственных элементов Mo, W, Re. Эти кластеры имеют ядерность Tc 4 , Tc 6 , Tc 8 и Tc 13 . Более стабильные кластеры Tc 6 и Tc 8 имеют форму призмы, в которой вертикальные пары атомов Tc соединены тройными связями, а плоские атомы - одинарными. Каждый атом технеция образует шесть связей, а оставшиеся валентные электроны могут быть насыщены одним аксиальным и двумя мостиковыми атомами галогена лиганда, такими как хлор или бром . [38]
Рений
[ редактировать ]Наиболее распространенными хлоридами рения являются ReCl 6 , ReCl 5 , ReCl 4 и ReCl 3 . [6] В структурах этих соединений часто наблюдаются обширные связи Re-Re, характерные для этого металла в степенях окисления ниже VII. Соли [Re 2 Cl 8 ] 2− имеют четырехкратную связь металл-металл. Хотя самый высокий уровень хлорида рения содержит Re(VI), фтор дает d 0 Re(VII) Производное гептафторида рения . Хорошо известны также бромиды и иодиды рения.
Подобно вольфраму и молибдену, с которыми он имеет сходство по химическому составу, рений образует множество оксигалогенидов . Оксихлориды наиболее распространены и включают ReOCl 4 , ReOCl 3 .
Металлоорганические соединения
[ редактировать ]Марганец
[ редактировать ]Впервые марганцевоорганические соединения были описаны в 1937 году Гилманом и Бэйли, которые описали реакцию фениллития и йодида марганца (II) с образованием йодида фенилмарганца (PhMnI) и дифенилмарганца (Ph 2 Mn). [39]
Следуя этому прецеденту, другие марганцево-галогениды могут быть получены путем алкилирования хлорида марганца (II) , бромида марганца (II) и йодида марганца (II) . Йодид марганца привлекателен тем, что безводное соединение можно получить in situ из марганца и йода в эфире . Типичными алкилирующими агентами являются литийорганические или магнийорганические соединения.
Химия металлоорганических соединений Mn(II) необычна среди переходных металлов из-за высокого ионного характера связи Mn(II)-C. [40] По реакционной способности марганцевоорганические соединения можно сравнить с магнийорганическими и цинкорганическими соединениями . Электроотрицательность ) Mn (1,55) сравнима с электроотрицательностью Mg (1,31) и Zn (1,65), что делает атом углерода (EN = 2,55 нуклеофильным . Восстановительный потенциал Mn также занимает промежуточное положение между Mg и Zn.
Технеций
[ редактировать ]
Технеций образует разнообразные координационные комплексы с органическими лигандами. Многие из них были хорошо исследованы из-за их значимости для ядерной медицины . [41]
Технеций образует разнообразные соединения со связями Tc–C, т. е. технецийорганические комплексы. Выдающимися представителями этого класса являются комплексы с CO, ареном и циклопентадиенильными лигандами. [42] Бинарный карбонил Tc 2 (CO) 10 представляет собой белое летучее твердое вещество. [43] В этой молекуле два атома технеция связаны друг с другом; каждый атом окружен октаэдрами из пяти карбонильных лигандов. Длина связи между атомами технеция 303 пм, [44] [45] значительно больше, чем расстояние между двумя атомами металлического технеция (272 пм). Подобные карбонилы образуются родственными технецию марганцем и рением. [46] Интерес к технецийорганическим соединениям обусловлен также применением их в ядерной медицине . [42] Необычный для карбонилов других металлов, Tc образует аквакарбонильные комплексы, наиболее заметными из которых являются [Tc(CO) 3 (H 2 O) 3 ] + . [42]
Рений
[ редактировать ]Декакарбонил дирения - наиболее распространенный элемент в химии органорения. натрия Его восстановление амальгамой дает Na[Re(CO) 5 ] с рением в формальной степени окисления -1. [47] Декакарбонил дирения можно окислить бромом до бромпентакарбонилрения(I) : [48]
- Re 2 (CO) 10 + Br 2 → 2 Re(CO) 5 Br
Восстановление этого пентакарбонила цинком и уксусной кислотой дает пентакарбонилгидридорений : [49]
- Re(CO) 5 Br + Zn + HOAc → Re(CO) 5 H + ZnBr(OAc)
Триоксид метилрения («МТО»), CH 3 ReO 3 — летучее бесцветное твердое вещество, использовавшееся в качестве катализатора в некоторых лабораторных экспериментах. Его можно получить многими способами, типичным методом является реакция Re 2 O 7 и тетраметилолова :
- Re 2 O 7 + (CH 3 ) 4 Sn → CH 3 ReO 3 + (CH 3 ) 3 SnOReO 3
Известны аналогичные алкильные и арильные производные. МТО катализирует окисление перекисью водорода . Концевые алкины дают соответствующую кислоту или сложный эфир, внутренние алкины дают дикетоны, а алкены дают эпоксиды. МТО также катализирует превращение альдегидов и диазоалканов в алкены. [50]
Полиоксометаллаты
[ редактировать ]Полиоксотехнетат (полиоксометаллат технеция) содержит как Tc(V), так и Tc(VII) в соотношении 4:16 и получается в виде гидроксониевой соли [H 7 O 3 ] 4 [Tc 20 O 68 ]·4H 2 O путем концентрирования HTcO 4 . Раствор [51] Первым эмпирически выделенным полиоксоренатом был белый [Re 4 O 15 ] 2− и содержал Re(VII) как в октаэдрической, так и в тетраэдрической координации. [52]
История
[ редактировать ]Марганец
[ редактировать ]Диоксид марганца, которого много в природе, издавна использовался в качестве пигмента. Наскальные рисунки в Гаргасе возрастом от 30 000 до 24 000 лет выполнены из минеральной формы пигментов MnO 2 . [53] Соединения марганца использовались египетскими и римскими стеклодувами для придания или удаления цвета стекла. [54] Использование его в качестве «мыла для стеклоделов» продолжалось в Средние века до наших дней, и это заметно по стеклу 14-го века из Венеции . [55]
Технеций и рений
[ редактировать ]Рений ( лат . Rhenus означает « Рейн ») [56] был последним из открытых элементов, имеющих стабильный изотоп (другие новые элементы, обнаруженные с тех пор в природе, такие как франций , радиоактивны). [57] Существование еще не открытого элемента в этой позиции периодической таблицы было впервые предсказано Дмитрием Менделеевым . Другая расчетная информация была получена Генри Мозли в 1914 году. [58] В 1908 году японский химик Масатака Огава объявил, что открыл 43-й элемент, и назвал его ниппонием (Np) в честь Японии ( Nippon по-японски). На самом деле у него был рений (75-й элемент), а не технеций . [59] [60] Символ Np позже использовался для элемента нептуния , а название «нихоний», также названное в честь Японии , вместе с символом Nh, позже использовалось для элемента 113 . Элемент 113 также был открыт группой японских ученых и назван в честь работы Огавы. [61]
Рений был заново открыт Уолтером Ноддаком , Идой Ноддак и Отто Бергом в Германии . В 1925 году они сообщили, что обнаружили этот элемент в платиновой руде и минерале колумбите . Они также нашли рений в гадолините и молибдените . [62] В 1928 году им удалось извлечь 1 г элемента, переработав 660 кг молибденита. [63] В 1968 году было подсчитано, что 75% металлического рения в Соединенных Штатах использовалось для исследований и разработки тугоплавких металлических сплавов. С этого момента прошло несколько лет, прежде чем суперсплавы стали широко использоваться. [64] [65]
Открытие 43- го элемента было окончательно подтверждено в эксперименте 1937 года в Университете Палермо на Сицилии Карло Перье и Эмилио Сегре . [66] В середине 1936 года Сегре посетил Соединенные Штаты, сначала Колумбийский университет в Нью-Йорке, а затем Национальную лабораторию Лоуренса Беркли в Калифорнии. Он убедил циклотрона изобретателя Эрнеста Лоуренса позволить ему забрать некоторые выброшенные детали циклотрона, которые стали радиоактивными . Лоуренс отправил ему по почте молибденовую фольгу, которая была частью дефлектора циклотрона. [67]
борий
[ редактировать ]Две группы заявили об открытии элемента бория . О наличии бория впервые сообщила в 1976 году советская исследовательская группа под руководством Юрия Оганесяна , в ходе которой мишени из висмута-209 и свинца -208 бомбардировались ускоренными ядрами хрома -54 и марганца -55 соответственно. [68] Были замечены две активности: одна с периодом полураспада от одной до двух миллисекунд, а другая с периодом полураспада примерно пять секунд. Поскольку соотношение интенсивностей этих двух активностей было постоянным на протяжении всего эксперимента, было высказано предположение, что первое происходит от изотопа бория -261, а второе - от его дочернего дубния -257. Позже изотоп дубния был исправлен до дубния-258, период полураспада которого действительно составляет пять секунд (период полураспада дубния-257 составляет одну секунду); однако период полураспада, наблюдаемый для его родителя, намного короче, чем период полураспада, наблюдавшийся позже при окончательном открытии бория в Дармштадте в 1981 году. Рабочая группа IUPAC / IUPAP по трансфермию (TWG) пришла к выводу, что, хотя дубний-258, вероятно, был обнаружен в этом эксперименте доказательства образования родительского бория-262 не были достаточно убедительными. [69]
В 1981 году немецкая исследовательская группа во главе с Питером Армбрустером и Готфридом Мюнценбергом в Центре исследований тяжелых ионов GSI имени Гельмгольца (GSI Helmholtzzentrum für Schwerionenforschung) в Дармштадте бомбардировала мишень из висмута-209 ускоренными ядрами хрома-54, чтобы произвести 5 атомов изотоп борий-262: [70]
- 209
83 Би
+ 54
24 Кр
→ 262
107 бат.ч.
+
н
Это открытие было дополнительно подтверждено детальными измерениями цепи альфа-распада образующихся атомов бория до ранее известных изотопов фермия и калифорния . Рабочая группа IUPAC / IUPAP Transfermium (TWG) признала сотрудничество GSI официальными первооткрывателями в своем отчете 1992 года. [69]
Возникновение и производство
[ редактировать ]Марганец
[ редактировать ]Марганец составляет около 1000 ppm (0,1%) земной коры , занимая 12-е место по распространенности среди элементов земной коры. [71] Почва содержит 7–9000 частей на миллион марганца, в среднем 440 частей на миллион. [71] В атмосфере содержится 0,01 мкг/м 3 . [71] Manganese occurs principally as pyrolusite ( MnO 2 ), braunite (Mn 2+ Мин. 3+ 6 )(SiO 12 ), [72] псиломелан (Ba,H 2 O) 2 Mn 5 O 10 и в меньшей степени родохрозит ( MnCO 3 ).

Наиболее важной марганцевой рудой является пиролюзит ( MnO 2 ). Другие экономически важные марганцевые руды обычно имеют близкое пространственное родство с железными рудами, такими как сфалерит . [74] [75] Ресурсы суши велики, но распределены неравномерно. Около 80% известных мировых ресурсов марганца находятся в Южной Африке; другие важные месторождения марганца находятся в Украине, Австралии, Индии, Китае, Габоне и Бразилии. [73] По оценкам 1978 года, на дне океана находится 500 миллиардов тонн марганцевых конкреций . [76] Попытки найти экономически выгодные методы добычи марганцевых конкреций были прекращены в 1970-х годах. [77]
В Южной Африке большинство выявленных месторождений расположены недалеко от Хотазеля в Северо-Капской провинции , их запасы на 2011 год оцениваются в 15 миллиардов тонн. В 2011 году Южная Африка произвела 3,4 миллиона тонн, превзойдя все другие страны. [78]
Марганец в основном добывают в Южной Африке, Австралии, Китае, Габоне, Бразилии, Индии, Казахстане, Гане, Украине и Малайзии. [79]
Для производства ферромарганца марганцевую руду смешивают с железной рудой и углеродом, а затем восстанавливают либо в доменной печи, либо в электродуговой печи. [80] Полученный ферромарганец имеет содержание марганца от 30 до 80%. [74] Чистый марганец, используемый для производства безжелезистых сплавов, получают путем выщелачивания марганцевой руды серной кислотой и последующего электролиза . [81]
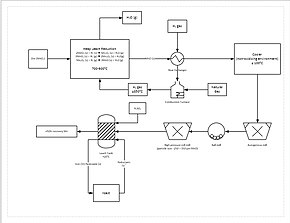
Более прогрессивный процесс добычи включает прямое восстановление (низкосортной) марганцевой руды при кучном выщелачивании. Это делается путем просачивания природного газа через дно кучи; природный газ обеспечивает тепло (должно быть не менее 850 °C) и восстановитель (окись углерода). Это превращает всю марганцевую руду в оксид марганца (MnO), который является выщелачиваемой формой. Затем руда проходит через контур измельчения , чтобы уменьшить размер частиц руды до 150–250 мкм, увеличивая площадь поверхности и способствуя выщелачиванию. Затем руду добавляют в резервуар для выщелачивания серной кислоты и двухвалентного железа (Fe 2+ ) в соотношении 1,6:1. Железо реагирует с диоксидом марганца (MnO 2 ) с образованием оксида-гидроксида железа(III) (FeO(OH)) и элементарного марганца (Mn):
Этот процесс дает около 92% извлечения марганца. Для дальнейшей очистки марганец затем можно отправить на установку электролиза. [82]
В 1972 году ЦРУ « проект Азориан » через миллиардера Говарда Хьюза заказал судно «Хьюз Гломар Эксплорер» под предлогом добычи марганцевых конкреций со дна моря. [83] Это вызвало всплеск активности по сбору марганцевых конкреций, что на самом деле было непрактично. Настоящая миссия Hughes Glomar Explorer заключалась в подъеме затонувшей советской подводной лодки К-129 с целью восстановления советских кодовых книг. [84]
Богатые ресурсы марганца в виде конкреций Mn, обнаруженных на дне океана. [85] [86] Эти узелки, состоящие на 29% из марганца, [87] расположены вдоль дна океана , и потенциальные последствия добычи этих конкреций исследуются. Из-за добычи конкреций могут возникнуть физические, химические и биологические воздействия на окружающую среду, которые нарушают морское дно и вызывают образование шлейфов отложений. В состав этой взвеси входят металлы и неорганические питательные вещества, что может привести к загрязнению придонных вод растворенными токсичными соединениями. Конкреции Mn также являются пастбищами, жилым пространством и защитой эндо- и эпифауны. Когда эти узелки удаляются, эти системы напрямую затрагиваются. В целом это может привести к тому, что виды покинут этот район или полностью вымрут. [88] До начала самой добычи аффилированные с Организацией Объединенных Наций органы и компании, спонсируемые государством, проводят исследования в попытке полностью понять воздействие на окружающую среду в надежде смягчить это воздействие. [89]
Технеций
[ редактировать ]Технеций был создан путем бомбардировки молибдена атомов дейтронами , ускоренными с помощью устройства, называемого циклотроном . Технеций естественным образом встречается в земной коре в минимальных концентрациях около 0,003 частей на триллион. Технеций настолько редок, потому что полураспада период 97 Тс и 98 Tc составляет всего 4,2 миллиона лет. прошло более тысячи таких периодов С момента образования Земли , поэтому вероятность выживания даже одного атома первичного технеция фактически равна нулю. Однако небольшие количества существуют в виде продуктов спонтанного деления в урановых рудах . Килограмм урана содержит примерно 1 нанограмм (10 −9 г) эквивалент десяти триллионам атомов технеция. [90] [91] [92] Некоторые красные гиганты спектральных классов S-, M- и N содержат спектральную линию поглощения, указывающую на присутствие технеция. [93] [94] Эти красные гиганты неофициально известны как звезды технеция .
Рений
[ редактировать ]
Рений — один из самых редких элементов в земной коре , его средняя концентрация составляет 1 миллиардную долю; [6] [95] другие источники указывают количество 0,5 частей на миллиард, что делает его 77-м по распространенности элементом в земной коре. [96] Рений, вероятно, не встречается в природе в свободном виде (возможность его природного происхождения не установлена), но встречается в количествах до 0,2%. [6] в минерале молибдените (который в основном представляет собой дисульфид молибдена ), основном коммерческом источнике, хотя были обнаружены единичные образцы молибденита с содержанием до 1,88%. [97] Чили обладает крупнейшими в мире запасами рения, частью месторождений медной руды и по состоянию на 2005 год была ведущим производителем. [98] Лишь недавно первый минерал (в 1994 году) был обнаружен и описан рения — сульфид рения (ReS 2 ), конденсирующийся из фумаролы вулкана Кудрявый , остров Итуруп , на Курильских островах . [99] Кудрявый сбрасывает до 20–60 кг рения в год, преимущественно в виде дисульфида рения. [100] [101] Этот редкий минерал, названный рениетом , пользуется высокой ценой среди коллекционеров. [102]

Большая часть добываемого рения поступает из молибден -порфировых месторождений. [103] Эти руды обычно содержат от 0,001% до 0,2% рения. [6] Обжиг руды улетучивает оксиды рения. [97] Оксид рения(VII) и перреневая кислота легко растворяются в воде; их выщелачивают из дымовой пыли и газов, экстрагируют путем осаждения хлоридом калия или аммония в виде перренатных солей и очищают перекристаллизацией . [6] Общий объем мирового производства составляет от 40 до 50 тонн в год; основные производители находятся в Чили, США, Перу и Польше. [104] Переработка отработанного катализатора Pt-Re и специальных сплавов позволяет извлекать еще 10 тонн в год. Цены на металл быстро выросли в начале 2008 года: со 1000–2000 долларов за кг в 2003–2006 годах до более 10 000 долларов в феврале 2008 года. [105] [106] Металлическую форму получают восстановлением перрената аммония водородом : при высоких температурах [25]
- 2 NH 4 ReO 4 + 7 H 2 → 2 Re + 8 H 2 O + 2 NH 3
- Существуют технологии попутного извлечения рения из продуктивных растворов подземного выщелачивания урановых руд. [107]
борий
[ редактировать ]Борий — синтетический элемент, не встречающийся в природе. Было синтезировано очень мало атомов, а также из-за его радиоактивности проведено лишь ограниченное исследование. Борий производится только в ядерных реакторах и никогда не выделялся в чистом виде.
Приложения
[ редактировать ]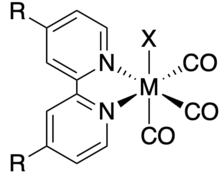
изомер Лицевой из 2,2'-бипиридилтрикарбонилгалогенидных комплексов рения и марганца широко исследовался в качестве катализаторов электрохимического восстановления диоксида углерода -за их высокой селективности и стабильности. Их обычно обозначают M(R-bpy)(CO) 3 X, где M = Mn, Re; R-bpy = 4,4'-дизамещенный 2,2'-бипиридин ; и X = Cl, Br.
Марганец
[ редактировать ]Редкость рения сместила исследования в сторону марганцевой версии этих катализаторов как более устойчивой альтернативы. [108] Первые сообщения о каталитической активности Mn(R-bpy)(CO) 3 Br в отношении восстановления CO 2 поступили от Шардон-Нобла и его коллег в 2011 году. [109] По сравнению с аналогами Re Mn(R-bpy)(CO) 3 Br проявляет каталитическую активность при меньших перенапряжениях. [110]
Каталитический механизм Mn(R-bpy)(CO) 3 X сложен и зависит от стерического профиля бипиридинового лиганда. Когда R не является объемистым, катализатор димеризуется с образованием [Mn(R-bpy)(CO) 3 ] 2 перед образованием активных частиц. Однако когда R является объемным, комплекс образует активные частицы без димеризации, уменьшая перенапряжение восстановления CO 2 на 200-300 мВ. В отличие от Re(R-bpy)(CO) 3 X, Mn(R-bpy)(CO) 3 X восстанавливает CO 2 только в присутствии кислоты. [110]
Технеций
[ редактировать ]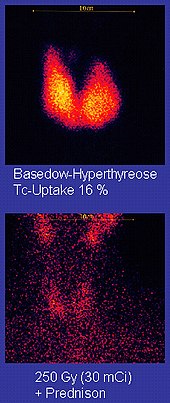
Технеций-99m («м» указывает на то, что это метастабильный ядерный изомер) используется в медицинских испытаниях радиоактивных изотопов . Например, технеций-99m — это радиоактивный индикатор , который отслеживает медицинское оборудование для визуализации в организме человека. [90] [111] [112] Он хорошо подходит для этой роли, поскольку излучает легко обнаруживаемые 140 кэВ гамма-лучи с энергией , а его период полураспада составляет 6,01 часа (это означает, что около 94% его распадается до технеция-99 за 24 часа). [113] Химия технеция позволяет связывать его с множеством биохимических соединений, каждое из которых определяет, как он метаболизируется и откладывается в организме, и этот единственный изотоп можно использовать для множества диагностических тестов. более 50 распространенных радиофармпрепаратов На основе технеция-99m создано , предназначенных для визуализации и функциональных исследований головного мозга , сердечной мышцы, щитовидной железы , легких , печени , желчного пузыря , почек , скелета , крови и опухолей . [114] Технеций-99m также используется в радиовизуализации. [115]
Долгоживущий изотоп технеций-95m с периодом полураспада 61 день используется в качестве радиоактивного индикатора для изучения движения технеция в окружающей среде, а также в растительных и животных системах. [116]
Технеций-99 почти полностью распадается в результате бета-распада, испуская бета-частицы с постоянными низкими энергиями и без сопутствующих гамма-лучей. Более того, его длительный период полураспада означает, что это выделение со временем уменьшается очень медленно. Его также можно извлечь до высокой химической и изотопной чистоты из радиоактивных отходов. По этим причинам это стандартный бета-излучатель Национального института стандартов и технологий (NIST) и используется для калибровки оборудования. [117] Технеций-99 также был предложен для использования в оптоэлектронных устройствах и наноразмерных ядерных батареях . [118]
Подобно рению и палладию , технеций может служить катализатором . В таких процессах, как дегидрирование изопропилового спирта , он является гораздо более эффективным катализатором, чем рений или палладий. Однако его радиоактивность является серьезной проблемой при безопасном каталитическом применении. [119]
Когда сталь погружают в воду, добавление небольшой концентрации (55 ppm в воду ) пертехнетата калия (VII) защищает сталь от коррозии, даже если температура повышается до 250 ° C (523 K). [120] По этой причине пертехнетат использовался в качестве ингибитора анодной коррозии стали, хотя радиоактивность технеция создает проблемы, которые ограничивают его применение автономными системами. [121] В то время как (например) CrO 2−
4 также может ингибировать коррозию, для этого требуется концентрация в десять раз выше. В одном эксперименте образец углеродистой стали выдерживался в водном растворе пертехнетата в течение 20 лет и до сих пор не подвергся коррозии. [120] Механизм, с помощью которого пертехнетат предотвращает коррозию, не совсем понятен, но, по-видимому, включает обратимое образование тонкого поверхностного слоя ( пассивацию ). Одна теория утверждает, что пертехнетат реагирует с поверхностью стали, образуя слой диоксида технеция , который предотвращает дальнейшую коррозию; тот же эффект объясняет, как можно использовать порошок железа для удаления пертехнетата из воды. Эффект быстро исчезает, если концентрация пертехнетата падает ниже минимальной концентрации или если добавляется слишком высокая концентрация других ионов. [122]
Как уже отмечалось, радиоактивная природа технеция (3 МБк/л в необходимых концентрациях) делает такую защиту от коррозии практически во всех ситуациях непрактичной. Тем не менее, защита от коррозии пертехнетат-ионами была предложена (но так и не была принята) для использования в реакторах с кипящей водой . [122]
Рений
[ редактировать ]Каталитическая активность Re(bpy)(CO) 3 Cl в отношении восстановления углекислого газа была впервые изучена Леном и соавт. [123] и Мейер и др. [124] в 1984 и 1985 годах соответственно. Комплексы Re(R-bpy)(CO) 3 X производят CO исключительно за счет CO 2 восстановления с фарадеевской эффективностью , близкой к 100%, даже в растворах с высокими концентрациями воды или кислот Бренстеда . [108]
Каталитический механизм Re(R-bpy)(CO) 3 X включает двукратное восстановление комплекса и потерю лиганда X с образованием пятикоординатной активной частицы, которая связывает CO 2 . Эти комплексы будут снижать содержание CO 2 как в присутствии дополнительной кислоты, так и без нее; однако присутствие кислоты увеличивает каталитическую активность. [108] высокая селективность этих комплексов к восстановлению CO 2 по сравнению с конкурирующей реакцией выделения водорода показали, что Исследования теории функционала плотности связана с более быстрой кинетикой связывания CO 2 по сравнению с H. + привязка. [110]
борий
[ редактировать ]Борий — синтетический элемент, слишком радиоактивный, чтобы его можно было использовать в чем-либо.
Токсичность и меры предосторожности
[ редактировать ]Соединения марганца менее токсичны, чем соединения других распространенных металлов, таких как никель и медь . [125] Однако воздействие марганцевой пыли и паров не должно превышать предельное значение в 5 мг/м. 3 даже на короткие периоды времени из-за уровня его токсичности. [126] Отравление марганцем связано с нарушением моторики и когнитивными расстройствами. [127]
Технеций обладает низкой химической токсичностью. Например, у крыс, которые потребляли до 15 мкг технеция-99 на грамм пищи в течение нескольких недель, не было обнаружено существенных изменений в формуле крови, массе тела и органов, а также в потреблении пищи. [128] В организме технеций быстро превращается в стабильный TcO. −
Ион 4 , который хорошо растворим в воде и быстро выводится из организма. Радиологическая токсичность технеция (на единицу массы) зависит от соединения, типа излучения рассматриваемого изотопа и периода полураспада изотопа. [129] Однако он радиоактивен, поэтому со всеми изотопами необходимо обращаться осторожно. Основная опасность при работе с технецием — вдыхание пыли; такое радиоактивное загрязнение легких может представлять значительный риск развития рака. Для большинства работ осторожного обращения в вытяжном шкафу достаточно , перчаточный ящик не требуется. [130]
О токсичности рения и его соединений известно очень мало, поскольку они используются в очень небольших количествах. Растворимые соли, такие как галогениды или перренаты рения, могут быть опасными из-за элементов, отличных от рения, или из-за самого рения. [131] Лишь несколько соединений рения были проверены на острую токсичность; Двумя примерами являются перренат калия и трихлорид рения, которые вводили крысам в виде раствора. Перренат имел значение LD 50 2800 мг/кг через семь дней (это очень низкая токсичность, аналогичная токсичности поваренной соли), а трихлорид рения показал LD 50 280 мг/кг. [132]
Биологическая роль
[ редактировать ]Из элементов 7 группы только марганец имеет значение в организме человека. Это важное микроэлементное вещество: в организме содержится около 10 миллиграммов в любой момент времени . Он присутствует в качестве кофермента в биологических процессах, которые включают метаболизм макронутриентов, формирование костей и от свободных радикалов системы защиты . Это важнейший компонент десятков белков и ферментов. [133] Марганец в организме человека сосредоточен в основном в костях, а остальная часть в мягких тканях сосредоточена в печени и почках. [134] В человеческом мозге марганец связан с металлопротеинами марганца , особенно с глутаминсинтетазой в астроцитах . [135] Технеций, рений и борий не имеют известной биологической роли. Однако технеций используется в радиовизуализации.
Ссылки
[ редактировать ]- ^ Эстлин, А.; Витос, Л. (2011). «Изначальный расчет структурной устойчивости 6d-переходных металлов». Физический обзор B . 84 (11): 113104. Бибкод : 2011PhRvB..84k3104O . дои : 10.1103/PhysRevB.84.113104 .
- ^ Jump up to: а б Хоффман, Дарлин К.; Ли, Диана М.; Першина, Валерия (2006). «Трансактиниды и элементы будущего». В Морссе; Эдельштейн, Норман М.; Фугер, Жан (ред.). Химия актинидных и трансактинидных элементов (3-е изд.). Дордрехт, Нидерланды: Springer Science+Business Media . ISBN 1-4020-3555-1 .
- ^ Гьянчандани, Джиоти; Сикка, Словакия (10 мая 2011 г.). «Физические свойства элементов 6 d-серии из теории функционала плотности: близкое сходство с более легкими переходными металлами». Физический обзор B . 83 (17): 172101. doi : 10.1103/PhysRevB.83.172101 .
- ^ Крац; Лизер (2013). Ядерная и радиохимия: основы и приложения (3-е изд.). п. 631.
- ^ Химия актинидных и трансактинидных элементов (3-е изд.). Дордрехт: Спрингер. 2006. ISBN 978-1-4020-3555-5 .
- ^ Jump up to: а б с д и ж г час я Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Наностержни гаусманита Mn 3 O 4 : синтез, характеристика и магнитные свойства Jin Du et al. Нанотехнологии, (2006), 17 4923-4928, дои : 10.1088/0957-4484/17/19/024
- ^ Одностадийный синтез наночастиц Mn 3 O 4 : структурное и магнитное исследование Васкес-Олмос А., Редон Р., Родригес-Гатторно Г., Мата-Самора М.Э., Моралес-Лил Ф., Фернандес-Осорио А.Л., Санигер Дж.М. Журнал Коллоид и интерфейсная наука, 291, 1, (2005), 175-180. doi : 10.1016/j.jcis.2005.05.005
- ^ Сунь, Сяомин; Лю, Цзюньфэн; Ли, Ядун (20 февраля 2006 г.). «Использование микросфер углеродистого полисахарида в качестве шаблонов для изготовления полых сфер из оксида металла» . Химия - Европейский журнал . 12 (7): 2039–2047. дои : 10.1002/chem.200500660 . ISSN 0947-6539 .
- ^ Уэллс А.Ф. (1984) Структурная неорганическая химия, 5-е издание Oxford Science Publications ISBN 0-19-855370-6
- ^ Фазовый переход высокого давления в Mn 2 O 3 в фазу типа CaIrO 3 Сантильян, Дж.; Шим, Южно-Американский геофизический союз, осеннее собрание 2005 г., тезисы № MR23B-0050.
- ^ Х. Люкс (1963). «Оксид марганца(VII)». В Г. Брауэре (ред.). Справочник по препаративной неорганической химии, 2-е изд . Том. 1. Нью-Йорк, Нью-Йорк: Академик Пресс. стр. 1459–1460.
- ^ Jump up to: а б А. Г. Шарп; HJ Эмелеус (1968). Достижения неорганической химии и радиохимии . Эльзевир Наука. п. 21. ISBN 9780080578606 .
- ^ Jump up to: а б Эдвард Андерс (1960). «РАДИОХИМИЯ ТЕХНЕЦИЯ» . ОСТИ.ГОВ . Отдел научно-технической информации Министерства энергетики США: 8. doi : 10.2172/4073069 . ОСТИ 4073069 . Проверено 4 ноября 2022 г.
- ^ Л. Б. Роджерс (1949). «Электроразделение технеция от рения и молибдена». Журнал Американского химического общества . 71 (4): 1507–1508. дои : 10.1021/ja01172a520 .
- ^ КМ Нельсон; Дж. Э. Бойд; Вм. Т. Смит-младший (1954). «Магнитохимия технеция и рения». Журнал Американского химического общества . 76 (2). Публикации ACS: 348–352. дои : 10.1021/ja01631a009 .
- ^ Брэдли Ковингтон Чайлдс (2017). Летучие оксиды технеция: значение для остекловывания ядерных отходов . Диссертации, диссертации, профессиональные статьи и основные положения UNLV (тезисы). дои : 10.34917/10985836 .
- ^ Эдвард Эндрюс (1959). «Химия технеция и астата» . Ежегодный обзор ядерной науки . 9 . Годовые обзоры: 203–220. doi : 10.1146/annurev.ns.09.120159.001223 .
- ^ Херрелл, AY; Бьюзи, Р.Х.; Гейер, К.Х. (1977). Оксид технеция (VII) в неорганическом синтезе . Том. XVII. стр. 155–158. дои : 10.1002/9780470132487.ch41 . ISBN 0-07-044327-0 .
- ^ Кребс, Бернт (1969). «Оксид технеция (VII): оксид переходного металла с твердотельной молекулярной структурой». Прикладная химия . 81 (9): 328–329. Бибкод : 1969АнгЧ..81..328К . дои : 10.1002/anie.19690810905 .
- ^ Г. Глемсер «Оксид рения (IV)», Справочник по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, Нью-Йорк. Том. 1. п. 1480.
- ^ «РЕНИЯ ДИОКСИД - Производитель» . Aaamolybdenum.com. Архивировано из оригинала 9 февраля 2003 г. Проверено 6 августа 2012 г.
- ^ Г. Глемсер «Ренат натрия (IV)» Справочник по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, Нью-Йорк. Том. 1. п. 1483.
- ^ Шмидт, Макс; Шмидбаур, Хуберт (1967). Триметилсилилперренат . Неорганические синтезы. Том. 9. стр. 149–151. дои : 10.1002/9780470132401.ch40 . ISBN 9780470132401 .
- ^ Jump up to: а б О. Глемсер (1963). «Рений». В Г. Брауэре (ред.). Справочник по препаративной неорганической химии . Том. 1 (2-е изд.). Академическая пресса. стр. 1476–1485.
- ^ Георг Надлер, Ганс (2000). «Рений и рениевые соединения». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a23_199 . ISBN 3527306730 .
- ^ Нечамкин, Х.; Хиски, CF; Мёллер, Теральд; Шумейкер, CE (январь 1950 г.), Одриет, Людвиг Ф. (редактор), «Оксид рения (VI) (триоксид рения)» , Inorganic Syntheses , vol. 3 (1-е изд.), Wiley, стр. 186–188, номер документа : 10.1002/9780470132340.ch49 , ISBN. 978-0-470-13162-6 , получено 26 августа 2023 г.
- ^ О. Глемсер; Р. Зауэр (1963). «Оксид рения (VI)». В Г. Брауэре (ред.). Справочник по препаративной неорганической химии, 2-е изд . Том. 2 страницы = 1482. Нью-Йорк, Нью-Йорк: Академическая пресса.
- ^ Стаут, Дж.В.; Рид, Стэнли А. (1954). «Кристаллическая структура MnF 2 , FeF 2 , CoF 2 , NiF 2 и ZnF 2 ». Дж. Ам. хим. Соц . 76 (21): 5279–5281. дои : 10.1021/ja01650a005 .
- ^ Эйрс, округ Колумбия; Хеллиер, Десмонд (1997). Словарь экологически важных химических веществ . ЦРК Пресс. п. 195. ИСБН 0-7514-0256-7 . Проверено 18 июня 2008 г.
- ^ «Шахматы» .
- ^ «Кемпите» .
- ^ Jump up to: а б Чепанец, Ивица (2004). Синтез биарилов . Эльсевейр. п. 104. ИСБН 0-08-044412-1 . Проверено 18 июня 2008 г.
- ^ Джонстон, EV (май 2014 г.). Бинарные галогениды технеция (Диссертация). Университет Невады, Лас-Вегас. doi : 10.34917/5836118 – через диссертации, диссертации, профессиональные статьи и основные положения UNLV.
- ^ Jump up to: а б с д Пуано, Фредерик; Джонстон, Эрик В.; Червински, Кеннет Р.; Саттельбергер, Альфред П. (2014). «Последние достижения в химии галогенидов технеция». Отчеты о химических исследованиях . 47 (2): 624–632. дои : 10.1021/ar400225b . ПМИД 24393028 .
- ^ Пуано, Фредерик; Джонстон, Эрик В.; Век, Филипп Ф.; Ким, Ынджа; Форстер, Пол М.; Скотт, Брайан Л.; Саттельбергер, Альфред П.; Червински, Кеннет Р. (2010). «Синтез и структура трихлорида технеция». Журнал Американского химического общества . 132 (45): 15864–5. дои : 10.1021/ja105730e . ПМИД 20977207 .
- ^ Швохау 2000 , стр. 7–9.
- ^ немецкий, КЭ; Крючков, С.В. (2002). «Полиядерные кластеры галогенидов технеция» . Российский журнал неорганической химии . 47 (4): 578–583. Архивировано из оригинала 22 декабря 2015 г.
- ^ Каье, Жерар; Дюпле, Кристоф; Буэндиа, Жюльен (2009). «Химия марганцевоорганических соединений(II)». хим. Откр. 109 (3): 1434–1476. дои : 10.1021/cr800341a . ПМИД 19209933 .
- ^ Лэйфилд, Ричард А. (2008). «Марганец (II): паршивая овца металлоорганического семейства». хим. Соц. Откр. 37 (6): 1098–1107. дои : 10.1039/b708850g . ПМИД 18497923 .
- ^ Бартоломя, Марк Д.; Луи, Аника С.; Вэллиант, Джон Ф.; Зубиета, Джон (2010). «Радиофармацевтические препараты, полученные из технеция и галлия: сравнение и сопоставление химического состава двух важных радиометаллов для эпохи молекулярной визуализации». Химические обзоры . 110 (5): 2903–20. дои : 10.1021/cr1000755 . ПМИД 20415476 .
- ^ Jump up to: а б с Альберто, Роджер (2010). «Металлоорганические радиофармпрепараты». Медицинская металлоорганическая химия . Темы металлоорганической химии. Том. 32. С. 219–246. дои : 10.1007/978-3-642-13185-1_9 . ISBN 978-3-642-13184-4 .
- ^ Хилман, Дж. К.; Хаггинс, ДК; Каес, HD (1961). «Карбонил технеция». Журнал Американского химического общества . 83 (13): 2953–2954. дои : 10.1021/ja01474a038 .
- ^ Бейли, МФ; Даль, Лоуренс Ф. (1965). «Кристаллическая структура декакарбонила дитехнеция». Неорганическая химия . 4 (8): 1140–1145. дои : 10.1021/ic50030a011 .
- ^ Уоллах, Д. (1962). «Элементарная ячейка и пространственная группа карбонила технеция, Tc2 (CO) 10». Акта Кристаллографика . 15 (10): 1058. дои : 10.1107/S0365110X62002789 .
- ^ Швохау 2000 , стр. 286, 328.
- ^ Бреймайр, Йозеф; Штайманн, Манфред; Вагнер, Барбара; Бек, Вольфганг (1990). «Нуклеофильное присоединение карбонильных металлятов к катионным алкиновым комплексам [CpL2M(η2-RC≡CR)]+ (M = Ru, Fe): μ-η1:η1-алкиновые комплексы». Химические отчеты . 123 :7. дои : 10.1002/cber.19901230103 .
- ^ Шмидт, Стивен П.; Троглер, Уильям К.; Басоло, Фред (1990). Галогениды пентакарбонилрения . Неорганические синтезы. Том. 28. стр. 154–159. дои : 10.1002/9780470132593.ch42 . ISBN 978-0-470-13259-3 .
- ^ Майкл А. Урбанчич; Джон Р. Шепли (1990). Пентакарбонилгидридорений . Неорганические синтезы. Том. 28. С. 165–168. дои : 10.1002/9780470132593.ch43 . ISBN 978-0-470-13259-3 .
- ^ Хадсон, А. (2002) «Метилтриоксорений» в Энциклопедии реагентов для органического синтеза . Джон Уайли и сыновья: Нью-Йорк, ISBN 9780470842898 , дои : 10.1002/047084289X .
- ^ Герман Константин Евгеньевич; Федосеев Александр Михайлович; Григорьев Михаил С.; Киракосян, Гаяне А.; Дюма, Томас; Ден Аувер, Кристоф; Мойзи, Филипп; Лоулер, Кейт В.; Форстер, Пол М.; Пуано, Фредерик (24 сентября 2021 г.). «70-летняя загадка химии технеция, объясненная новым полиоксометаллатом технеция [H 7 O 3 ] 4 [Tc 20 O 68 ] ⋅ 4H 2 O» . Химия – Европейский журнал . 27 (54): 13624–13631. дои : 10.1002/chem.202102035 . ISSN 0947-6539 .
- ^ Волков Михаил А.; Новиков Антон П.; Борисова, Наталья Е.; Григорьев Михаил С.; Герман, Константин Евгеньевич (21 августа 2023 г.). «Внутримолекулярные невалентные взаимодействия Re···O как стабилизатор полиоксорената (VII)» . Неорганическая химия . 62 (33): 13485–13494. doi : 10.1021/acs.inorgchem.3c01863 . ISSN 0020-1669 .
- ^ Чалмин, Э.; Виньо, К.; Саломон, Х.; Фарж, Ф.; Сузини, Дж.; Меню, М. (2006). «Минералы, обнаруженные в палеолитических черных пигментах с помощью просвечивающей электронной микроскопии и микрорентгеновской абсорбционной прикраевой структуры» (PDF) . Прикладная физика А. 83 (12): 213–218. Бибкод : 2006ApPhA..83..213C . дои : 10.1007/s00339-006-3510-7 . hdl : 2268/67458 . S2CID 9221234 .
- ^ Сейр, EV; Смит, RW (1961). «Композиционные категории древнего стекла». Наука . 133 (3467): 1824–1826. Бибкод : 1961Sci...133.1824S . дои : 10.1126/science.133.3467.1824 . ПМИД 17818999 . S2CID 25198686 .
- ^ Маккрей, В. Патрик (1998). «Стеклопроизводство в Италии эпохи Возрождения: инновация венецианского кристалло». ДЖОМ . 50 (5): 14–19. Бибкод : 1998JOM....50e..14M . дои : 10.1007/s11837-998-0024-0 . S2CID 111314824 .
- ^ Тилгнер, Ханс Георг (2000). Исследования поиска и зависимости (на немецком языке). Книги по требованию. ISBN 978-3-89811-272-7 .
- ^ «Рений: статистика и информация» . Информация о минералах . Геологическая служба США . 2011 . Проверено 25 мая 2011 г.
- ^ Мозли, Генри (1914). «Высокочастотные спектры элементов, часть II» . Философский журнал . 27 (160): 703–713. дои : 10.1080/14786440408635141 . Архивировано из оригинала 22 января 2010 г. Проверено 14 мая 2009 г.
- ^ Ёшихара, Гонконг (2004). «Открытие нового элемента« ниппоний »: переоценка новаторских работ Масатаки Огавы и его сына Эйджиро Огавы». Spectrochimica Acta Часть B: Атомная спектроскопия . 59 (8): 1305–1310. Бибкод : 2004AcSpe..59.1305Y . дои : 10.1016/j.sab.2003.12.027 .
- ^ Хисамацу, Ёдзи; Эгашира, Казухиро; Маэно, Ёситеру (2022). «Ниппоний Огавы и его переприсвоение рению» . Основы химии . 24 : 15–57. дои : 10.1007/s10698-021-09410-x . Проверено 16 ноября 2023 г.
- ^ Орстрем, Ларс; Ридейк, январь (28 ноября 2016 г.). «Названия и символы элементов с атомными номерами 113, 115, 117 и 118 (Рекомендации ИЮПАК 2016 г.)» (PDF) . Чистое приложение. Хим . 88 (12): 1225–1229. дои : 10.1515/pac-2016-0501 . hdl : 1887/47427 . S2CID 99429711 . Проверено 22 апреля 2017 г.
- ^ Ноддак, В.; Таке, И.; Берг, О. (1925). «Экаманганы». естественные науки . 13 (26): 567–574. Бибкод : 1925NW.....13..567. . дои : 10.1007/BF01558746 . S2CID 32974087 .
- ^ Ноддак, В.; Ноддак, И. (1929). «Производство грамма рения». Журнал неорганической и общей химии (на немецком языке). 183 (1): 353–375. дои : 10.1002/zaac.19291830126 .
- ^ Комитет по техническим аспектам критических и стратегических материалов, Национальный исследовательский совет (США) (1968). Тенденции использования рения: Отчет . стр. 4–5.
- ^ Savitskiĭ, Evgeniĭ Mikhaĭlovich; Tulkina, Mariia Aronovna; Povarova, Kira Borisovna (1970). Rhenium alloys .
- ^ Хейзерман, Д.Л. (1992). «Элемент 43: Технеций» . Изучение химических элементов и их соединений . Нью-Йорк: TAB Books. п. 164. ИСБН 978-0-8306-3018-9 .
- ^ Сегре, Эмилио (1993). Разум всегда в движении: автобиография Эмилио Сегре . Беркли, Калифорния: Издательство Калифорнийского университета. стр. 115–118 . ISBN 978-0520076273 .
- ^ Ю; Демин, А.Г.; Данилов, Н.А.; Флеров Г.Н.; Иванов, депутат; Ильжинов А.С.; Колесников Н.Н.; Марков Б.Н.; Плотко В.М.; Третьякова, СП (1976). «О спонтанном делении нейтронодефицитных изотопов элементов». Ядерная физика А . 273 : 505–522. дои : 10.1016/0375-9474(76)90607-2 .
- ^ Jump up to: а б Барбер, Р.К.; Гринвуд, штат Нью-Йорк; Гринкевич, АЗ; Жаннен, Ю.П.; Лефорт, М.; Сакаи, М.; Улехла, И.; Вапстра, AP; Уилкинсон, Д.Х. (1993). «Открытие трансфермиевых элементов. Часть II: Введение в профили открытия. Часть III: Профили открытия трансфермиевых элементов» . Чистая и прикладная химия . 65 (8): 1757. doi : 10.1351/pac199365081757 . S2CID 195819585 .
- ^ Мюнценберг, Г.; Хофманн, С.; Хессбергер, ФП; Рейсдорф, В.; Шмидт, К.Х.; Шнайдер, JHR; Армбрустер, П.; Сам, CC; Тума, Б. (1981). «Идентификация элемента 107 по α-корреляционным цепочкам» . Журнал физики А. 300 (1): 107–8. Бибкод : 1981ZPhyA.300..107M . дои : 10.1007/BF01412623 . S2CID 118312056 . Проверено 24 декабря 2016 г.
- ^ Jump up to: а б с Эмсли 2001 , стр. 249–253.
- ^ Бхаттачарья, ПК; Дасгупта, Сомнатх; Фукуока, М.; Рой Суприя (1984). «Геохимия браунита и связанных с ним фаз в метаморфизованных неизвестковых марганцевых рудах Индии». Вклад в минералогию и петрологию . 87 (1): 65–71. Бибкод : 1984CoMP...87...65B . дои : 10.1007/BF00371403 . S2CID 129495326 .
- ^ Jump up to: а б Обзор минеральных ресурсов Геологической службы США за 2009 г.
- ^ Jump up to: а б Холлеман, Арнольд Ф.; Виберг, Эгон; Виберг, Нильс (1985). «Марганец». Учебник неорганической химии (на немецком языке) (91–100 изд.). Вальтер де Грюйтер. стр. 1110–1117. ISBN 978-3-11-007511-3 .
- ^ Кук, Найджел Дж.; Чобану, Кристиана Л.; Принг, Аллан; Скиннер, Уильям; Симидзу, Масааки; Данюшевский Леонид; Сайни-Эйдукат, Бернхардт; Мельчер, Фрэнк (2009). «Следы и второстепенные элементы в сфалерите: исследование LA-ICPMS» . Geochimica et Cosmochimica Acta . 73 (16): 4761–4791. Бибкод : 2009GeCoA..73.4761C . дои : 10.1016/j.gca.2009.05.045 .
- ^ Ван, X; Шредер, ХК; Винс, М; Шлоссмахер, У; Мюллер, WEG (2009). «Марганцевые/полиметаллические конкреции: микроструктурная характеристика экзолитобионтических и эндолитобионтических микробных биопленок с помощью сканирующей электронной микроскопии». Микрон . 40 (3): 350–358. дои : 10.1016/j.micron.2008.10.005 . ПМИД 19027306 .
- ^ Управление ООН по экономике и технологиям океана, Технологический отдел, Организация Объединенных Наций (1978 год). «Марганцевые конкреции: размеры и перспективы». Морская геология . 41 (3–4). Спрингер: 343. Бибкод : 1981MGeol..41..343C . дои : 10.1016/0025-3227(81)90092-X . ISBN 978-90-277-0500-6 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ «Добыча марганца в Южной Африке – обзор» . MBendi.com. Архивировано из оригинала 5 февраля 2016 года . Проверено 4 января 2014 г.
{{cite web}}: CS1 maint: bot: исходный статус URL неизвестен ( ссылка ) - ^ Эллиотт, Р.; Коли, К; Мостагель, С; Барати, М (2018). «Обзор обработки марганца для производства сталей TRIP/TWIP, Часть 1: Текущая практика и основы обработки». ДЖОМ . 70 (5): 680–690. Бибкод : 2018JOM....70e.680E . дои : 10.1007/s11837-018-2769-4 . S2CID 139950857 .
- ^ Коратерс, Луизиана; Мачамер, Дж. Ф. (2006). «Марганец» . Промышленные минералы и горные породы: товары, рынки и использование (7-е изд.). МСП. стр. 631–636. ISBN 978-0-87335-233-8 .
- ^ Чжан, Вэньшэн; Ченг, Чу Юн (2007). «Обзор металлургии марганца. Часть I: Выщелачивание руд/вторичных материалов и извлечение электролитического/химического диоксида марганца». Гидрометаллургия . 89 (3–4): 137–159. doi : 10.1016/j.гидромет.2007.08.010 .
- ^ Чоу, Норман; Наку, Анка; Варкентин, Дуг; Аксенов, Игорь и Тех, Мотыга (2010). «Извлечение марганца из низкосортных ресурсов: завершена программа стендовых металлургических испытаний» (PDF) . Kemetco Research Inc. Архивировано из оригинала (PDF) 2 февраля 2012 года.
- ^ «Тайна ЦРУ на дне океана» . Новости Би-би-си . 19 февраля 2018 года . Проверено 3 мая 2018 г.
- ^ «Проект Азориан: рассекреченная ЦРУ история Glomar Explorer» . Архив национальной безопасности Университета Джорджа Вашингтона. 12 февраля 2010 г. Проверено 18 сентября 2013 г.
- ^ Хейн, Джеймс Р. (январь 2016 г.). Энциклопедия морских геолого-геофизических наук — Марганцевые конкреции . Спрингер. стр. 408–412 . Проверено 2 февраля 2021 г.
- ^ Хосейнпур, Вахид; Гаеми, Насер (1 декабря 2018 г.). «Зеленый синтез наночастиц марганца: применение и будущие перспективы – обзор» . Журнал фотохимии и фотобиологии B: Биология . 189 : 234–243. doi : 10.1016/j.jphotobiol.2018.10.022 . ПМИД 30412855 . S2CID 53248245 . Проверено 2 февраля 2021 г.
- ^ Международный орган по морскому дну. «Полиметаллические конкреции» (PDF) . isa.org . Международный орган по морскому дну. Архивировано из оригинала (PDF) 23 октября 2021 года . Проверено 2 февраля 2021 г.
- ^ Обиус, Хорст У; Беккер, Герман Дж; Ролински, Сюзанна; Янковский, Яцек А. (январь 2001 г.). «Параметризация и оценка воздействия на морскую окружающую среду глубоководной добычи марганцевых конкреций» . Глубоководные исследования, часть II: Актуальные исследования в океанографии . 48 (17–18): 3453–3467. Бибкод : 2001DSRII..48.3453O . дои : 10.1016/s0967-0645(01)00052-2 . ISSN 0967-0645 .
- ^ Томпсон, Кирстен Ф.; Миллер, Кэтрин А.; Карри, Дункан; Джонстон, Пол; Сантильо, Дэвид (2018). «Добыча полезных ископаемых на морском дне и подходы к управлению глубоководными участками морского дна» . Границы морской науки . 5 . дои : 10.3389/fmars.2018.00480 . hdl : 10871/130176 . S2CID 54465407 .
- ^ Jump up to: а б Эмсли 2001 , стр. 422–425 .
- ^ Диксон, П.; Кертис, Дэвид Б.; Масгрейв, Джон; Ренш, Фред; Роуч, Джефф; Рокоп, Дон (1997). «Анализ естественно произведенного технеция и плутония в геологических материалах». Аналитическая химия . 69 (9): 1692–1699. дои : 10.1021/ac961159q . ПМИД 21639292 .
- ^ Кертис, Д.; Фабрика-Мартин, июнь; Диксон, Пол; Крамер, Ян (1999). «Необычные элементы природы: плутоний и технеций» . Geochimica et Cosmochimica Acta . 63 (2): 275. Бибкод : 1999GeCoA..63..275C . дои : 10.1016/S0016-7037(98)00282-8 .
- ^ Хаммонд 2004 , с. 4-1 .
- ^ Мур, CE (1951). «Технеций на Солнце». Наука . 114 (2951): 59–61. Бибкод : 1951Sci...114...59M . дои : 10.1126/science.114.2951.59 . ПМИД 17782983 .
- ^ «Рений - Информация об элементе, свойства и использование | Таблица Менделеева» . www.rsc.org . Проверено 2 декабря 2019 г.
- ^ Эмсли 2001 , стр. 358–360 .
- ^ Jump up to: а б Рушиас, Джордж (1974). «Последние достижения химии рения». Химические обзоры . 74 (5): 531. doi : 10.1021/cr60291a002 .
- ^ Андерсон, Стив Т. «Ежегодник полезных ископаемых за 2005 год: Чили» (PDF) . Геологическая служба США . Проверено 26 октября 2008 г.
- ^ Коржинский, М.А.; Ткаченко С.И.; Шмулович, К.И.; Таран Ю.А.; Стейнберг, Г.С. (5 мая 2004 г.). «Открытие чистого минерала рения на вулкане Кудрявый». Природа . 369 (6475): 51–52. Бибкод : 1994Natur.369...51K . дои : 10.1038/369051a0 . S2CID 4344624 .
- ^ Кременецкий А.А.; Чаплыгин, ИВ (2010). «Концентрация рения и других редких металлов в газах вулкана Кудрявый (остров Итуруп, Курильские острова)». Доклады наук о Земле . 430 (1):114. Бибкод : 2010ДокЕС.430..114К . дои : 10.1134/S1028334X10010253 . S2CID 140632604 .
- ^ Тессалина, С.; Юдовская, М.; Чаплыгин И.; Бирк, Дж.; Капмас, Ф. (2008). «Источники уникального обогащения рения в фумаролах и сульфидах вулкана Кудрявый». Geochimica et Cosmochimica Acta . 72 (3): 889. Бибкод : 2008GeCoA..72..889T . дои : 10.1016/j.gca.2007.11.015 .
- ^ «Минерал Рениет» . Аметистовые галереи.
- ^ Джон, окружной прокурор; Тейлор, Р.Д. (2016). «Глава 7: Побочные продукты медно-порфировых и молибденовых месторождений». У Филипа Л. Верпланка и Мюррея В. Хитцмана (ред.). Редкоземельные и критические элементы в рудных месторождениях . Том. 18. стр. 137–164.
- ^ Мадьяр, Майкл Дж. (январь 2012 г.). «Рений» (PDF) . Обзоры минеральных товаров . Геологическая служба США . Проверено 4 сентября 2013 г.
- ^ «Цены на MinorMetal» . minormetals.com. Архивировано из оригинала 15 мая 2008 г. Проверено 17 февраля 2008 г.
- ^ Харви, Ян (10 июля 2008 г.). «Анализ: сверхгорячий металл рений может достичь «цены на платину» » . Рейтер Индия. Архивировано из оригинала 11 января 2009 г. Проверено 26 октября 2008 г.
- ^ Руденко А.А.; Трошкина И.Д.; Данилейко В.В.; Барабанов О.С.; Вацура, финансовый год (2021 г.). «Перспективы селективного и опережающего извлечения рения из продуктивных растворов подземного выщелачивания урановых руд месторождения Добровольное» . Горные науки и технологии (Россия) . 6 (3): 158–169. дои : 10.17073/2500-0632-2021-3-158-169 . S2CID 241476783 .
- ^ Jump up to: а б с Грайс, Кайл (2014). «Недавние исследования бипиридинкарбонильных катализаторов рения и марганца для электрохимического восстановления CO2». Достижения неорганической химии . 66 : 163–188. дои : 10.1016/B978-0-12-420221-4.00005-6 . ISBN 9780124202214 .
- ^ Буррес, Марк (2011). «[Mn(бипиридил)(CO)3Br]: богатый карбонильный комплекс металла как эффективный электрокатализатор восстановления CO2». Angewandte Chemie International Edition на английском языке . 50 (42): 9903–9906. дои : 10.1002/anie.201103616 . ПМИД 21922614 .
- ^ Jump up to: а б с Франке, Роберт (2018). «Гомогенно-катализируемое электровосстановление диоксида углерода - методы, механизмы и катализаторы». Химические обзоры . 118 (9): 4631–4701. doi : 10.1021/acs.chemrev.7b00459 . ПМИД 29319300 .
- ^ Лоуренс Найт (30 мая 2015 г.). «Элемент, который может заставить кости светиться» . Би-би-си . Проверено 30 мая 2015 г.
- ^ Герен Б; Трамбле С; Родриг С; Руссо Ж.А.; и др. (2010). «Циклотронное производство 99 м Tc: подход к кризису медицинских изотопов» (PDF) . Journal of Nuclear Medicine . 51 (4): 13N–6N. PMID 20351346 .
- ^ Римшоу, SJ (1968). Хэмпель, Калифорния (ред.). Энциклопедия химических элементов . Нью-Йорк: Книжная корпорация Рейнхолда. стр. 689–693 .
- ^ Швохау 2000 , с. 414.
- ^ Альберто, Роджер; Надим, Кайсар (2021). «Глава 7. 99 м Агенты визуализации на основе технеция и разработки в области 99 Tc Chemistry». Ионы металлов в методах биовизуализации . Springer. стр. 195–238. doi : 10.1515/9783110685701-013 . S2CID 233684677 .
- ^ Швохау 2000 , стр. 12–27.
- ^ Швохау 2000 , с. 87.
- ^ Джеймс С. Туленко; Дин Шенфельд; Дэвид Хинтенланг; Карл Крейн; Шеннон Риджуэй; Хосе Сантьяго; Чарльз Шир (30 ноября 2006 г.). Университетская исследовательская программа в области робототехники ОТЧЕТ (PDF) (Отчет). Университет Флориды. дои : 10.2172/895620 . Проверено 12 октября 2007 г.
- ^ Швохау 2000 , стр. 87–90.
- ^ Jump up to: а б Эмсли 2001 , с. 425.
- ^ «Глава 14, методы разделения» (PDF) . Агентство по охране окружающей среды: 402-b-04-001b-14-final . Агентство по охране окружающей среды США. Июль 2004 г. Архивировано (PDF) из оригинала 8 марта 2014 г. Проверено 4 августа 2008 г.
- ^ Jump up to: а б Швохау 2000 , с. 91.
- ^ Хавекер, Жанно (1984). «Электрокаталитическое восстановление углекислого газа, опосредованное Re (bipy) (CO) 3Cl (bipy = 2,2'-бипиридин)». Дж. Хим. Соц., хим. Коммун. : 328–330. дои : 10.1039/C39840000328 .
- ^ Салливан, Б. Патрик (1985). «Одно- и двухэлектронные пути электрокаталитического восстановления CO2 с помощью fac-Re(bpy)(CO)3Cl (bpy = 2,2'-бипиридин)». Дж. Хим. Соц., хим. Коммун. : 1414–1416. дои : 10.1039/C39850001414 .
- ^ Хасан, Хизер (2008). Марганец . Издательская группа Розен. п. 31. ISBN 978-1-4042-1408-8 .
- ^ «Химическая основа марганца» . Институт морской и экологической отчетности Меткалфа, Университет Род-Айленда. Апрель 2006 г. Архивировано из оригинала 28 августа 2006 г. Проверено 30 апреля 2008 г.
- ^ «Краткая информация о токсичности информационной системы оценки рисков для марганца» . Окриджская национальная лаборатория . Проверено 23 апреля 2008 г.
- ^ Десмет, Г.; Миттенар, К. (1986). Технеций в окружающей среде . Спрингер. стр. 392–395. ISBN 978-0-85334-421-6 .
- ^ Швохау 2000 , стр. 371–381.
- ^ Швохау 2000 , с. 40.
- ^ Эмсли 2001 , с. 358-361.
- ^ Хейли, Томас Дж.; Картрайт, Фрэнк Д. (1968). «Фармакология и токсикология перрената калия и трихлорида рения». Журнал фармацевтических наук . 57 (2): 321–323. дои : 10.1002/jps.2600570218 . ПМИД 5641681 .
- ^ Эриксон, К.М.; Ашнер, М. (2019). «Марганец: его роль в болезнях и здоровье». Незаменимые металлы в медицине: терапевтическое использование и токсичность ионов металлов в клинике . Ионы металлов в науках о жизни . Том. 19. стр. 253–266. дои : 10.1515/9783110527872-016 . ISBN 978-3-11-052787-2 . ПМИД 30855111 . S2CID 73725546 .
- ^ Эмсли 2001 , стр. 249–253 .
- ^ Такеда, А. (2003). «Действие марганца на функцию мозга». Обзоры исследований мозга . 41 (1): 79–87. дои : 10.1016/S0165-0173(02)00234-5 . ПМИД 12505649 . S2CID 1922613 .
Библиография
[ редактировать ]- Эмсли, Джон (2001). Строительные блоки природы: Путеводитель по элементам от Аризоны . Оксфорд, Великобритания: Издательство Оксфордского университета. ISBN 978-0-19-850340-8 .
- Хаммонд, ЧР (2004). Лиде, Дэвид Р. (ред.). CRC справочник по химии и физике: готовый справочник химических и физических данных . Бока-Ратон: CRC Press. ISBN 978-0-8493-0485-9 .
- Швохау, К. (2000). Технеций: химия и радиофармацевтические применения . Вайнхайм, Германия: Wiley-VCH. ISBN 978-3-527-29496-1 .


