Оксид марганца(II,III)
 | |
| Имена | |
|---|---|
| Название ИЮПАК оксид марганца(II) димарганца(III) | |
| Другие имена четырехокись марганца; Оксид марганца, Оксид марганца, Тетраоксид тримарганца, Четырехокись тримарганца [1] | |
| Идентификаторы | |
3D model ( JSmol ) | |
| Информационная карта ECHA | 100.013.879 |
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| Mn3OMn3O4 MnO Mn 2 O 3 | |
| Молярная масса | 228.812 g/mol |
| Появление | коричневато-черный порошок [1] |
| Плотность | 4,86 г/см 3 |
| Температура плавления | 1567 ° C (2853 ° F; 1840 К) |
| Точка кипения | 2847 ° C (5157 ° F; 3120 К) |
| нерастворимый | |
| Растворимость | растворим в HCl |
| +12,400·10 −6 см 3 /моль | |
| Структура | |
| Шпинель (тетрагональная), tI 28 | |
| И 4 1 /амд, № 141 | |
| Опасности | |
| NIOSH (пределы воздействия на здоровье в США): | |
МЕХ (Допускается) | С 5 мг/м 3 [1] |
РЕЛ (рекомендуется) | Не установлено [1] |
IDLH (Непосредственная опасность) | без даты [1] |
| Термохимия | |
Стандартный моляр энтропия ( S ⦵ 298 ) | 149 Дж·моль −1 ·К −1 [2] |
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | −1387 кДж·моль −1 [2] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Оксид марганца(II,III) – химическое соединение формулы Mn 3 O 4 . Марганец присутствует в двух степенях окисления +2 и +3, и формулу иногда записывают как MnO · Mn 2 O 3 . Mn 3 O 4 встречается в природе в виде минерала гаусманнита .
Подготовка
[ редактировать ]Mn 3 O 4 образуется при нагревании любого оксида марганца на воздухе выше 1000 °С. [3] Значительные исследования были сосредоточены на производстве нанокристаллического Mn 3 O 4 и различных синтезах, включающих окисление Mn. II или уменьшение Mn МЫ . [4] [5] [6]
Реакции
[ редактировать ]Было обнаружено, что Mn 3 O 4 действует как катализатор ряда реакций, например, окисления метана и монооксида углерода; [7] [8] разложение NO, [9] восстановление нитробензола [10] и каталитическое горение органических соединений. [11]
Структура
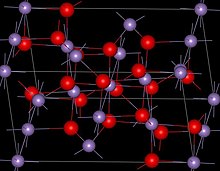
[ редактировать ]Mn 3 O 4 имеет структуру шпинели , в которой ионы оксида имеют кубическую плотную упаковку, а ионы Mn II занимают тетраэдрические позиции, а Mn III октаэдрические площадки. [3] Структура искажается из-за эффекта Яна-Теллера . [3] При комнатной температуре Mn 3 O 4 парамагнитен . , ниже 41-43 К — ферримагнитен [12] хотя сообщается, что в нанокристаллических образцах это снижает температуру примерно до 39 К. [13]
Использование
[ редактировать ]Mn 3 O 4 иногда используется в качестве исходного материала при производстве мягких ферритов, например феррита марганца-цинка, [14] и оксид лития-марганца, используемый в литиевых батареях. [15]
Четырехокись марганца также может использоваться в качестве утяжелителя при бурении пластов нефтяных и газовых скважин. [ нужна ссылка ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и Карманный справочник NIOSH по химическим опасностям. «#0381» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Jump up to: а б Зумдал, Стивен С. (2009). Химические принципы 6-е изд . Компания Хоутон Миффлин. п. А22. ISBN 978-0-618-94690-7 .
- ^ Jump up to: а б с Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Наностержни гаусманита Mn 3 O 4 : синтез, характеристика и магнитные свойства Jin Du et al. Нанотехнологии, (2006), 17 4923-4928, дои : 10.1088/0957-4484/17/19/024
- ^ Одностадийный синтез наночастиц Mn 3 O 4 : структурное и магнитное исследование Васкес-Олмос А., Редон Р., Родригес-Гатторно Г., Мата-Самора М.Э., Моралес-Лил Ф., Фернандес-Осорио А.Л., Санигер Дж.М. Журнал Коллоид и интерфейсная наука, 291, 1, (2005), 175-180. doi : 10.1016/j.jcis.2005.05.005
- ^ Использование микросфер углеродистого полисахарида в качестве шаблонов для изготовления полых сфер из оксида металла Сяомин Сунь, Цзюньфэн Лю, Ядун Ли, Химия - Европейский журнал, (2005), 12, 7, 2039–2047, doi : 10.1002/chem.200500660
- ^ Восстановление и окисление оксидов марганца Стобхе Э.Р., де Бур А.Д., Геус Дж.В., Катализ сегодня. (1999), 47, 161–167. дои : 10.1016/S0920-5861(98)00296-X
- ^ Рентгеновское исследование in situ одно- и дважды промотированных катализаторов сочетания оксида марганца с метаном. Моггридж Г.Д., Рэймент Т., Ламберт Р.М. Журнал катализа, (1992), 134, 242–252, дои : 10.1016/0021-9517(92)90225-7
- ^ НЕТ Разложение над Mn 2 O 3 и Mn 3 O 4 . Ямашита Т., Ваннис А., Журнал катализа (1996), 163, 158–168, два : 10.1006/jcat.1996.0315
- ^ Селективное восстановление нитробензола до нитрозобензола с использованием различных типов катализаторов тетраоксида тримарганца. Ван В.М., Ян Ю.Н., Чжан Дж.Ю., Applied Catalysis A. (1995), 133, 1, 81–93. два : 10.1016/0926-860X(95)00186-7
- ^ Каталитическое горение углеводородов и оксигенатов C3 над Mn 3 O 4 . Балди М., Финоккио Э., Милелла Ф., Буска Г., Прикладной катализ Б. (1998), 16, 1, 43–51, дои : 10.1016/S0926-3373(97)00061-1
- ^ Магнитная структура Mn 3 O 4 по данным нейтронной дифракции Баушер Б., Буль Р., Перрин М., J. Appl. Физ. 42, 1615 (1971); дои : 10.1063/1.1660364
- ^ Синтез суперпарамагнитных нанокристаллитов Mn 3 O 4 ультразвуковым облучением И. К. Гопалакришнан, Н. Багкар, Р. Гангули и С. К. Кулшрешта Journal of Crystal Growth 280, 3-4, (2005), 436-441, дои : 10.1016/j.jcrysgro.2005.03.060
- ^ Способ изготовления марганцево-цинкового феррита Номер патента США: 4093688 (1978).Артур Уитоп, Роджер Эмиль Травальи
- ^ Процесс получения оксидов лития-марганца, номер патента США: 6706443 (2004), Хорст Крампиц, Герхард Вонер