Диоксид серы
 | |
 | |
| Имена | |
|---|---|
| Другие имена оксид дисеры(II) ТАК димер | |
| Идентификаторы | |
3D model ( JSmol ) | |
ПабХим CID | |
| Характеристики | |
| S2OS2O2 | |
| Молярная масса | 96.1299 g/mol |
| Появление | газ |
| Структура | |
| согнутый | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | токсичный |
| Родственные соединения | |
Родственные соединения | тетрасера ТАК , S3С3О S2С2О |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Диоксид серы , димерный монооксид серы или димер SO представляет собой с формулой оксид серы S 2 O 2 . [2] Твердое вещество нестабильно, его время жизни составляет несколько секунд при комнатной температуре. [3]
Структура
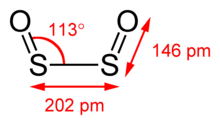
[ редактировать ]Диоксид дисеры имеет - планарную структуру с C2v цис симметрией . Длина связи S-O составляет 145,8 пм, что короче, чем в монооксиде серы . Длина связи S-S составляет 202,45 пм, а угол O-S-S составляет 112,7 °. S 2 O 2 имеет дипольный момент 3,17 Д. [4] Это асимметричная верхняя молекула. [1] [5]
Формирование
[ редактировать ]Окись серы (SO) самопроизвольно и обратимо превращается в диоксид серы (S 2 O 2 ). [4] Таким образом, вещество можно получить методами, производящими окись серы. Диоксид серы также образуется в результате электрического разряда в диоксиде серы . [5] Другая лабораторная процедура заключается в реакции атомов кислорода с карбонилсульфидом или парами сероуглерода . [6]
Хотя большинство форм элементарной серы ( S 8 и другие кольца и цепочки) не соединяются с SO 2 , атомарная сера делает это с образованием монооксида серы, который димеризуется: [7]
- С + ТАК 2 → С 2 О 2 ⇌ 2 ТАК
Диоксид серы также образуется при микроволновом разряде в диоксиде серы, разбавленном гелием . [8] При давлении 0,1 мм рт. ст. (13 Па) пять процентов результата составляет S 2 O 2 . [9]
Диоксид серы образуется временно, когда сероводород и кислород подвергаются мгновенному фотолизу . [10]
Характеристики
[ редактировать ]Энергия ионизации диоксида серы составляет 9,93 ± 0,02 эВ . [6]
Диоксид серы поглощает длину волны 320–400 нм, как это наблюдается в атмосфере Венеры . [11] и, как полагают, способствовал парниковому эффекту на этой планете. [12]
Реакции и разложение
[ редактировать ]Хотя диоксид серы существует в равновесии с монооксидом серы , он также реагирует с монооксидом серы с образованием диоксида серы и монооксида дисеры . [8] [13]
Разложение S 2 O 2 протекает по следующей реакции диспропорционирования :
- С 2 О 2 → ТАК 2 + 1/ 8 С 8
Комплексы
[ редактировать ]S 2 O 2 может быть лигандом переходных металлов. Он связывается в η 2 Положение -S–S, в котором оба атома серы связаны с атомом металла. [14] Впервые это было показано в 2003 году. Бис(триметилфосфин) тиран S -оксидный комплекс платины при нагревании в толуоле при 110 °C теряет этилен и образует комплекс с S 2 O 2 : (Ph 3 P) 2 Pt(S 2 О 2 ). [15] Атомы иридия также могут образовывать комплекс: цис -[(dppe) 2 IrS 2 ]Cl с периодатом натрия окисляется до [(dppe) 2 IrS 2 O], а затем до [(dppe) 2 IrS 2 O 2 ], причем dppe представляет собой 1,2-бис(дифенилфосфино)этан . [16] [17] Это вещество имеет S 2 O 2 в цис -положении. В тех же условиях может образоваться транс- комплекс, но вместо этого он содержит два отдельных радикала SO . Комплекс иридия можно разложить трифенилфосфином с образованием оксида трифенилфосфина и сульфида трифенилфосфина . [16]
Анион
[ редактировать ]С
22О −
2- радикал анион- наблюдался в газовой фазе. Он может принимать треугольную форму, подобную SO 3 . [18]
Спектр
[ редактировать ]Микроволновая печь
[ редактировать ]| Переход | Частота (МГц) [5] |
|---|---|
| 2 1,1 −2 0,2 | 11013.840 |
| 4 1,3 −4 0,4 | 14081.640 |
| 1 1,1 −0 0,0 | 15717.946 |
| 4 0,4 −3 1,3 | 16714.167 |
| 3 1,3 −2 0,2 | 26342.817 |
| 4 2,2 −4 1,3 | 26553.915 |
| 2 2,0 −2 1,1 | 28493.046 |
| 6 0,6 −5 1,5 | 30629.283 |
| 5 2,4 −5 1,5 | 35295.199 |
| 5 1,5 −4 0,4 | 35794.527 |
В Солнечной системе
[ редактировать ]Есть некоторые свидетельства того, что диоксид серы может быть небольшим компонентом атмосферы Венеры планеты и что он может существенно способствовать серьезному парниковому эффекту . [11] В земной атмосфере он не обнаружен ни в каком существенном количестве.
Ссылки
[ редактировать ]- ^ Jump up to: а б Демезон, Жан; Фогт, Юрген (2011). «836. O 2 S 2 Диоксид серы» (PDF) . Асимметричные верхние молекулы. Часть 3 . Ландольт-Бёрнштейн: молекулы и радикалы группы II. Том. 29Д3. Спрингер. п. 492. дои : 10.1007/978-3-642-14145-4_258 . ISBN 9783642141454 .
- ^ Холлеман, Арнольд Ф.; Вибер, Эгон; Виберг, Нильс, ред. (2001). «Оксиды серы» . Неорганическая химия . Академическая пресса. п. 530. ИСБН 9780123526519 .
- ^ Митчелл, Стивен С. (2004). Биологические взаимодействия соединений серы . ЦРК Пресс. п. 7. ISBN 9780203362525 .
- ^ Jump up to: а б Ловас, Ф.Дж. (1974). «Спектроскопические исследования разрядной системы SO 2. II. Микроволновой спектр димера SO». Журнал химической физики . 60 (12): 5005. Бибкод : 1974ЖЧФ..60.5005Л . дои : 10.1063/1.1681015 .
- ^ Jump up to: а б с Торвирт, Свен; Теуле, П.; Готлиб, Калифорния; Мюллер, HSP; Маккарти, MC; Таддеус, П. (2006). «Вращательная спектроскопия S 2 O: колебательные спутники», 33 Изотопомеры S и спектр субмиллиметровых волн » (PDF) . Journal of Molecular Structure . 795 (1–3): 219–229. Бибкод : 2006JMoSt.795..219T . doi : 10.1016/j.molstruc.2006.02.055 .
- ^ Jump up to: а б Ченг, Бин-Мин; Хун, Вэнь-Цзин (1999). «Спектр эффективности фотоионизации и энергия ионизации S 2 O 2 ». Журнал химической физики . 110 (1): 188. Бибкод : 1999JChPh.110..188C . дои : 10.1063/1.478094 . ISSN 0021-9606 .
- ^ Мураками, Ёсинори; Ониси, Сёичи; Кобаяши, Такаоми; Фуджи, Нобуюки; Ишики, Нобуясу; Цучия, Кентаро; Тезаки, Ацуму; Мацуи, Хироюки (2003). «Высокотемпературная реакция S + SO 2 → SO + SO: последствия образования промежуточного комплекса S 2 O 2 ». Журнал физической химии А. 107 (50): 10996–11000. Бибкод : 2003JPCA..10710996M . дои : 10.1021/jp030471i . ISSN 1089-5639 .
- ^ Jump up to: а б Филд, штат Калифорния; Слэттери, А.Е.; Адамс, диджей; Моррисон, Д.Д. (2005). «Экспериментальное наблюдение диссоциативного присоединения электронов к S 2 O и S 2 O 2 с помощью нового спектрометра нестабильных молекул» (PDF) . Журнал физики B: атомная, молекулярная и оптическая физика . 38 (3): 255–264. Бибкод : 2005JPhB...38..255F . дои : 10.1088/0953-4075/38/3/009 . ISSN 0953-4075 . S2CID 122789729 . Архивировано из оригинала (PDF) 24 сентября 2015 г. Проверено 13 мая 2013 г.
- ^ Саху, Баларам; Наяк, Нимай Чаран; Самантарай, Асутош; Пуджапанда, Прафулла Кумар (2012). Неорганическая химия . Обучение PHI. п. 461. ИСБН 9788120343085 . Проверено 16 мая 2013 г.
- ^ Комптон, Род-Джеймс; Бэмфорд, Швейцария; Типпер, CFH (1972). «Окисление H 2 S» . Реакции неметаллических неорганических соединений . Комплексная химическая кинетика. Эльзевир. п. 50. ISBN 9780080868011 .
- ^ Jump up to: а б Франдсен, Б.Н.; Веннберг, ПО; Кьергаард, Х.Г. (2016). «Идентификация OSSO как поглотителя ближнего УФ-излучения в атмосфере Венеры» (PDF) . Письма о геофизических исследованиях . 43 (21): 11146–11155. Бибкод : 2016GeoRL..4311146F . дои : 10.1002/2016GL070916 .
- ^ «Редкая молекула на Венере может помочь объяснить погоду на планете» . Новости ЦБК . Проверено 11 ноября 2016 г.
- ^ Херрон, Джей Ти; Хьюэ, RE (1980). «Константы скорости при 298 К реакций SO + SO + M → (SO) 2 + M и SO + (SO) 2 → SO 2 + S 2 O». Письма по химической физике . 76 (2): 322–324. Бибкод : 1980CPL....76..322H . дои : 10.1016/0009-2614(80)87032-1 .
- ^ Халкроу, Малкольм А.; Хаффман, Джон К.; Кристу, Джордж (1994). «Синтез, характеристика и молекулярная структура нового комплекса S 2 O Mo(S 2 O) (S 2 CNEt 2 ) 3 ·1/2Et 2 O» (PDF) . Неорганическая химия . 33 (17): 3639–3644. дои : 10.1021/ic00095a005 . ISSN 0020-1669 . Архивировано из оригинала (PDF) 6 ноября 2015 г. Проверено 13 мая 2013 г.
- ^ Лоренц, Инго-Питер; Кулл, Юрген (1986). «Комплексная стабилизация диоксида серы при фрагментации S -оксида тирана на бис (трифенилфосфан) платине (0)». Angewandte Chemie International Edition на английском языке . 25 (3): 261–262. дои : 10.1002/anie.198602611 . ISSN 0570-0833 .
- ^ Jump up to: а б Шмид, Гюнтер; Риттер, Гюнтер; Дебаердемакер, Тони (1975). «Сложная химия низших оксидов серы. II. Моноксид серы и диоксид серы как комплексные лиганды» [Сложная химия низших оксидов серы. II Моноксид серы и диоксид серы как комплексные лиганды. Химические отчеты . 108 (9): 3008–3013. дои : 10.1002/cber.19751080921 . ISSN 0009-2940 .
- ^ Нагата, К.; Такеда, Н.; Токито, Н. (2003). «Необычное окисление дихалькогенидных комплексов платины». Химические письма . 32 (2): 170–171. дои : 10.1246/кл.2003.170 . ISSN 0366-7022 .
- ^ Клементс, Тодд Г.; Ханс-Юрген Дейерль; Роберт Э. Континетти (2002). «Динамика диссоциативного фотоотрыва S
22О −
2 " (PDF) . Журнал физической химии A. 106 ( 2): 279–284. Бибкод : 2002JPCA..106..279C . doi : 10.1021/jp013329v . ISSN 1089-5639 . Проверено 13 мая 2013 г.