Индий
 | ||||||||||||||||||||||||||
| Индий | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | / ˈ ɪ n d i ə m / | |||||||||||||||||||||||||
| Появление | серебристый блестящий серый | |||||||||||||||||||||||||
| Стандартный атомный вес А р °(В) | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
| Индий в таблице Менделеева | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
| Атомный номер ( Z ) | 49 | |||||||||||||||||||||||||
| Группа | группа 13 (группа бора) | |||||||||||||||||||||||||
| Период | период 5 | |||||||||||||||||||||||||
| Блокировать | p-блок | |||||||||||||||||||||||||
| Электронная конфигурация | [ Кр ]4д 10 5 с 2 5 пенсов 1 | |||||||||||||||||||||||||
| Электроны на оболочку | 2, 8, 18, 18, 3 | |||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||
| Фаза в СТП | твердый | |||||||||||||||||||||||||
| Температура плавления | 429,7485 К (156,5985 °С, 313,8773 °F) | |||||||||||||||||||||||||
| Точка кипения | 2345 К (2072 °С, 3762 °F) | |||||||||||||||||||||||||
| Плотность (при 20°С) | 7,290 г/см 3 [3] | |||||||||||||||||||||||||
| в жидком состоянии (при температуре плавления ) | 7,02 г/см 3 | |||||||||||||||||||||||||
| Тройная точка | 429,7445 К, ~1 кПа [4] | |||||||||||||||||||||||||
| Теплота плавления | 3,281 кДж/моль | |||||||||||||||||||||||||
| Теплота испарения | 231,8 кДж/моль | |||||||||||||||||||||||||
| Молярная теплоемкость | 26,74 Дж/(моль·К) | |||||||||||||||||||||||||
Давление пара
| ||||||||||||||||||||||||||
| Атомные свойства | ||||||||||||||||||||||||||
| Стадии окисления | −5, −2, −1, 0, [5] +1, +2, +3 [6] ( амфотерный оксид) | |||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 1,78. | |||||||||||||||||||||||||
| Энергии ионизации |
| |||||||||||||||||||||||||
| Атомный радиус | эмпирический: 167 вечера | |||||||||||||||||||||||||
| Ковалентный радиус | 142±17:00 | |||||||||||||||||||||||||
| Радиус Ван-дер-Ваальса | 193 вечера | |||||||||||||||||||||||||
| Другие объекты недвижимости | ||||||||||||||||||||||||||
| Естественное явление | первобытный | |||||||||||||||||||||||||
| Кристаллическая структура | объемно-центрированный тетрагонал ( tI2 ) | |||||||||||||||||||||||||
| Константы решетки | а = 15:25,16 с = 494,71 вечера (при 20 ° C) [3] | |||||||||||||||||||||||||
| Тепловое расширение | 32.2 × 10 −6 /К (при 20 °С) [а] | |||||||||||||||||||||||||
| Теплопроводность | 81,8 Вт/(м⋅К) | |||||||||||||||||||||||||
| Электрическое сопротивление | 83,7 нОм⋅м (при 20 °C) | |||||||||||||||||||||||||
| Магнитный заказ | диамагнитный [7] | |||||||||||||||||||||||||
| Молярная магнитная восприимчивость | −64.0 × 10 −6 см 3 /моль (298 К) [8] | |||||||||||||||||||||||||
| Модуль Юнга | 11 ГПа | |||||||||||||||||||||||||
| Скорость звука тонкого стержня | 1215 м/с (при 20 °C) | |||||||||||||||||||||||||
| Твердость по шкале Мооса | 1.2 | |||||||||||||||||||||||||
| Твердость по Бринеллю | 8,8–10,0 МПа | |||||||||||||||||||||||||
| Номер CAS | 7440-74-6 | |||||||||||||||||||||||||
| История | ||||||||||||||||||||||||||
| Открытие | Фердинанд Райх и Иероним Теодор Рихтер (1863) | |||||||||||||||||||||||||
| Первая изоляция | Иероним Теодор Рихтер (1864) | |||||||||||||||||||||||||
| Изотопы индия | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
Индий — химический элемент ; он имеет символ In и атомный номер 49. Это серебристо-белый постпереходный металл и один из самых мягких элементов. По химическому составу индий подобен галлию и таллию , а его свойства в значительной степени являются промежуточными между ними. [10] Он был открыт в 1863 году Фердинандом Райхом и Иеронимом Теодором Рихтером с помощью спектроскопических методов и назван в честь синей линии индиго в его спектре. [11]
Индий — технологически важный элемент, используемый в основном в производстве плоских дисплеев в виде оксида индия и олова (ITO) , прозрачного и проводящего покрытия, наносимого на стекло. [12] [13] [14] Индий также используется в полупроводниковой промышленности . [15] в легкоплавких металлических сплавах, таких как припои и высоковакуумные уплотнения из мягких металлов. Его получают исключительно как побочный продукт при переработке руд других металлов, главным образом сфалерита и других сульфидных цинковых руд . [16]
Индий не играет биологической роли, а его соединения токсичны при вдыхании или попадании в кровоток, хотя при проглатывании они плохо всасываются. [17] [18]
Этимология
[ редактировать ]Название происходит от латинского слова indicum, означающего фиолетовый или индиго . [19]
Характеристики
[ редактировать ]Физический
[ редактировать ]
Индий — блестящий серебристо-белый, очень пластичный постпереходный металл с ярким блеском . [20] Он настолько мягкий ( твердость по шкале Мооса 1,2), что его можно резать ножом, и при растирании на бумаге он оставляет видимые линии, как карандаш. [21] Он входит в 13-ю группу , периодической таблицы и его свойства в основном занимают промежуточное положение между его вертикальными соседями галлием и таллием . Как и олово пронзительный крик , при сгибании индия слышен – потрескивающий звук из-за двойникования кристаллов . [20] Как и галлий, индий способен смачивать стекло. Как и оба, индий имеет низкую температуру плавления - 156,60 ° C (313,88 ° F); выше, чем у его более легкого гомолога галлия, но ниже, чем у его более тяжелого гомолога таллия, и ниже, чем у олова. [22] Температура кипения составляет 2072 ° C (3762 ° F), что выше, чем у таллия, но ниже, чем у галлия, в отличие от общей тенденции температур плавления, но аналогично тенденциям понижения других групп постпереходных металлов из-за слабости металлической связи с небольшим количеством делокализованных электронов . [23]
Плотность индия 7,31 г/см. 3 , также больше, чем у галлия, но ниже, чем у таллия. Ниже критической температуры 3,41 К индий становится сверхпроводником . Индий кристаллизуется в объемноцентрированной тетрагональной кристаллической системе в пространственной группе I 4/ ммм ( параметры решетки : а = 325 пм , с = 495 пм): [22] это слегка искаженная гранецентрированная кубическая структура, где каждый атом индия имеет четырех соседей на расстоянии 324 пм и восемь соседей чуть дальше (336 пм). [24] Индий растворяется в жидкой ртути лучше, чем любой другой металл (более 50 массовых процентов индия при 0 ° C). [25] Индий демонстрирует пластичную вязкопластическую реакцию, которая, как выяснилось, не зависит от размера при растяжении и сжатии. Однако он имеет размерный эффект при изгибе и вдавливании, связанный с масштабом длины порядка 50–100 мкм. [26] значительно больше по сравнению с другими металлами.
Химическая
[ редактировать ]Индий имеет 49 электронов с электронной конфигурацией [ Kr ]4d. 10 5 с 2 5 пенсов 1 . В соединениях индий чаще всего отдает три крайних электрона, превращаясь в индий (III). 3+ . В некоторых случаях пара 5s-электронов не отдается, в результате чего образуется индий(I), In + . Стабилизация одновалентного состояния объясняется эффектом инертной пары , при котором релятивистские эффекты стабилизируют 5s-орбиталь, наблюдаемую в более тяжелых элементах. индия Таллий (более тяжелый гомолог ) демонстрирует еще более сильный эффект, в результате чего окисление до таллия (I) более вероятно, чем до таллия (III), [27] тогда как галлий (более легкий гомолог индия) обычно показывает только степень окисления +3. Таким образом, хотя таллий (III) является умеренно сильным окислителем , индий (III) им не является, а многие соединения индия (I) являются мощными восстановителями . [28] Хотя энергия, необходимая для включения s-электронов в химическую связь, у индия самая низкая среди металлов группы 13, энергии связи уменьшаются вниз по группе, так что у индия энергия, выделяемая при образовании двух дополнительных связей и достижении состояния +3, не увеличивается. всегда достаточно, чтобы перевесить энергию, необходимую для участия 5s-электронов. [29] Оксид и гидроксид индия (I) являются более основными, а оксид и гидроксид индия (III) более кислыми. [29]
Ряд стандартных электродных потенциалов в зависимости от исследуемой реакции: [30] сообщается для индия, что отражает пониженную стабильность степени окисления +3: [24]
В 2+ + и − ⇌ В + И 0 = −0.40 V В 3+ + и − ⇌ В 2+ И 0 = −0.49 V В 3+ + 2 и − ⇌ В + И 0 = −0.443 V В 3+ + 3 и − ⇌ В И 0 = −0.3382 V В + + и − ⇌ В И 0 = −0.14 V
Металлический индий не реагирует с водой, но окисляется более сильными окислителями, такими как галогены, с образованием соединений индия (III). Он не образует борида , силицида или карбида , а гидрид InH 3 в лучшем случае имеет временное существование в эфирных растворах при низких температурах, будучи достаточно нестабильным, чтобы самопроизвольно полимеризоваться без координации. [28] Индий является довольно основным в водных растворах, проявляя лишь незначительные амфотерные характеристики и в отличие от своих более легких гомологов алюминия и галлия, он нерастворим в водных щелочных растворах. [31]
изотопы
[ редактировать ]Индий имеет 39 известных изотопов с массовым числом от 97 до 135. Только два изотопа встречаются в природе в виде первичных нуклидов : индий-113, единственный стабильный изотоп , и индий-115, период полураспада которого составляет 4,41 × 10. 14 лет, что на четыре порядка превышает возраст Вселенной и почти в 30 000 раз превышает период полураспада тория-232 . [32] Период полураспада 115 Это очень долго, потому что бета-распад до 115 Sn запрещен по спину . [33] Индий-115 составляет 95,7% всего индия. Индий — один из трех известных элементов (остальные — теллур и рений ), стабильный изотоп которых менее распространен в природе, чем долгоживущие первичные радиоизотопы. [34]
Самый стабильный искусственный изотоп — индий-111 с периодом полураспада примерно 2,8 дня. Все остальные изотопы имеют период полураспада менее 5 часов. Индий также имеет 47 метасостояний, среди которых индий-114m1 (период полураспада около 49,51 дня) является наиболее стабильным, более стабильным, чем основное состояние любого изотопа индия, кроме первичного. Весь распад происходит путем изомерного перехода . Изотопы индия легче, чем 113 Преимущественно распад происходит за счет захвата электронов или эмиссии позитронов с образованием изотопов кадмия , тогда как изотопы индия тяжелее, чем 113 Преимущественно распадается через бета-минус-распад с образованием изотопов олова. [32]
Соединения
[ редактировать ]Индий(III)
[ редактировать ]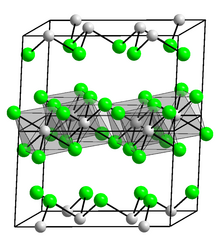
Оксид индия(III) In 2 O 3 образуется при сгорании металлического индия на воздухе или при нагревании гидроксида или нитрата. [35] In 2 O 3 имеет структуру, подобную оксиду алюминия , и является амфотерным, то есть способен реагировать как с кислотами, так и с основаниями. Индий реагирует с водой с образованием растворимого гидроксида индия (III) , который также является амфотерным; со щелочами с получением индатов(III); и с кислотами для получения солей индия (III):
- In(OH) 3 + 3 HCl → InCl 3 + 3 H 2 O
аналогичные сескви-халькогениды с серой , селеном и теллуром . Известны также [36] Индий образует ожидаемые тригалогениды . Хлорирование, бромирование и йодирование In дают бесцветные InCl 3 , InBr 3 и желтый InI 3 . Соединения представляют собой кислоты Льюиса , чем-то похожие на более известные тригалогениды алюминия. Опять же, как и родственное соединение алюминия, InF 3 является полимерным. [37]
Прямая реакция индия с пниктогенами приводит к образованию серых или полуметаллических полупроводников III–V . Многие из них медленно разлагаются во влажном воздухе, что обусловливает необходимость бережного хранения полупроводниковых соединений во избежание контакта с атмосферой. Нитрид индия легко подвергается воздействию кислот и щелочей. [38]
Индий(I)
[ редактировать ]Соединения индия (I) встречаются нечасто. Хлорид, бромид и йодид имеют глубокую окраску, в отличие от исходных тригалогенидов, из которых они получены. Фторид известен только как нестабильное газообразное соединение. [39] Черный порошок оксида индия (I) получается при разложении оксида индия (III) при нагревании до 700 ° C. [35]
Другие степени окисления
[ редактировать ]Реже индий образует соединения со степенью окисления +2 и даже дробными степенями окисления. Обычно такие материалы имеют связь In-In, особенно в галогенидах In 2 X 4 и [In 2 X 6 ]. 2− , [40] и различные субхалькогениды, такие как In 4 Se 3 . [41] Известно несколько других соединений, сочетающих в себе индий (I) и индий (III), например In я 6 (В III Cl6 ) Cl3 , [42] В я 5 (в III Бр 4 ) 2 (В III Бр 6 ), [43] и в я В III Бр 4 . [40]
Индийорганические соединения
[ редактировать ]Индийорганические соединения содержат связи In–C. Большинство из них являются производными In(III), но циклопентадиенилиндий(I) является исключением. Это было первое известное индийорганическое соединение. [44] и является полимерным, состоящим из зигзагообразных цепочек чередующихся атомов индия и циклопентадиенильных комплексов . [45] Пожалуй, самым известным индийорганическим соединением является триметилиндий In(CH 3 ) 3 , используемый для изготовления некоторых полупроводниковых материалов. [46] [47]
История
[ редактировать ]В 1863 году немецкие химики Фердинанд Райх и Иероним Теодор Рихтер тестировали руду из рудников вокруг Фрайберга, Саксония . Они растворяли минералы пирит , арсенопирит , галенит и сфалерит в соляной кислоте и перегоняли сырой хлорид цинка . Райх, который был дальтоником , нанял Рихтера в качестве помощника для обнаружения цветных спектральных линий. Зная, что руды этого региона иногда содержат таллий , они искали зеленые линии спектра излучения таллия. Вместо этого они обнаружили ярко-синюю линию. Поскольку эта синяя линия не соответствовала ни одному известному элементу, они предположили, что в минералах присутствует новый элемент. Они назвали элемент индием по цвету индиго , наблюдаемому в его спектре, в честь латинского indicum , что означает « Индийский ». [48] [11] [49] [50]
Рихтер продолжил изолировать металл в 1864 году. [51] Слиток массой 0,5 кг (1,1 фунта) был представлен на Всемирной выставке 1867 года. [52] Позже Райх и Рихтер поссорились, когда последний заявил, что является единственным первооткрывателем. [50]
возникновение
[ редактировать ]
Индий создается в результате длительного (до тысяч лет) s-процесса (медленного захвата нейтронов) в звездах малой и средней массы (диапазон масс от 0,6 до 10 масс Солнца ). Когда атом серебра-109 захватывает нейтрон, он превращается в серебро-110, которое затем подвергается бета-распаду и становится кадмием-110. Захватывая дальнейшие нейтроны, он превращается в кадмий-115, который распадается до индия-115 в результате еще одного бета-распада . Это объясняет, почему радиоактивного изотопа больше, чем стабильного. [53] Стабильный изотоп индия, индий-113, является одним из p-ядер , происхождение которого до конца не изучено; хотя известно, что индий-113 производится непосредственно в s- и r-процессах (быстрый захват нейтронов), а также как дочка очень долгоживущего кадмия-113, период полураспада которого составляет около восьми квадриллионов лет, это не может объяснить весь индий-113. [54] [55]
Индий является 68-м по распространенности элементом в земной коре ( около 50 частей на миллиард) . Это похоже на изобилие в земной коре серебра , висмута и ртути . Он очень редко образует собственные минералы или встречается в элементарной форме. менее 10 минералов индия, таких как рокезит (CuInS 2 ), и ни один из них не встречается в концентрациях, достаточных для экономической добычи. Известно [56] Вместо этого индий обычно является микроэлементом более распространенных рудных минералов, таких как сфалерит и халькопирит . [57] [58] Из них его можно извлечь в качестве побочного продукта при плавке. [16] Хотя обогащение индия в этих месторождениях велико по сравнению с его содержанием в земной коре, при нынешних ценах оно недостаточно для поддержки добычи индия как основного продукта. [56]
Существуют разные оценки количества индия, содержащегося в рудах других металлов. [59] [60] Однако эти количества невозможно извлечь без добычи исходных материалов (см. «Производство и доступность»). Таким образом, доступность индия в основном определяется скоростью добычи этих руд, а не их абсолютным количеством. Этот аспект часто забывается в текущих дебатах, например, группой Гределя в Йельском университете в своих оценках критичности. [61] объясняя парадоксально малое время истощения, на которое ссылаются некоторые исследования. [62] [16]
Производство и доступность
[ редактировать ]
Индий производится исключительно как побочный продукт при переработке руд других металлов. Его основным источником являются сульфидно-цинковые руды, в которых он преимущественно содержится сфалеритом. [16] Незначительные количества также добываются из сульфидных медных руд. Во время процесса обжига-выщелачивания-электролиза при выплавке цинка индий накапливается в богатых железом остатках. Из них его можно извлечь разными способами. Его также можно извлечь непосредственно из технологических растворов. Дальнейшая очистка осуществляется электролизом . [64] Точный процесс зависит от режима работы плавильного завода. [20] [16]
Его статус побочного продукта означает, что производство индия ограничено количеством сульфидных цинковых (и медных) руд, добываемых каждый год. Поэтому его наличие необходимо обсуждать с точки зрения потенциала поставок. Потенциал предложения побочного продукта определяется как количество, которое экономически можно извлечь из исходных материалов в год при текущих рыночных условиях (т. е. технологии и цене). [65] Запасы и ресурсы не имеют значения для побочной продукции, поскольку их невозможно извлечь независимо от основной продукции. [16] По последним оценкам, потенциал поставок индия составляет как минимум 1300 т/год из сульфидных цинковых руд и 20 т/год из сульфидных медных руд. [16] Эти цифры значительно превышают текущий объем производства (655 т в 2016 году). [66] Таким образом, значительное будущее увеличение производства побочной продукции индия будет возможно без значительного увеличения производственных затрат или цен. Средняя цена на индий в 2016 году составила 240 долларов США /кг по сравнению с 705 долларами США /кг в 2014 году. [67]
Китай является ведущим производителем индия (290 тонн в 2016 году), за ним следуют Южная Корея (195 тонн), Япония (70 тонн) и Канада (65 тонн). [66] Нефтеперерабатывающий завод Teck Resources в Трейле, Британская Колумбия , является крупным производителем индия с единственным источником, с объемом производства 32,5 тонны в 2005 году, 41,8 тонны в 2004 году и 36,1 тонны в 2003 году.
Основным потреблением индия во всем мире является производство ЖК-дисплеев . Спрос быстро рос с конца 1990-х по 2010 год благодаря популярности компьютерных ЖК-мониторов и телевизоров, на которые сейчас приходится 50% потребления индия. [14] Повышение эффективности производства и переработки (особенно в Японии) поддерживают баланс между спросом и предложением. По данным ЮНЕП , уровень переработки индия по окончании срока службы составляет менее 1%. [68]
Приложения
[ редактировать ]
В 1924 году было обнаружено, что индий обладает ценным свойством стабилизации цветных металлов , и это стало первым значительным применением этого элемента. [69] Первым крупномасштабным применением индия стало покрытие подшипников высокопроизводительных авиационных двигателей во время Второй мировой войны для защиты от повреждений и коррозии ; это больше не является основным использованием элемента. [64] Новые применения были найдены в легкоплавких сплавах , припоях и электронике . В 1950-х годах крошечные шарики индия использовались для изготовления эмиттеров и коллекторов PNP- транзисторов со сплавным переходом . В середине и конце 1980-х годов большой интерес вызвала разработка на основе фосфида индия полупроводников и тонких пленок оксида индия и олова для жидкокристаллических дисплеев (ЖКД). К 1992 году применение тонких пленок стало крупнейшим конечным применением. [70] [71]
Оксид индия (III) и оксид индия-олова (ITO) используются в качестве прозрачного проводящего покрытия на стеклянных подложках в электролюминесцентных панелях. [72] Оксид индия и олова используется в качестве светофильтра в натриевых лампах низкого давления . Инфракрасное излучение отражается обратно в лампу, что повышает температуру внутри трубки и улучшает работу лампы. [71]
Индий имеет множество применений, связанных с полупроводниками . Некоторые соединения индия, такие как антимонид индия и фосфид индия , [73] являются полупроводниками с полезными свойствами: одним из прекурсоров обычно является триметилиндий (TMI), который также используется в качестве легирующей примеси II – VI в полупроводниковых соединениях . [74] InAs и InSb используются для низкотемпературных транзисторов, а InP — для высокотемпературных. [64] Сложные полупроводники InGaN и InGaP используются в светоизлучающих диодах (LED) и лазерных диодах. [75] Индий используется в фотоэлектрической энергетике в качестве полупроводникового селенида меди, индия, галлия (CIGS), также называемого солнечными элементами CIGS , типом тонкопленочных солнечных элементов второго поколения . [76] Индий используется в транзисторах с биполярным переходом PNP с германием : при пайке при низкой температуре индий не оказывает воздействия на германий. [64]

Индиевая проволока используется в качестве вакуумного уплотнения и теплопроводника в криогенике и сверхвысоком вакууме , а также в таких производственных приложениях, как прокладки , которые деформируются для заполнения зазоров. [77] Благодаря большой пластичности и адгезии к металлам листы индия иногда применяют для холодной пайки в СВЧ- схемах и соединениях волноводов , где прямая пайка затруднена. Индий является ингредиентом галлинстана из сплава галлий-индий-олово , который является жидким при комнатной температуре и заменяет ртуть в некоторых термометрах . [78] Другие сплавы индия с висмутом , кадмием , свинцом и оловом , имеющие более высокие, но все же низкие температуры плавления (от 50 до 100 °C), используются в спринклерных системах пожаротушения и регуляторах тепла. [64]
Индий является одним из многих заменителей ртути в щелочных батареях, предотвращающих цинка коррозию и выделение газообразного водорода . [79] Индий добавляют в некоторые сплавы стоматологической амальгамы , чтобы уменьшить поверхностное натяжение ртути и обеспечить меньшее количество ртути и более легкое амальгамирование. [80]
Высокое сечение захвата тепловых нейтронов Индием делает его пригодным для использования в стержнях управления ядерных реакторов , обычно в сплаве, состоящем из 80% серебра , 15% индия и 5% кадмия . [81] В ядерной технике (n,n') реакции 113 В и 115 В используются для определения величин нейтронных потоков. [82]
В 2009 году профессор Мас Субраманиан и бывший аспирант Эндрю Смит из Университета штата Орегон обнаружили, что индий можно объединить с иттрием и марганцем, образуя интенсивно синий , нетоксичный, инертный, устойчивый к выцветанию пигмент пигмент YInMn blue , первый новый неорганический . синий пигмент открыт через 200 лет. [83]
Биологическая роль и меры предосторожности
[ редактировать ]| Опасности | |
|---|---|
| СГС Маркировка : | |
 | |
| Предупреждение | |
| Х302 , Х312 , Х315 , Х319 , Х332 , Х335 | |
| П261 , П280 , П305+П351+П338 [84] | |
| NFPA 704 (огненный алмаз) | |
Индий не играет метаболической роли ни в одном организме. Подобно солям алюминия, ионы индия (III) могут быть токсичными для почек при инъекционном введении. [18] Оксид индия-олова и фосфид индия вредят легочной и иммунной системам, преимущественно за счет ионов индия, [85] хотя гидратированный оксид индия более чем в сорок раз токсичен при инъекции, если судить по количеству введенного индия. [18] Радиоактивный индий-111 (в очень небольших количествах по химическому составу) используется в ядерной медицины испытаниях в качестве радиофармпрепарата для отслеживания движения меченых белков и лейкоцитов в организме. [86] [87] Соединения индия в основном не всасываются при приеме внутрь и лишь умеренно всасываются при вдыхании; они, как правило, временно сохраняются в мышцах , коже и костях , прежде чем выводятся из организма, а биологический период полураспада индия у человека составляет около двух недель. [88]
Люди могут подвергаться воздействию индия на рабочем месте при вдыхании, проглатывании, контакте с кожей и глазами. Индиумное легкое - заболевание легких, характеризующееся легочным альвеолярным протеинозом и фиброзом легких, впервые описанное японскими исследователями в 2003 году. По состоянию на 2010 год. [update]было описано 10 случаев, хотя более чем у 100 рабочих, работающих с индием, были зарегистрированы респираторные нарушения. [17] Национальный институт безопасности и гигиены труда установил рекомендуемый предел воздействия (REL) 0,1 мг/м. 3 более восьмичасового рабочего дня. [89]
См. также
[ редактировать ]Примечания
[ редактировать ]- ^ Тепловое расширение анизотропно : параметры (при 20 ° C) для каждой оси кристалла составляют α a = 53,2 × 10. −6 /K, α c = −9,75 × 10 −6 /K, а α среднее = α V /3 = 32,2 × 10. −6 /К. [3]
Ссылки
[ редактировать ]- ^ «Стандартные атомные массы: Индий» . ЦИАВ . 2011.
- ^ Прохаска, Томас; Ирргехер, Йоханна; Бенефилд, Жаклин; Бёлке, Джон К.; Чессон, Лесли А.; Коплен, Тайлер Б.; Дин, Типинг; Данн, Филип Дж. Х.; Грёнинг, Манфред; Холден, Норман Э.; Мейер, Харро Эй Джей (04 мая 2022 г.). «Стандартные атомные веса элементов 2021 (Технический отчет ИЮПАК)» . Чистая и прикладная химия . дои : 10.1515/pac-2019-0603 . ISSN 1365-3075 .
- ^ Jump up to: а б с Арбластер, Джон В. (2018). Некоторые значения кристаллографических свойств элементов . Парк материалов, Огайо: ASM International. ISBN 978-1-62708-155-9 .
- ^ Мангум, BW (1989). «Определение температуры замерзания индия и температур тройной точки». Метрология . 26 (4): 211. Бибкод : 1989Метро..26..211М . дои : 10.1088/0026-1394/26/4/001 .
- ^ Обнаружены нестабильные карбонилы и кластеры In(0), см. [1] , с. 6.
- ^ Гулой А.М.; Корбетт, доктор медицинских наук (1996). «Синтез, структура и соединение двух германидов лантана и индия с новой структурой и свойствами». Неорганическая химия . 35 (9): 2616–22. дои : 10.1021/ic951378e . ПМИД 11666477 .
- ^ Лиде, Д.Р., изд. (2005). «Магнитная восприимчивость элементов и неорганических соединений». Справочник CRC по химии и физике (PDF) (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5 .
- ^ Уэст, Роберт (1984). CRC, Справочник по химии и физике . Бока-Ратон, Флорида: Издательство компании Chemical Rubber Company. стр. E110. ISBN 0-8493-0464-4 .
- ^ Кондев, ФГ; Ван, М.; Хуанг, WJ; Наими, С.; Ауди, Г. (2021). «Оценка ядерных свойств NUBASE2020» (PDF) . Китайская физика C . 45 (3): 030001. doi : 10.1088/1674-1137/abddae .
- ^ В.М. Хейнс (2010). Дэвид Р. Лид (ред.). Справочник CRC по химии и физике: Готовый справочник химических и физических данных . ЦРК Пресс. ISBN 978-1-4398-2077-3 .
- ^ Jump up to: а б Венецкий, С. (1971). "Индий". Металлург . 15 (2): 148–150. дои : 10.1007/BF01088126 .
- ^ Ван, Чжаокуй; Нака, Сигэки; Окада, Хироюки (30 ноября 2009 г.). «Влияние рисунка ITO на надежность органических светоизлучающих устройств» . Тонкие твердые пленки . 518 (2): 497–500. Бибкод : 2009TSF...518..497W . дои : 10.1016/j.tsf.2009.07.029 . ISSN 0040-6090 .
- ^ Чен, Чжансянь; Ли, Ваньчао; Ли, Ран; Чжан, Юньфэн; Сюй, Гоцинь; Ченг, Хансонг (28 октября 2013 г.). «Изготовление высокопрозрачных и проводящих тонких пленок оксида индия-олова с высокой добротностью методом обработки раствора» . Ленгмюр . 29 (45): 13836–13842. дои : 10.1021/la4033282 . ISSN 0743-7463 . ПМИД 24117323 .
- ^ Jump up to: а б «Цена на индий поддерживается спросом на ЖК-дисплеи и новыми способами использования металла» . Геология.com . Архивировано из оригинала (PDF) 21 декабря 2007 г. Проверено 26 декабря 2007 г.
- ^ Нирмал, Д.; Аджаян, Дж. (01 января 2019 г.), Кошик, Браджеш Кумар (ред.), «Глава 3 - Транзисторы с высокой подвижностью электронов на основе InP для высокочастотных приложений» , Nanoelectronics , Advanced Nanomaterials, Elsevier, стр. 95–114, doi : 10.1016/b978-0-12-813353-8.00012-9 , ISBN 978-0-12-813353-8 , получено 8 декабря 2023 г.
- ^ Jump up to: а б с д и ж г Френцель, Макс; Миколайчак, Клэр; Рейтер, Маркус А.; Гутцмер, Йенс (июнь 2017 г.). «Количественная оценка относительной доступности металлов-побочных продуктов высоких технологий - примеры галлия, германия и индия» . Ресурсная политика . 52 : 327–335. Бибкод : 2017RePol..52..327F . doi : 10.1016/j.resourpol.2017.04.008 .
- ^ Jump up to: а б Саулер, Маор; Гулати, Мриду (декабрь 2012 г.). «Недавно выявленные профессиональные и экологические причины хронических терминальных заболеваний дыхательных путей и паренхиматозных заболеваний легких» . Клиники грудной медицины . 33 (4): 667–680. дои : 10.1016/j.ccm.2012.09.002 . ПМЦ 3515663 . ПМИД 23153608 .
- ^ Jump up to: а б с Кастроново, ФП; Вагнер, HN (октябрь 1971 г.). «Факторы, влияющие на токсичность элемента Индий» . Британский журнал экспериментальной патологии . 52 (5): 543–559. ПМК 2072430 . ПМИД 5125268 .
- ^ Королевское химическое общество, https://www.rsc.org/. Архивировано 20 апреля 2021 г. в Wayback Machine.
- ^ Jump up to: а б с Альфантази, AM; Москалык, Р.Р. (2003). «Обработка индия: обзор». Минеральное машиностроение . 16 (8): 687–694. Бибкод : 2003MiEng..16..687A . дои : 10.1016/S0892-6875(03)00168-7 .
- ^ Биндер, Гарри Х. (1999). Лексикон химических элементов (на немецком языке). С. Хирзель Верлаг. ISBN 978-3-7776-0736-8 .
- ^ Jump up to: а б Дин, Джон А. (523). Справочник Ланге по химии (Пятнадцатое изд.). McGraw-Hill, Inc. ISBN 978-0-07-016190-0 .
- ^ Гринвуд и Эрншоу, с. 222
- ^ Jump up to: а б Гринвуд и Эрншоу, с. 252
- ^ Окамото, Х. (2012). «Фазовая диаграмма Hg-In». Журнал фазового равновесия и диффузии . 33 (2): 159–160. дои : 10.1007/s11669-012-9993-3 . S2CID 93043767 .
- ^ Илиев, ИП; Чен, X.; Патан, М.В.; Тагариелли, В.Л. (23 января 2017 г.). «Измерения механического отклика индия и его размерной зависимости при изгибе и вдавливании». Материаловедение и инженерия: А. 683 : 244–251. дои : 10.1016/j.msea.2016.12.017 . hdl : 10044/1/43082 .
- ^ Холлеман, Арнольд Ф.; Виберг, Эгон; Виберг, Нильс (1985). «Таллий». Учебник неорганической химии (на немецком языке) (91–100 изд.). Вальтер де Грюйтер. стр. 892–893. ISBN 978-3-11-007511-3 .
- ^ Jump up to: а б Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Jump up to: а б Гринвуд и Эрншоу, с. 256
- ^ Хейнс, Уильям М., изд. (2011). Справочник CRC по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press . п. 8.20. ISBN 1-4398-5511-0 .
- ^ Гринвуд и Эрншоу, с. 255
- ^ Jump up to: а б Ауди, Жорж; Берсильон, Оливье; Блашо, Жан; Вапстра, Аалдерт Хендрик (2003), « Оценка NUBASE свойств ядра и распада» , Nuclear Physics A , 729 : 3–128, Бибкод : 2003NuPhA.729....3A , doi : 10.1016/j.nuclphysa.2003.11 .001
- ^ Дворницкий Р.; Шимкович, Ф. (13–16 июня 2011 г.). «Второй уникальный запрещенный β-распад 115 In и масса нейтрино». AIP Conf. Proc . AIP Conference Proceedings. 1417 (33): 33. Bibcode : 2011AIPC.1417...33D . doi : 10.1063/1.3671032 .
- ^ «Периодическая таблица изотопов ИЮПАК» (PDF) . ciaaw.org . ИЮПАК . 1 октября 2013 г. Архивировано (PDF) из оригинала 14 февраля 2019 г. . Проверено 21 июня 2016 г.
- ^ Jump up to: а б Энтони Джон Даунс (1993). Химия алюминия, галлия, индия и таллия . Спрингер. ISBN 978-0-7514-0103-5 .
- ^ Гринвуд и Эрншоу, с. 286
- ^ Гринвуд и Эрншоу, стр. 263–7.
- ^ Гринвуд и Эрншоу, с. 288
- ^ Гринвуд и Эрншоу, стр. 270–1.
- ^ Jump up to: а б Синклер, Ян; Уорролл, Ян Дж. (1982). «Нейтральные комплексы дигалогенидов индия» . Канадский химический журнал . 60 (6): 695–698. дои : 10.1139/v82-102 .
- ^ Гринвуд и Эрншоу, с. 287
- ^ Бек, Хорст Филипп; Вильгельм, Дорис (1991). «In7Cl9 — новое «старое» соединение в системе In-Cl». Angewandte Chemie International Edition на английском языке . 30 (7): 824–825. дои : 10.1002/anie.199108241 .
- ^ Дронсковский, Ричард (1995). «Синтез, структура и распад In4Br7». Angewandte Chemie International Edition на английском языке . 34 (10): 1126–1128. дои : 10.1002/anie.199511261 .
- ^ Фишер, Э.О.; Хофманн, HP (1957). «Металл циклопентадиенилы индия». Прикладная химия (на немецком языке). 69 (20): 639–640. Бибкод : 1957АнгЧ..69..639Ф . дои : 10.1002/anie.19570692008 .
- ^ Бичли ОТ; Пазик Ю.С.; Глассман Т.Э.; Черчилль М.Р.; Феттингер Дж. К.; Блом Р. (1988). «Синтез, характеристика и структурные исследования In(C 5 H 4 Me) методами рентгеновской дифракции и дифракции электронов, а также повторное исследование кристаллического состояния In (C 5 H 5 ) с помощью рентгеновских дифракционных исследований». Металлоорганические соединения . 7 (5): 1051–1059. дои : 10.1021/om00095a007 .
- ^ Шенаи, Део В.; Тиммонс, Майкл Л.; Дикарло, Рональд Л.; Лемна, Грегори К.; Стенник, Роберт С. (2003). «Корреляция уравнения давления пара и свойств пленок с чистотой триметилиндия для соединений III – V, выращенных методом MOVPE». Журнал роста кристаллов . 248 : 91–98. Бибкод : 2003JCrGr.248...91S . дои : 10.1016/S0022-0248(02)01854-7 .
- ^ Шенаи, Деодатта В.; Тиммонс, Майкл Л.; Дикарло, Рональд Л.; Марсман, Чарльз Дж. (2004). «Корреляция свойств пленок и пониженных концентраций примесей в источниках для III/V-MOVPE с использованием триметилиндия высокой чистоты и третичного бутилфосфина». Журнал роста кристаллов . 272 (1–4): 603–608. Бибкод : 2004JCrGr.272..603S . дои : 10.1016/j.jcrysgro.2004.09.006 .
- ^ Райх, Ф.; Рихтер, Т. (1863). «Об индии» . Журнал практической химии (на немецком языке). 90 (1): 172–176. дои : 10.1002/prac.18630900122 . S2CID 94381243 . Архивировано из оригинала 2 февраля 2020 г. Проверено 30 июня 2019 г.
- ^ Гринвуд и Эрншоу, с. 244
- ^ Jump up to: а б Уикс, Мария Эльвира (1932). «Открытие элементов: XIII. Некоторые спектроскопические исследования» . Журнал химического образования . 9 (8): 1413–1434. Бибкод : 1932JChEd...9.1413W . дои : 10.1021/ed009p1413 . [ постоянная мертвая ссылка ]
- ^ Райх, Ф.; Рихтер, Т. (1864). «Об индии». Журнал практической химии (на немецком языке). 92 (1): 480–485. дои : 10.1002/prac.18640920180 .
- ^ Шварц-Шампера, Ульрих; Герциг, Питер М. (2002). Индий: геология, минералогия и экономика . Спрингер. ISBN 978-3-540-43135-0 .
- ^ Бутройд, AI (2006). «Тяжелые элементы в звездах». Наука . 314 (5806): 1690–1691. дои : 10.1126/science.1136842 . ПМИД 17170281 . S2CID 116938510 .
- ^ Арландини, К.; Кеппелер, Ф.; Висшак, К.; Галлино, Р.; Лугаро, М.; Буссо, М.; Страньеро, О. (1999). «Захват нейтрона в асимптотических звездах ветви гигантов малой массы: поперечные сечения и признаки изобилия». Астрофизический журнал . 525 (2): 886–900. arXiv : astro-ph/9906266 . Бибкод : 1999ApJ...525..886A . дои : 10.1086/307938 . S2CID 10847307 .
- ^ Зс; Кеппелер, Ф.; Тайс, К.; Бельгия, Т.; Йейтс, SW (1994). «Нуклеосинтез в области Cd-In-Sn». Астрофизический журнал . 426 : 357–365. Бибкод : 1994ApJ...426..357N . дои : 10.1086/174071 .
- ^ Jump up to: а б Френцель, Макс (2016). «Распределение галлия, германия и индия в традиционных и нетрадиционных ресурсах - последствия для глобальной доступности (доступна загрузка в формате PDF)» . Исследовательские ворота . дои : 10.13140/rg.2.2.20956.18564 . Архивировано из оригинала 06.10.2018 . Проверено 2 июня 2017 г.
- ^ Френцель, Макс; Хирш, Тамино; Гутцмер, Йенс (июль 2016 г.). «Галлий, германий, индий и другие микроэлементы и второстепенные элементы в сфалерите в зависимости от типа месторождения - метаанализ». Обзоры рудной геологии . 76 : 52–78. Бибкод : 2016ОГРв...76...52Ф . дои : 10.1016/j.oregeorev.2015.12.017 .
- ^ Бахманн, Кай; Френцель, Макс; Краузе, Иоахим; Гутцмер, Йенс (июнь 2017 г.). «Расширенная идентификация и количественная оценка содержащих минералов с помощью анализа изображений на основе сканирующего электронного микроскопа». Микроскопия и микроанализ . 23 (3): 527–537. Бибкод : 2017MiMic..23..527B . дои : 10.1017/S1431927617000460 . ISSN 1431-9276 . ПМИД 28464970 . S2CID 6751828 .
- ^ «Краткий обзор минерального сырья за 2007 год: Индий» (PDF) . Геологическая служба США. Архивировано (PDF) из оригинала 9 мая 2008 г. Проверено 26 декабря 2007 г.
- ^ Вернер, ТТ; Мадд, генеральный менеджер; Джоуитт, С.М. (02 октября 2015 г.). «Индий: ключевые проблемы оценки минеральных ресурсов и долгосрочных поставок от переработки». Прикладная наука о Земле . 124 (4): 213–226. Бибкод : 2015ApEaS.124..213W . дои : 10.1179/1743275815Y.0000000007 . ISSN 0371-7453 . S2CID 128555024 .
- ^ Гредель, Т.Э.; Барр, Рэйчел; Чендлер, Челси; Чейз, Томас; Чой, Джоанн; Кристофферсен, Ли; Фридлендер, Элизабет; Хенли, Клэр; Джун, Кристина (17 января 2012 г.). «Методика определения критичности металлов». Экологические науки и технологии . 46 (2): 1063–1070. Бибкод : 2012EnST...46.1063G . дои : 10.1021/es203534z . ISSN 0013-936X . ПМИД 22191617 .
- ^ Харпер, Э.М.; Кавлак, Гоксин; Бурмейстер, Лара; Экельман, Мэтью Дж.; Эрбис, Серкан; Себастьян Эспиноза, Висенте; Нусс, Филип; Гредель, Т.Э. (1 августа 2015 г.). «Критичность геологического семейства цинка, олова и свинца» . Журнал промышленной экологии . 19 (4): 628–644. Бибкод : 2015JInEc..19..628H . дои : 10.1111/jiec.12213 . ISSN 1530-9290 . S2CID 153380535 . [ постоянная мертвая ссылка ]
- ^ Геологическая служба США - Историческая статистика минерального и материального сырья в Соединенных Штатах ; СТАТИСТИКА ИНДИЯ // Геологическая служба США, 1 апреля 2014 г.
- ^ Jump up to: а б с д и Гринвуд и Эрншоу, с. 247
- ^ Френцель, Макс; Толосана-Дельгадо, Раймон; Гутцмер, Йенс (декабрь 2015 г.). «Оценка потенциала поставок высокотехнологичных металлов – общий метод». Ресурсная политика . 46, Часть 2: 45–58. Бибкод : 2015RePol..46...45F . doi : 10.1016/j.resourpol.2015.08.002 .
- ^ Jump up to: а б Индий - в: Обзоры минеральных ресурсов Геологической службы США (PDF) . Геологическая служба США. 2017. Архивировано (PDF) из оригинала 11 января 2019 г. Проверено 2 июня 2017 г.
- ^ Келли, Т.Д.; Матос, GR (2015). «Историческая статистика минерального и материального сырья в Соединенных Штатах» . Архивировано из оригинала 11 мая 2017 г. Проверено 2 июня 2017 г.
- ^ «Обзоры минеральных ресурсов Геологической службы США за 2011 год» (PDF) . Геологическая служба США и Министерство сельского хозяйства США. Архивировано (PDF) из оригинала 11 января 2019 г. Проверено 2 августа 2011 г.
- ^ Френч, Сидни Дж. (1934). «История индия». Журнал химического образования . 11 (5): 270. Бибкод : 1934JChEd..11..270F . дои : 10.1021/ed011p270 .
- ^ Толчин, Эми К. «Ежегодник минералов 2007: Индий» (PDF) . Геологическая служба США. Архивировано (PDF) из оригинала 31 декабря 2016 г. Проверено 3 декабря 2009 г.
- ^ Jump up to: а б Даунс, Энтони Джон (1993). Химия алюминия, галлия, индия и таллия . Спрингер. стр. 89 и 106. ISBN. 978-0-7514-0103-5 .
- ^ «Электролюминесцентный световой меч» . Архив новостей нанотехнологий . Азонано. 2 июня 2005 года. Архивировано из оригинала 12 октября 2007 года . Проверено 29 августа 2007 г.
- ^ Бахманн, К.Дж. (1981). «Свойства, получение и применение фосфида индия». Ежегодный обзор материаловедения . 11 : 441–484. Бибкод : 1981AnRMS..11..441B . дои : 10.1146/annurev.ms.11.080181.002301 .
- ^ Шенаи, Деодатта В.; Тиммонс, Майкл Л.; ДиКарло младший, Рональд Л.; Марсман, Чарльз Дж. (2004). «Корреляция свойств пленок и пониженных концентраций примесей в источниках для III/V-MOVPE с использованием триметилиндия высокой чистоты и третичного бутилфосфина». Журнал роста кристаллов . 272 (1–4): 603–608. Бибкод : 2004JCrGr.272..603S . дои : 10.1016/j.jcrysgro.2004.09.006 .
- ^ Шуберт, Э. Фред (2003). Светоизлучающие диоды . Издательство Кембриджского университета. п. 16. ISBN 978-0-521-53351-5 .
- ^ Повалла, М.; Диммлер, Б. (2000). «Масштабирование проблем солнечных элементов CIGS». Тонкие твердые пленки . 361–362 (1–2): 540–546. Бибкод : 2000TSF...361..540P . дои : 10.1016/S0040-6090(99)00849-4 .
- ^ Вайслер, Г.Л., изд. (1990). Вакуумная физика и технология . Сан-Диего: Акад. Нажимать. п. 296. ИСБН 978-0-12-475914-5 .
- ^ Сурманн, П; Зеят, Х. (ноябрь 2005 г.). «Вольтамперометрический анализ с использованием самовозобновляемого безртутного электрода». Аналитическая и биоаналитическая химия . 383 (6): 1009–13. дои : 10.1007/s00216-005-0069-7 . ПМИД 16228199 . S2CID 22732411 .
- ^ Геологическая служба (США) (2010). Ежегодник полезных ископаемых, 2008, Т. 1, Металлы и полезные ископаемые . Государственная типография. стр. 35–2. ISBN 978-1-4113-3015-3 .
- ^ Пауэлл Л.В.; Джонсон Г.Х.; Бэйлз-ди-джей (1989). «Влияние добавки индия на выделение паров ртути из зубной амальгамы». Журнал стоматологических исследований . 68 (8): 1231–3. CiteSeerX 10.1.1.576.2654 . дои : 10.1177/00220345890680080301 . ПМИД 2632609 . S2CID 28342583 .
- ^ Скуллос, Майкл Дж. (31 декабря 2001 г.). «Прочие виды кадмиевых сплавов» . Ртуть, кадмий, свинец: справочник по устойчивой политике и регулированию в отношении тяжелых металлов . Спрингер. п. 222. ИСБН 978-1-4020-0224-3 .
- ^ Бергер, Гарольд; Национальное бюро стандартов, США; Комитет E-7 по неразрушающему контролю, Американское общество испытаний и материалов (1976). «Детекторы изображений других нейтронных энергий» . Практическое применение нейтронной радиографии и измерений: симпозиум . стр. 50–51.
{{cite book}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Купфершмидт, Кай (2 мая 2019 г.). «В поисках синего». Наука . 364 (6439). Американская ассоциация содействия развитию науки (AAAS): 424–429. Бибкод : 2019Sci...364..424K . дои : 10.1126/science.364.6439.424 . ISSN 0036-8075 . ПМИД 31048474 . S2CID 143434096 .
- ^ «Индий 57083» . Архивировано из оригинала 2 октября 2018 г. Проверено 02 октября 2018 г.
- ^ Гвинн, ВМ; Цюй, В.; Буске, RW; Прайс, Х.; Шайнс, CJ; Тейлор, Дж.Дж.; Ваалкес, член парламента; Морган, Д.Л. (2014). «Солюбилизация макрофагов и цитотоксичность индийсодержащих частиц, поскольку in vitro коррелирует с легочной токсичностью in vivo» . Токсикологические науки . 144 (1): 17–26. дои : 10.1093/toxsci/kfu273 . ПМЦ 4349143 . ПМИД 25527823 .
- ^ «ИНФ-111 ТЕХНИЧЕСКИЕ ДАННЫЕ» (PDF) . Nordion(Canada), Inc. Архивировано из оригинала (PDF) 3 декабря 2011 года . Проверено 23 сентября 2012 г.
- ^ Ван Ностранд, Д.; Абреу, Ш.; Каллаган, Джей-Джей; Аткинс, ФБ; Ступс, ХК; Савори, CG (май 1988 г.). «Поглощение меченных In-111 лейкоцитов при неинфицированных закрытых переломах у людей: проспективное исследование». Радиология . 167 (2): 495–498. дои : 10.1148/radiology.167.2.3357961 . ПМИД 3357961 .
- ^ Нордберг, Гуннар Ф.; Фаулер, Брюс А.; Нордберг, Моника (7 августа 2014 г.). Справочник по токсикологии металлов (4-е изд.). Академическая пресса. п. 845. ИСБН 978-0-12-397339-9 .
- ^ «CDC - Карманный справочник NIOSH по химическим опасностям - Индий» . www.cdc.gov . Архивировано из оригинала 8 декабря 2015 г. Проверено 6 ноября 2015 г.
Источники
[ редактировать ]- Гринвуд, Норман Н .; Эрншоу, Алан (1984). Химия элементов . Оксфорд: Пергамон Пресс . ISBN 978-0-08-022057-4 .
Внешние ссылки
[ редактировать ]- Индий. Архивировано 13 марта 2023 г. в Wayback Machine в Периодической таблице видео (Ноттингемский университет).
- Восстановители > Низковалентный индий. Архивировано 9 июля 2023 г. на Wayback Machine.
- Карманный справочник NIOSH по химическим опасностям. Архивировано 8 декабря 2015 г. в Wayback Machine (Центры по контролю и профилактике заболеваний).


