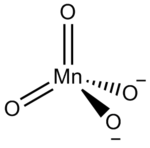
Манганат натрия
 | |
| Идентификаторы | |
|---|---|
3D model ( JSmol ) | |
ПабХим CID | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| Mn Na 2 O 4 | |
| Молярная масса | 164.914 g·mol −1 |
| Появление | темно-зеленый твердый |
| Родственные соединения | |
Родственные соединения | Манганат бария |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Манганат натрия неорганическое соединение формулы 2 Na Mn 4 O . – Это темно-зеленое твердое вещество является редко встречающимся аналогом родственной соли K 2 MnO 4 . Манганат натрия встречается редко, поскольку его нельзя легко получить окислением диоксида марганца и гидроксида натрия. Вместо этого эта реакция окисления имеет тенденцию останавливаться при образовании гипоманганата натрия Na 3 MnO 4 , и даже эта соль Mn(V) нестабильна в растворе. [1] Манганат натрия можно получить восстановлением перманганата натрия при основных условиях:
- 4 NaOH + 4NaMnO 4 → 4 Na 2 MnO 4 + 2 H 2 O + O 2
Поскольку NaMnO 4 трудно приготовить, перманганат натрия дороже перманганата калия .
Ссылки
[ редактировать ]- ^ Арно Х. Рейдис (2002). «Соединения марганца». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a16_123 . ISBN 3-527-30673-0 .