Бикарбонат натрия
 | |||
| |||
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК гидрокарбонат натрия | |||
| Другие имена Пищевая сода, бикарбонат (лабораторный сленг), бикарбонат соды, нахколит , гидрокарбонат натрия, натрон | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| 4153970 | |||
| ЧЭБИ | |||
| ЧЕМБЛ | |||
| ХимическийПаук | |||
| Лекарственный Банк | |||
| Информационная карта ECHA | 100.005.122 | ||
| Номер ЕС |
| ||
| номер Е | E500(ii) (регуляторы кислотности, ...) | ||
| КЕГГ | |||
| МеШ | Натрий+бикарбонат | ||
ПабХим CID | |||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| NaHCO 3 | |||
| Молярная масса | 84.0066 g mol −1 | ||
| Появление | Белые кристаллы | ||
| Запах | Без запаха | ||
| Плотность |
| ||
| Температура плавления | (Разлагается до карбоната натрия, начиная с 50 °C. [1] [6] ) | ||
| Растворимость | 0,02 мас.% ацетона, 2,13 мас.% метанола при 22 °C. [4] нерастворим в этаноле | ||
| войти P | −0.82 | ||
| Кислотность ( pKa ) | |||
Показатель преломления ( n D ) | nα = 1,377 nβ = 1,501 nγ = 1,583 | ||
| Структура | |||
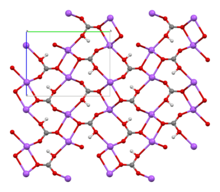
| Моноклиника | |||
| Термохимия | |||
Теплоемкость ( С ) | 87,6 Дж/моль К [7] | ||
Стандартный моляр энтропия ( S ⦵ 298 ) | 101,7 Дж/моль К [7] | ||
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | −950,8 кДж/моль [7] | ||
Свободная энергия Гиббса (Δ f G ⦵ ) | −851,0 кДж/моль [7] | ||
| Фармакология | |||
| B05CB04 ( ВОЗ ) B05XA02 ( ВОЗ ), QG04BQ01 ( ВОЗ ) | |||
| Внутривенно, перорально | |||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | Вызывает серьезное раздражение глаз | ||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | Огнестойкий | ||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза ) | 4220 мг/кг (крыса, перорально) [8] | ||
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов | ||
| Родственные соединения | |||
Другие анионы | Карбонат натрия | ||
Другие катионы | |||
Родственные соединения | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||

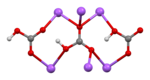
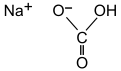
Бикарбонат натрия ( название IUPAC : гидрокарбонат натрия) . [9] ), широко известный как пищевая сода или бикарбонат соды , представляет собой химическое соединение с формулой NaHCO 3 . Это соль , состоящая из натрия катиона ( Na + ) и бикарбонат- анион ( HCO 3 − ). Бикарбонат натрия представляет собой белое твердое вещество, кристаллическое , но часто выглядит как мелкий порошок. Имеет слегка соленый, щелочной вкус, напоминающий стиральную соду ( карбонат натрия ). Природной минеральной формой является наколит , хотя он чаще встречается как компонент минерала трона . [10]
Поскольку соль давно известна и широко используется, она имеет много разных названий, таких как пищевая сода, хлебная сода, пищевая сода, пивоваренная сода и бикарбонат соды, и ее часто можно найти рядом с разрыхлителем в магазинах. Термин «пищевая сода» более распространен в Соединенных Штатах, а бикарбонат соды — в Австралии, Великобритании и Новой Зеландии. [11] сокращенные разговорные формы, такие как бикарбонат натрия , бикарбонат соды , бикарбонат и бикарбонат . Распространены [12]
Код пищевой добавки с номером E — E500. [13]
Приставка би- в слове «бикарбонат» происходит от устаревшей системы наименований, существовавшей еще до молекулярных знаний. Он основан на наблюдении, что карбонатов (CO 3 −2 ) на натрий в бикарбонате натрия (NaHCO 3 ), как и в карбонате натрия (Na 2 CO 3 ). [14] Современные химические формулы этих соединений теперь отражают их точные химические составы, которые были неизвестны, когда было придумано название бикарбонат калия (см. Также: бикарбонат ).
Использует [ править ]
Кулинария [ править ]
В кулинарии пищевая сода в основном используется в выпечке в качестве разрыхлителя . Когда он вступает в реакцию с кислотой или нагревается, выделяется углекислый газ, который вызывает расширение теста и формирует характерную текстуру и зернистость тортов, быстрого хлеба , содового хлеба и других выпеченных и жареных продуктов. При использовании кислоты кислотно-основную реакцию можно в общих чертах представить следующим образом: [15]
- NaHCO 3 + Н + → Вот и все + + СО 2 + Н 2 О
К кислым веществам, вызывающим эту реакцию, относятся гидрофосфаты , винный камень , лимонный сок, йогурт , пахта , какао и уксус . Пищевую соду можно использовать вместе с кислой закваской , в результате чего получается более легкий продукт с менее кислым вкусом. [16] Поскольку при комнатной температуре реакция протекает медленно, смеси (тесто для торта и т. п.) можно оставить стоять, не поднимаясь, до тех пор, пока они не разогреются в духовке. [ нужна ссылка ]
Нагревание также само по себе может привести к тому, что бикарбонат натрия будет действовать как разрыхлитель при выпечке из-за термического разложения , выделяя углекислый газ при температуре выше 80 ° C (180 ° F), а именно: [17]
- 2 NaHCO 3 → Na 2 CO 3 + H 2 O + CO 2
При таком использовании самостоятельно, без присутствия кислого компонента (будь то в тесте или при использовании разрыхлителя, содержащего кислоту), только половина доступного CO 2 выделяется CO 2 ( на каждые две молекулы CO 2 образуется одна молекула ). эквиваленты NaHCO 3 ). Кроме того, в отсутствие кислоты при термическом разложении бикарбоната натрия образуется также карбонат натрия , который является сильнощелочным и придает выпечке горьковатый мыльный вкус и желтый цвет.
Разрыхлитель [ править ]
Разрыхлитель , который также продается для приготовления пищи, содержит около 30% бикарбоната и различные кислотные ингредиенты, которые активируются добавлением воды, без необходимости добавления дополнительных кислот в среду для приготовления пищи. [18] [19] [20] Многие формы разрыхлителя содержат бикарбонат натрия в сочетании с фосфатом кальция , фосфатом алюминия-натрия или винным камнем . [21] Пищевая сода является щелочной; кислота, используемая в разрыхлителе, позволяет избежать металлического привкуса, поскольку в результате химического изменения во время выпечки образуется карбонат натрия. [22]
Пиротехника [ править ]
Бикарбонат натрия — один из основных компонентов обычного фейерверка «черная змея» . Эффект вызван термическим разложением, в результате которого выделяется углекислый газ с образованием длинного змеевидного пепла в качестве продукта сгорания другого основного компонента, сахарозы . [23] Бикарбонат натрия также замедляет реакции горения за счет выделения углекислого газа и воды, которые при нагревании являются антипиренами.
Мягкое дезинфицирующее средство [ править ]
Обладает слабыми дезинфицирующими свойствами. [24] [25] и это может быть эффективным фунгицидом против некоторых организмов. [26] Поскольку пищевая сода поглощает затхлый запах, для продавцов подержанных книг она стала надежным методом уменьшения неприятного запаха книг. [27]
Огнетушитель [ править ]
Бикарбонат натрия можно использовать для тушения небольших пожаров, связанных с жиром или электричеством, бросая его в огонь, поскольку при нагревании бикарбоната натрия выделяется углекислый газ. [28] Однако его не следует применять при пожаре во фритюрницах ; внезапный выброс газа может привести к разбрызгиванию смазки. [28] Бикарбонат натрия используется в сухих химических огнетушителях BC в качестве альтернативы более агрессивному моноаммонийфосфату в огнетушителях ABC. Щелочная природа бикарбоната натрия делает его единственным сухим химическим агентом, помимо Purple-K , который использовался в крупномасштабных системах пожаротушения, установленных на коммерческих кухнях. [29]
Бикарбонат натрия обладает несколькими механизмами пожаротушения, действующими одновременно. При нагревании он разлагается на воду и углекислый газ — эндотермическая реакция , лишающая огонь тепла. Кроме того, он образует промежуточные соединения, которые могут удалять свободные радикалы , ответственные за распространение огня . [30] В частности, при пожаре жира он также оказывает мягкий эффект омыления , образуя мыльную пену, которая может помочь потушить огонь. [29]
Нейтрализация кислот [ править ]
Бикарбонат натрия самопроизвольно реагирует с кислотами, выделяя CO 2 в качестве продукта реакции газообразный . Его обычно используют для нейтрализации нежелательных кислотных растворов или разливов кислоты в химических лабораториях. [31] Нецелесообразно использовать бикарбонат натрия для нейтрализации основания. [32] хотя он амфотерен и реагирует как с кислотами, так и с основаниями. [33]
Спортивная добавка [ править ]
Бикарбонат натрия принимают в качестве спортивной добавки для повышения мышечной выносливости. [34] Исследования, проведенные в основном среди мужчин, показали, что бикарбонат натрия наиболее эффективен для повышения производительности при кратковременных высокоинтенсивных занятиях. [35]
Сельское хозяйство [ править ]
Бикарбонат натрия может предотвратить рост грибков при нанесении на листья, хотя и не убивает грибок. Избыточное количество бикарбоната натрия может вызвать изменение окраски плодов (двухпроцентный раствор) и хлороз (однопроцентный раствор). [36]
Медицинское использование и здоровье
Бикарбонат натрия, смешанный с водой, можно использовать в качестве антацида при лечении кислотного расстройства желудка и изжоги . [37] [38] Его реакция с желудочной кислотой приводит к образованию соли , воды и углекислого газа :
- NaHCO 3 + HCl → NaCl + H 2 O + CO 2 (г)
Смесь бикарбоната натрия и полиэтиленгликоля, такая как PegLyte, [39] растворенный в воде и принимаемый перорально, является эффективным препаратом для промывания желудочно-кишечного тракта и слабительным средством перед желудочно-кишечными операциями, гастроскопией и т. д. [ нужна ссылка ]
Внутривенное введение бикарбоната натрия в водном растворе иногда применяют в случаях ацидоза или при недостаточном количестве ионов натрия или бикарбоната в крови. [40] В случаях респираторного ацидоза введенный ион бикарбоната смещает углекислотный/бикарбонатный буфер плазмы влево и, таким образом, повышает pH. По этой причине бикарбонат натрия используется при сердечно-легочной реанимации под медицинским наблюдением . Инфузия бикарбоната показана только при рН крови (< 7,1–7,0). значительно низком [41]
HCOHCO3 − используется для лечения гиперкалиемии , так как он выводит K + обратно в клетки в периоды ацидоза. [42] Поскольку бикарбонат натрия может вызвать алкалоз , его иногда используют для лечения передозировки аспирина. Для правильного всасывания аспирину необходима кислая среда, а основная среда снижает всасывание аспирина в случае передозировки. [43] Бикарбонат натрия также использовался при лечении передозировки трициклическими антидепрессантами . [44] Его также можно применять местно в виде пасты (три части пищевой соды на одну часть воды), чтобы облегчить некоторые виды укусов насекомых (а также сопутствующие отеки). [45]
Некоторые практикующие альтернативные методы лечения, такие как Туллио Симончини , пропагандируют пищевую соду как лекарство от рака, против чего Американское онкологическое общество предостерегает как из-за ее недоказанной эффективности, так и из-за потенциальной опасности при использовании. [46] Эдзард Эрнст назвал продвижение бикарбоната натрия как лекарства от рака «одним из наиболее отвратительных альтернативных мошенничеств с раком, которые я видел за долгое время». [47]
Бикарбонат натрия можно добавлять к местным анестетикам , чтобы ускорить наступление их действия и сделать их инъекции менее болезненными. [48] Он также является компонентом раствора Моффетта , используемого в назальной хирургии. [49]
Было высказано предположение, что кислая диета ослабляет кости. [50] Один систематический метаанализ исследования не выявил такого эффекта. [51] Другой также обнаружил, что нет никаких доказательств того, что щелочная диета улучшает здоровье костей, но предполагает, что щелочная диета «может иметь некоторую ценность» по другим причинам. [52]
Антацидные растворы (например, пищевая сода) готовились и использовались протестующими для смягчения последствий воздействия слезоточивого газа во время протестов. [ не удалось пройти проверку ] [53]
Подобно использованию в выпечке, бикарбонат натрия используется вместе с мягкой кислотой, такой как винная кислота , в качестве вспомогательного вещества в шипучих таблетках: когда такую таблетку опускают в стакан с водой, карбонат покидает реакционную среду в виде углекислого газа ( ОХС 3 − + Ч + → H 2 O + CO 2 ↑ или, точнее, HCO 3 − + Н3О + → 2 H 2 O + CO 2 ↑). Это приводит к распаду таблетки, в результате чего лекарство остается во взвешенном состоянии и/или растворяется в воде вместе с образовавшейся солью (в данном примере тартратом натрия ). [54]
Личная гигиена [ править ]
Бикарбонат натрия также используется в качестве ингредиента в некоторых средствах для полоскания рта. Обладает противокариесными и абразивными свойствами. [55] Он действует как механическое очищающее средство для зубов и десен, нейтрализует выработку кислоты во рту, а также действует как антисептик , помогая предотвратить инфекции. [56] [57] Бикарбонат натрия в сочетании с другими ингредиентами можно использовать для приготовления сухого или влажного дезодоранта . [58] [59] Бикарбонат натрия можно использовать в качестве буферного агента в сочетании с поваренной солью при приготовлении раствора для назального орошения . [60]
Его используют в гигиене глаз для лечения блефарита . Это делается путем добавления чайной ложки бикарбоната натрия в прохладную, только что кипяченную воду, после чего следует осторожно протереть основание ресниц ватным тампоном, смоченным в растворе. [61] [62]
Ветеринария [ править ]
Бикарбонат натрия используется в качестве добавки к корму для крупного рогатого скота, в частности в качестве буферного агента для рубца . [63]
Чистящее средство [ править ]
Бикарбонат натрия используется в процессе удаления краски и коррозии, который называется натриеструйной обработкой . В качестве средства для струйной обработки бикарбонат натрия используется для удаления поверхностных загрязнений с более мягких и менее упругих оснований, таких как алюминий, медь или древесина, которые могут быть повреждены абразивными материалами из кварцевого песка. [64]
Производитель рекомендует в качестве мягкого чистящего порошка пасту из пищевой соды с минимальным содержанием воды. [28] Такая паста может быть полезна для удаления поверхностной ржавчины, поскольку в концентрированном щелочном растворе ржавчина образует водорастворимое соединение. [65] Следует использовать холодную воду, поскольку растворы горячей воды могут вызвать коррозию стали. [66] Бикарбонат натрия разрушает тонкий защитный оксидный слой, образующийся на алюминии, что делает его непригодным для очистки этого металла. [67] Раствор в теплой воде удалит потускнение с серебра при контакте серебра с куском алюминиевой фольги . [67] [68] Пищевую соду обычно добавляют в стиральные машины вместо смягчителя воды и для удаления запахов с одежды. Разбавленный теплой водой, он почти так же эффективен для удаления сильных пятен от чая и кофе с чашек, как и гидроксид натрия .
Во время Манхэттенского проекта по разработке ядерной бомбы в начале 1940-х годов химическая токсичность урана была проблемой. Было обнаружено, что оксиды урана очень хорошо прилипают к хлопчатобумажной ткани и не смываются мылом или стиральным порошком. Однако уран вымывается 2% раствором бикарбоната натрия. Одежда может загрязняться токсичной пылью обедненного урана (ОУ), которая очень плотна, поэтому ее используют для противовесов в гражданском контексте и в бронебойных снарядах. ОУ не удаляется обычной стиркой; промывка примерно 6 унциями (170 г) пищевой соды в 2 галлонах (7,5 л) воды поможет смыть его. [69]
Контроль запаха [ править ]
Часто утверждают, что пищевая сода эффективно удаляет запахи. [70] [ нужен лучший источник ] и рекомендовал хранить в холодильнике открытую коробку, чтобы впитать запах. [71] Эту идею продвигал ведущий американский бренд пищевой соды Arm & Hammer в рекламной кампании, начавшейся в 1972 году. [72] Хотя эта кампания считается классикой маркетинга, в результате которой за год в более чем половине американских холодильников оказалась коробка с пищевой содой. [73] [74] существует мало доказательств того, что он эффективен в этом применении. [75] [76]
Химия [ править ]

Бикарбонат натрия – амфотерное соединение. [33] Водные растворы слабощелочные из -за образования угольной кислоты и гидроксид- иона: [33]
- ОЗС −
3 + Н 2 О → Ч
22CO
3 + ОН −
Бикарбонат натрия иногда можно использовать в качестве мягкого нейтрализующего агента и более безопасной альтернативы сильным основаниям, таким как гидроксид натрия . [77] Реакция бикарбоната натрия и кислоты дает соль и угольную кислоту, которая легко разлагается на углекислый газ и воду: [77]
- NaHCO 3 + HCl → NaCl + H 2 O+CO 2
- H 2 CO 3 → H 2 O + CO 2 (г)
Бикарбонат натрия реагирует с уксусной кислотой (содержащейся в уксусе), образуя ацетат натрия , воду и углекислый газ :
- NaHCO 3 + CH 3 COOH → CH 3 COONa + H 2 O + CO 2 (г)
Бикарбонат натрия реагирует с основаниями , такими как гидроксид натрия, с образованием карбонатов:
- NaHCO 3 + NaOH → Na 2 CO 3 + H 2 O
Термическое разложение [ править ]
При температуре 80–100 ° C (176–212 ° F) бикарбонат натрия постепенно разлагается на карбонат натрия , воду и углекислый газ. Преобразование происходит быстрее при 200 °C (392 °F): [78]
- 2 NaHCO 3 → Na 2 CO 3 + H 2 O + CO 2
Большинство бикарбонатов подвергаются этой реакции дегидратации . Дальнейшее нагревание превращает карбонат в оксид (выше 850 °C/1560 °F): [78]
- Na 2 CO 3 → Na 2 O + CO 2
Образование углекислого газа и воды частично объясняет огнетушащие свойства NaHCO 3 , [29] хотя другие факторы, такие как поглощение тепла и удаление радикалов , более важны. [30]
Естественное явление [ править ]
В природе бикарбонат натрия встречается почти исключительно в виде нахколита или троны . Трона встречается чаще, поскольку нахколит лучше растворяется в воде, а химическое равновесие между двумя минералами благоприятствует троне. [10] Значительные месторождения нахколита находятся в США, Ботсване и Кении, Уганде, Турции и Мексике. [79] Крупнейшие месторождения троны находятся в бассейне реки Грин в Вайоминге. [80]
Наколит иногда встречается в составе горючих сланцев . [81]
Стабильность и срок годности [ править ]
При хранении в прохладном (комнатная температура) и сухом месте (для защиты от влажного воздуха рекомендуется использовать герметичный контейнер) бикарбонат натрия можно хранить без значительного разложения в течение как минимум двух или трех лет. [82] [83] [84] [85]
История [ править ]
Слово натрон использовалось во многих языках в наше время (в формах anatron , natrum и natron ) и возникло (как и испанский, французский и английский natron , а также « натрий ») через арабский naṭrūn (или anatrūn ; ср. нижнегипетский «Натронталь» Вади-эль-Натрун смесь карбоната натрия и гидрокарбоната натрия. , где для обезвоживания мумий использовалась [86] ) от греческого нитрон (νίτρον) (Геродот; аттический литрон (λίτρον) ), который восходит к древнеегипетскому нтр . Греческое слово нитрон (сода, селитра) также использовалось в латинском языке (sal) nitrum и в немецком языке Salniter (источник азота , нитрата и т. д.). [87] [88] Слово saleratus , от латинского sal æratus (что означает «газированная соль»), широко использовалось в 19 веке как для бикарбоната натрия, так и для бикарбоната калия . [89]
В 1791 году французский химик Николя Леблан получил карбонат натрия (также известный как кальцинированная сода). Аптекарю Валентину Розе Младшему приписывают открытие бикарбоната натрия в 1801 году в Берлине. В 1846 году два американских пекаря, Джон Дуайт и Остин Чёрч , основали первую в США фабрику по производству пищевой соды из карбоната натрия и углекислого газа . [90]
Салератус , бикарбонат калия или натрия, упоминается в романе Отважные капитаны» « Редьярда Киплинга как широко использовавшийся в 1800-х годах в коммерческом рыболовстве для предотвращения порчи только что пойманной рыбы. [91]
В 1919 году сенатор США Ли Оверман заявил, что бикарбонат соды может вылечить испанский грипп . В разгар дебатов 26 января 1919 года он прервал дискуссию, чтобы объявить об открытии лекарства. «Я хочу сказать для тех, кто проводит это расследование, — сообщил он, — что судья высшего суда горной страны Северной Каролины сообщил мне, что они нашли лекарство от этой болезни». Предполагаемое лечение подразумевало критику современной науки и признание простой мудрости простых людей. «Они говорят, что обычная пищевая сода излечит болезнь, — продолжал он, — что они вылечили ее с ее помощью, что у них там вообще нет смертей; они используют обычную пищевую соду, которая излечивает болезнь». [92]
Производство [ править ]
Бикарбонат натрия в промышленности получают из карбоната натрия : [93]
- Na 2 CO 3 + CO 2 + H 2 O → 2 NaHCO 3
Его производят в масштабах около 100 000 тонн в год (по состоянию на 2001 год). [ сомнительно – обсудить ] [94] с мировой производственной мощностью 2,4 миллиона тонн в год (по состоянию на 2002 год). [95] Аналогичным методом производят и промышленные количества пищевой соды: кальцинированную соду, добываемую в виде руды трона , растворяют в воде и обрабатывают углекислым газом. Из этого раствора бикарбонат натрия выпадает в осадок в виде твердого вещества. [ нужна ссылка ]
Что касается процесса Сольве , бикарбонат натрия является промежуточным продуктом реакции хлорида натрия , аммиака и диоксида углерода . Однако продукт имеет низкую чистоту (75%). [ нужна ссылка ]
Хотя практического значения не имеет, NaHCO 3 может быть получен реакцией углекислого газа с водным раствором гидроксида натрия: [ нужна ссылка ]
- CO 2 + NaOH → NaHCO 3
Горное дело [ править ]
Природные месторождения нахколита (NaHCO 3 ) обнаружены в эоценового возраста (55,8–33,9 млн лет назад) формации Грин-Ривер , бассейн Пиканс в Колорадо . Нахколит откладывался в виде пластов в периоды сильного испарения в бассейне. В коммерческих целях его добывают с использованием обычных методов подземной добычи, таких как буровая, барабанная и длинные забои, что очень похоже на добычу угля. [ нужна ссылка ]
Его также производят путем добычи раствором, прокачивания нагретой воды через пласты нахколита и кристаллизации растворенного нахколита в процессе охлаждающей кристаллизации.
Поскольку нахколит иногда встречается в сланцах, его можно производить как побочный продукт добычи сланцевого масла , где его извлекают путем добычи раствором. [81]
В популярной культуре [ править ]
Бикарбонат натрия, как «бикарбонат соды», был частым источником изюминок Граучо Маркса в фильмах братьев Маркс . В «Утином супе » Маркс играет лидера нации, находящейся в состоянии войны. В одной из сцен он получает сообщение с поля боя о том, что его генерал сообщает о газовой атаке, и Граучо говорит своему помощнику: «Скажите ему, чтобы он принял чайную ложку бикарбоната соды и полстакана воды». [96] В «Ночи в опере» персонаж Граучо обращается к публике на премьере оперы, говоря о ведущем теноре: «Синьор Ласспарри происходит из очень известной семьи. Его мать была известной бас-певицей. Его отец был первым мужчиной. начинять спагетти бикарбонатом соды, вызывая таким образом и одновременно излечивая расстройство желудка». [97]
В классическом фильме Джозефа Л. Манкевича « Все о Еве » персонаж Макса Фабиана ( Грегори Ратофф ) имеет расширенную сцену с Марго Ченнинг ( Бетт Дэвис ), в которой, страдая от изжоги, он просит, а затем пьет бикарбонат газировки, вызывая заметную отрыжку. . Ченнинг обещает всегда иметь при себе коробку бикарбоната с именем Макса.
См. также [ править ]
Ссылки [ править ]
- ^ Jump up to: Перейти обратно: а б Хейнс, с. 4,90
- ^ Jump up to: Перейти обратно: а б с Хейнс, с. 5.194
- ^ Jump up to: Перейти обратно: а б с «Бикарбонат натрия» (PDF) . Программа ООН по окружающей среде . Архивировано из оригинала (PDF) 16 мая 2011 года.
- ^ Эллингбо Дж.Л., Раннелс Дж.Х. (1966). «Растворимость карбоната натрия и бикарбоната натрия в смесях ацетон-вода и метанол-вода». Дж. Хим. англ. Данные . 11 (3): 323–324. дои : 10.1021/je60030a009 .
- ^ Jump up to: Перейти обратно: а б Хейнс, с. 7.23
- ^ Паскуали I, Беттини Р., Джордано Ф (2007). «Термическое поведение диклофенака, диклофенака натрия и композиций бикарбоната натрия». Журнал термического анализа и калориметрии . 90 (3): 903–907. дои : 10.1007/s10973-006-8182-1 . S2CID 95695262 .
- ^ Jump up to: Перейти обратно: а б с д Хейнс, с. 5.19
- ^ Гриффит Дж. Ф. (1964). «Межлабораторные вариации в определении острой пероральной ЛД50». Токсикология и прикладная фармакология . 6 (6): 726–730. дои : 10.1016/0041-008X(64)90124-3 . ПМИД 14235840 .
- ^ Номенклатура неорганической химии Рекомендации ИЮПАК 2005 г. (PDF) , ИЮПАК, стр. 137, заархивировано (PDF) из оригинала 18 мая 2017 г.
- ^ Jump up to: Перейти обратно: а б Гертнер Р.С., Виткамп Г.Дж. (август 2007 г.). «Реактивная перекристаллизация троны (полуторного карбоната натрия) в смешанном растворителе в соду (безводный карбонат натрия)» . Гидрометаллургия . 88 (1–4): 75–91. doi : 10.1016/j.гидромет.2007.03.006 .
- ^ «Разрыхлитель, пищевая сода или бикарбонат соды?» . Ридерс Дайджест Австралия . Проверено 2 июня 2024 г.
- ^ ПабХим. «Бикарбонат натрия» . pubchem.ncbi.nlm.nih.gov . Проверено 25 января 2021 г.
- ^ «Разрешенные добавки и номера E» . Агентство по пищевым стандартам . Проверено 7 декабря 2020 г.
- ^ Волластон WH (январь 1814 г.). «I. Синоптическая шкала химических эквивалентов» . Философские труды Лондонского королевского общества . 104 : 1–22. дои : 10.1098/rstl.1814.0001 . S2CID 96774986 .
- ^ Бент А.Дж., изд. (1997). Технология приготовления тортов (6-е изд.). Спрингер. п. 102. ИСБН 9780751403497 . Проверено 12 августа 2009 г.
- ^ Касцио Дж. «Закваска» (PDF) . Университета Аляски в Фэрбенксе Служба кооперативного распространения знаний . ФНХ-00061. Архивировано из оригинала (PDF) 27 марта 2016 года . Проверено 2 мая 2017 г.
- ^ «Множество практических применений пищевой соды на кухне» . О.com Еда . Архивировано из оригинала 2 февраля 2017 года . Проверено 22 января 2017 г.
- ^ Черногорский Дж. Х., Хукер Р. «Химия выпечки» (PDF) . Новозеландский институт химии. Архивировано из оригинала (PDF) 27 ноября 2016 года . Проверено 22 января 2017 г.
- ^ «Пищевая сода и разрыхлитель» . FineCooking.com . Архивировано из оригинала 2 февраля 2017 года . Проверено 22 января 2017 г.
- ^ «Часто задаваемые вопросы о пищевой соде» . Мультибрендовый бренд Arm & Hammer . Компания Черч и Дуайт. В чем разница пищевой соды и разрыхлителя? Архивировано из оригинала 27 июня 2017 года . Проверено 20 июля 2017 г.
- ^ «Глоссарий ингредиентов» . Кулинарный сайт.com. Архивировано из оригинала 15 сентября 2008 года.
- ^ «Бикарбонат натрия» . БРП Адхикари . 11 июля 2016 года . Проверено 25 января 2021 г.
- ^ «Сахарная змея» . МЭЛ Наука . МЭЛ Наука 2015–2019. Архивировано из оригинала 6 октября 2019 года . Проверено 28 октября 2019 г.
- ^ Малик Ю.С., Гоял С.М. (май 2006 г.). «Вирулицидная эффективность бикарбоната натрия на поверхности, контактирующей с пищевыми продуктами, против кошачьего калицивируса, суррогата норовируса». Международный журнал пищевой микробиологии . 109 (1–2): 160–3. doi : 10.1016/j.ijfoodmicro.2005.08.033 . ПМИД 16540196 .
- ^ Рутала В.А., Барби С.Л., Агиар Северная Каролина, Собси Мэриленд, Вебер DJ (январь 2000 г.). «Противомикробная активность домашних дезинфицирующих средств и натуральных продуктов в отношении потенциальных патогенов человека». Инфекционный контроль и госпитальная эпидемиология . 21 (1): 33–8. дои : 10.1086/501694 . ПМИД 10656352 . S2CID 34461187 .
- ^ Замани М., Шарифи Техрани А., Али Абади А.А. (2007). «Оценка противогрибковой активности карбонатных и бикарбонатных солей отдельно или в сочетании с агентами биоконтроля при борьбе с зеленой плесенью цитрусовых». Коммуникации в сельскохозяйственных и прикладных биологических науках . 72 (4): 773–7. ПМИД 18396809 .
- ^ Альтман Г. (22 мая 2006 г.). «Ремонт книг для книгомыслящих: как удалить запахи из книг» . Книжный мыслитель (69).
- ^ Jump up to: Перейти обратно: а б с «Пищевая сода Arm & Hammer – Основы – Магия пищевой соды Arm & Hammer» . www.armandhammer.com . Архивировано из оригинала 31 августа 2009 года . Проверено 30 июля 2009 г.
- ^ Jump up to: Перейти обратно: а б с Фёлкерт Дж.К. (2015). «Пожар и пожаротушение. Краткое руководство по химии огня и теории пожаротушения для специалистов по обслуживанию пожарного оборудования» (PDF) . п. 14–15. Архивировано из оригинала (PDF) 31 мая 2024 года . Проверено 22 сентября 2023 г.
- ^ Jump up to: Перейти обратно: а б Лю Ю, Чжан Ю, Мэн Х, Ян К, Ван З, Лю Дж, Ван З, Ян П, Дай В, Ли Ф (апрель 2022 г.). «Исследование распространения пламени и взрывного избыточного давления при тушении взрыва сланцевой пыли с помощью NaHCO3» . Топливо . 314 : 122778. doi : 10.1016/j.fuel.2021.122778 .
- ^ «Подготовка к чрезвычайным ситуациям от неконтролируемых опасностей» . Американское химическое общество.
- ^ Хурум Д. «Лабораторная безопасность» (PDF) . Гражданское строительство . Северо-Западный университет.
- ^ Jump up to: Перейти обратно: а б с Дэвидсон Д. (ноябрь 1955 г.). «Амфотерные молекулы, ионы и соли» . Журнал химического образования . 32 (11): 550. doi : 10.1021/ed032p550 . ISSN 0021-9584 .
- ^ Гргич Дж., Родригес Р.Ф., Гарофолини А., Сондерс Б., Бишоп Д.Д., Шенфельд Б.Дж., Педисич З. (июль 2020 г.). «Влияние добавок бикарбоната натрия на мышечную силу и выносливость: систематический обзор и метаанализ» . Спортивная медицина . 50 (7): 1361–1375. дои : 10.1007/s40279-020-01275-y . ПМИД 32096113 . S2CID 211254185 .
- ^ Гргич Дж, Гргич И, Педишич З (2021). «Влияние добавок бикарбоната натрия на физическую работоспособность: общий обзор» . Журнал Международного общества спортивного питания . 18 (1): 71. дои : 10.1186/s12970-021-00469-7 . ПМЦ 8600864 . ПМИД 34794476 .
- ^ «Мифы о садоводстве» . Факультет растениеводства и почвоведения Университета Вермонта . Архивировано из оригинала 7 августа 2019 года . Проверено 18 октября 2021 г.
- ^ «Бикарбонат натрия» . Джексон Сигельбаум Гастроэнтерология. 1998. Архивировано из оригинала 5 октября 2016 года . Проверено 4 октября 2016 г.
- ^ «Побочные эффекты бикарбоната натрия (пероральный, внутривенный, подкожный) - Клиника Мэйо» . www.mayoclinic.org . Проверено 5 мая 2023 г.
- ^ «ПегЛайт» . Пендо Пхама .
- ^ «Внутривенная инфузия бикарбоната натрия» (PDF) . Информация о потребительских лекарствах . Канал «Лучшее здоровье». 13 июля 2004 г. Архивировано из оригинала (PDF) 22 августа 2008 г.
- ^ «Респираторный ацидоз: лечение и медикаментозное лечение» . медицина. 26 марта 2020 г.
- ^ Дарт РК (2004). Медицинская токсикология . Липпинкотт Уильямс и Уилкинс. стр. 910–. ISBN 978-0-7817-2845-4 .
- ^ Тканевые подгузники . Дональд К. Купер, доктор философии. стр. 46–.
- ^ [ нужно обновить ] Кнудсен К., Абрахамссон Дж. (апрель 1997 г.). «Адреналин и бикарбонат натрия независимо и дополнительно увеличивают выживаемость при экспериментальном отравлении амитриптилином». Медицина критических состояний . 25 (4): 669–74. дои : 10.1097/00003246-199704000-00019 . ПМИД 9142034 .
- ^ «Укусы насекомых: Первая помощь» . Клиника Майо. 15 января 2008 г.
- ^ «Бикарбонат натрия» . Американское онкологическое общество . 28 ноября 2008 г. Архивировано из оригинала 19 февраля 2013 г. Проверено 19 февраля 2013 г.
{{cite web}}: CS1 maint: неподходящий URL ( ссылка ) - ^ Эрнст Э (3 февраля 2017 г.). «Это, должно быть, самая отвратительная афера с раком, которую я когда-либо видел» .
- ^ Эджкомб Х., Хокинг Дж. (6 октября 2006 г.). «Фармакология местных анестетиков» . Анестезия Великобритания . Архивировано из оригинала 22 декабря 2015 года.
- ^ Бенджамин Э., Вонг Д., Чоа Д. (2004). « Решение Моффетта: обзор доказательств и научной основы местной подготовки носа» . Клиническая отоларингология и смежные науки . 29 (6): 582–587. дои : 10.1111/j.1365-2273.2004.00894.x . ПМИД 15533141 .
- ^ Фокс Д. (15 декабря 2001 г.). «Твердый сыр» . Новый учёный . Проверено 20 июля 2017 г.
- ^ Фентон Т.Р., Tough SC, Лион А.В., Элиашив М., Хэнли Д.А. (2011). «Причинная оценка пищевой кислотной нагрузки и заболеваний костей: систематический обзор и метаанализ с применением эпидемиологических критериев причинности Хилла» . Журнал питания . 10:41 . дои : 10.1186/1475-2891-10-41 . ПМК 3114717 . ПМИД 21529374 .
- ^ Швальфенберг ГК (2012). «Щелочная диета: есть ли доказательства того, что диета с щелочным pH полезна для здоровья?» . Журнал окружающей среды и общественного здравоохранения . 2012 : 1–7. дои : 10.1155/2012/727630 . ПМК 3195546 . ПМИД 22013455 .
- ^ «Медицинская информация из Праги 2000» . Архивировано из оригинала 18 октября 2014 года.
- ^ Ширсанд С.Б., Суреш С., Джодхана Л.С., Свами П.В. (2010). «Разработка рецептуры и оптимизация быстро распадающихся таблеток лоразепама шипучим методом» . Индийский журнал фармацевтических наук . 72 (4): 431–436. дои : 10.4103/0250-474X.73911 . ISSN 0250-474X . ПМК 3013557 . ПМИД 21218052 .
- ^ Сторехаген С., Осе Н., Мидха С. «Ингредиенты средств для ухода за зубами и ополаскивателей для рта и их использование» (PDF) . Кафедра клинической одонтологии . Университет Осло.
- ^ США 4132770A , Барт Дж., «Продукт для перорального применения», выпущен в 1979 г.
- ^ Икбал К., Асмат М., Джавед С., Муштак А., Мохсин Ф., Ханиф С. и др. (июль 2011 г.). «Роль различных ингредиентов зубных паст и жидкостей для полоскания рта в здоровье полости рта» (PDF) . Журнал Пакистанской стоматологической ассоциации . 20 (3): 163–70.
- ^ Лэмб Дж. Х. (1946). «Бикарбонат натрия: отличный дезодорант» . Журнал исследовательской дерматологии . 7 (3): 131–133. дои : 10.1038/jid.1946.13 .
- ^ «Бикарбовая сода: натуральный дезодорант для тела» . Sustainableecho.com. 10 марта 2009 г.
- ^ Метсон РБ (2005). Руководство Гарвардской медицинской школы по исцелению пазух . МакГроу Хилл. п. 68. ИСБН 9780071444699 .
- ^ «Блефарит: Информационный буклет для пациентов» (PDF) . Ouh.nhs.uk. Проверено 28 февраля 2022 г.
- ^ «Блефарит. Лечение и причины. Воспаление век | Пациент» . Пациент . Архивировано из оригинала 5 декабря 2015 года . Проверено 31 мая 2016 г.
- ^ Патон Л.Дж., Бошемин К.А., Вейра Д.М., фон Кейзерлингк М.А. (2006). «Использование бикарбоната натрия, предлагаемого по выбору или добавленного в рацион, для снижения риска рубцового ацидоза у крупного рогатого скота» . Канадский журнал зоотехники . 86 (3): 429–437. дои : 10.4141/A06-014 .
- ^ «Удалите грязь с помощью пищевой соды» . Популярная механика. 5 августа 2013 года . Проверено 2 августа 2020 г.
- ^ Housecroft CE, Sharpe AG (2008). «Глава 22: d -блок химия металлов: элементы первого ряда». Неорганическая химия, 3-е издание . Пирсон. п. 716. ИСБН 978-0-13-175553-6 .
- ^ «Научная лаборатория.com» . MSDS- Карбонат натрия . sciencelab.com. Архивировано из оригинала 5 сентября 2012 года.
- ^ Jump up to: Перейти обратно: а б «Техника отделочной обработки металлов» . Художественный музей Филадельфии.
- ^ «Придайте этому блеск» . scifun.chem.wisc.edu. Архивировано из оригинала 31 июля 2012 года . Проверено 6 марта 2011 г.
- ^ Оркатт Дж.А. «Обедненный уран и здоровье: факты и полезные предложения» . Фармакология и токсикология соединений урана . МакГроу-Хилл. Архивировано из оригинала 17 января 2013 года . Проверено 21 марта 2012 г.
- ^ Раймонд Дж. (10 июня 2016 г.). «Свечи, продукты и хитрости для устранения кухонного запаха» . cravedujour.com . Архивировано из оригинала 7 августа 2020 года . Проверено 29 июня 2016 г.
- ^ Вики Лански, Марта Кэмпбелл, Пищевая сода: более 500 потрясающих, забавных и скромных способов применения, о которых вы, вероятно, никогда не думали , 2009 г., ISBN 1931863733 , с. 28
- ^ «Решение, которому доверяют более 170 лет. Чисто и просто», Arm & Hammer «О нас». страница
- ^ Кейт Сойер, Групповой гений: творческая сила сотрудничества , 2017, ISBN 0465093582 , «сохраняйте свежесть еды»
- ^ Клейтон М. Кристенсен, Скотт Кук, Тэдди Холл, Злоупотребление служебным положением в маркетинге: причина и лечение , Harvard Business Review , декабрь 2005 г., [1]
- ^ «Миф № 100: Открытая коробка с пищевой содой в холодильнике поглощает запахи», Брюс Вайнштейн, Марк Скарбро, Омары кричат, когда их варишь; И 100 других мифов о еде и кулинарии , 2011, ISBN 1439195382 , с. 312
- ^ «Пищевая сода как поглотитель запахов | Cook's Illustrated» . Cooksillustrated.com . Проверено 28 февраля 2022 г.
- ^ Jump up to: Перейти обратно: а б Папуга А., Поланчик А (6 декабря 2023 г.). «Анализ последних рекомендаций по нейтрализации отдельных кислот, включая рекомендации для аварийно-спасательных служб» . Зешиты Наукове СГСП . 1 (88): 75–95. дои : 10.5604/01.3001.0054.1220 . ISSN 0239-5223 .
- ^ Jump up to: Перейти обратно: а б «Разложение карбонатов» . Общая химия онлайн. Архивировано из оригинала 2 октября 1999 года . Проверено 16 марта 2010 г.
- ^ «Нахколите» . Британская энциклопедия . 2012 . Проверено 2 июня 2024 г.
- ^ Болен В.П. (январь 2024 г.). Кальцинированная сода (PDF) . Геологическая служба США . Архивировано из оригинала (PDF) 4 марта 2024 года.
- ^ Jump up to: Перейти обратно: а б Джонсон Р.К., Мерсье Т.Дж., Браунфилд М.Э., член парламента Пантеа, Селф (2020). Оценка пластовых ресурсов сланца в формации Грин-Ривер, бассейн Пайсанс, Колорадо . Геологическая служба США .
- ^ ПабХим. «Бикарбонат натрия» . pubchem.ncbi.nlm.nih.gov . Проверено 16 мая 2021 г.
- ^ «Нумерация партий бикарбоната натрия (S300) и срок годности – Solvay Chemicals, Inc» (PDF) . 31 января 2019 г.
- ^ «Re: Срок годности — бикарбонат натрия (все сорта) — Tronox Alkali Corporation» (PDF) . 1 апреля 2015 г.
- ^ «Пищевая сода испортилась? Как узнать, что она все еще хороша» . Ель ест . Проверено 16 мая 2021 г.
- ^ Рената Гернер: Инструменты и вещества, используемые при мумификации. В: Рената Гернер, Розмари Дренхан (ред.): Mumie und Computer. Междисциплинарный исследовательский проект в Ганновере. Специальная выставка Музея Кестнера в Ганновере с 26 сентября 1991 г. по 19 января 1992 г. Музей Кестнера, Ганновер 1991 г., ISBN 3-924029-17-2 , с. 28 ф.
- ^ Франц Дорнсайф: «Греческие слова на немецком языке». Вальтер де Грюйтер и компания, Берлин, 1950 г., с. 44.
- ^ Фридрих Клюге , Альфред Гетце (филолог): Этимологический словарь немецкого языка . 20-е издание, изд. Вальтер Мицка, Де Грюйтер, Берлин/Нью-Йорк, 1967; Перепечатка («21-е неизмененное издание») там же, 1975 г., ISBN 3-11-005709-3 , с. 504.
- ^ «Определение САЛЕРАТУСА» . www.merriam-webster.com . Проверено 6 декабря 2020 г.
- ^ «История компании» . Church & Dwight Co. Архивировано из оригинала 16 октября 2011 года.
- ^ Киплинг Р. (1897). Капитаны отважные . п. 25.
- ^ Бристоу Н.К. (2012), Американская пандемия: затерянные миры эпидемии гриппа 1918 года , Oxford University Press, стр. 178, ISBN 978-0199811342
- ^ Тиме С (2000). «Карбонаты натрия». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a24_299 . ISBN 3527306730 .
- ^ Холлеман А.Ф., Виберг Э. (2001). Неорганическая химия . Сан-Диего: Академическая пресса. ISBN 0-12-352651-5 .
- ^ Страница 45, раздел 3.6.2.1 «Справочного документа по передовым методам обработки (BREF) для кальцинированной соды», отчета, подготовленного Европейской ассоциацией производителей кальцинированной соды . Архивировано 3 октября 2006 г. в Wayback Machine , март 2004 г.
- ^ «Утиный суп (1933)» . IMDB . Проверено 4 августа 2015 г.
- ^ «Ночь в опере (1935)» . IMDB . Проверено 4 августа 2015 г.
Библиография [ править ]
- Хейнс WM, изд. (2011). Справочник CRC по химии и физике (92-е изд.). ЦРК Пресс . ISBN 978-1439855119 .