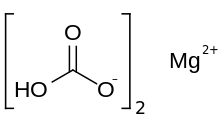
Бикарбонат магния
 | |
| Имена | |
|---|---|
| Название ИЮПАК Гидрокарбонат магния | |
| Другие имена Бикарбонат магния | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.016.582 |
| Номер ЕС |
|
| номер Е | E504(ii) (регуляторы кислотности, ...) |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| Mg(HCO 3 ) 2 | |
| Молярная масса | 146.34 g/mol |
| 5,7 г/(100 мл) | |
| Родственные соединения | |
Другие катионы | Бикарбонат кальция |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Бикарбонат магния или магния , Mg ( HCO3 собой 2 ) гидрокарбонат , представляет бикарбонатную соль магния . Он может образоваться в результате реакции разбавленных растворов угольной кислоты (например, сельтерской воды ) и гидроксида магния (магниевого молока).
Его можно получить синтезом ацетата магния и бикарбоната натрия :
- Mg(CH 3 COO) 2 + 2 NaHCO 3 → Mg(HCO 3 ) 2 + 2 CH 3 COONa
Бикарбонат магния существует только в водном растворе. Магний не образует твердый бикарбонат, как литий. Для его получения суспензию гидроксида магния обрабатывают углекислым газом под давлением , получая раствор бикарбоната магния: [1]
- Mg(OH) 2 + 2 CO 2 → Mg(HCO 3 ) 2
Высушивание полученного раствора приводит к разложению бикарбоната магния с образованием карбоната магния , диоксида углерода и воды:
- мг 2+ + 2HCO3 − → MgCO 3 + CO 2 + H 2 O
Ссылки
[ редактировать ]- ^ Маргарет Сигер; Уолтер Отто; Вильгельм Флик; Фридрих Бикельгаупт; Отто С. Аккерман. «Соединения магния». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a15_595.pub2 . ISBN 978-3527306732 .