Карбонат кобальта(II)
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Карбонат кобальта(II) | |
| Другие имена карбонат кобальта; соль кобальта(II) | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.007.428 |
ПабХим CID | |
| НЕКОТОРЫЙ |
|
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| КоСО 3 | |
| Молярная масса | 118.941 g/mol |
| Появление | красно-розовый твердый |
| Плотность | 4,13 г/см 3 |
| Температура плавления | 427 ° С (801 ° F; 700 К) [3] разлагается перед плавлением на оксид кобальта (II) (безводный) 140 ° С (284 ° F; 413 К) разлагается (гексагидрат) |
| 0,000142 г/100 мл (20 °С) [1] | |
Произведение растворимости ( K sp ) | 1.0·10 −10 [2] |
| Растворимость | растворим в кислоте незначительно в спирте , метилацетате нерастворим в этаноле |
Показатель преломления ( n D ) | 1.855 |
| Структура | |
| Ромбоэдрический (безводный) Тригональный (гексагидрат) | |
| Термохимия | |
Стандартный моляр энтропия ( S ⦵ 298 ) | 79,9 Дж/моль·К [3] |
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | −722,6 кДж/моль [3] |
Свободная энергия Гиббса (Δ f G ⦵ ) | -651 кДж/моль [3] |
| Опасности | |
| СГС Маркировка : | |
  [4] [4] | |
| Предупреждение | |
| Х302 , Х315 , Х317 , Х319 , Х335 , Х351 [4] | |
| П261 , П280 , П305+П351+П338 [4] | |
| NFPA 704 (огненный алмаз) | |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза ) | 640 мг/кг (перорально, крысы) |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Карбонат кобальта(II) — неорганическое соединение формулы CoCO 3 . Это красноватое парамагнитное твердое вещество является промежуточным продуктом гидрометаллургической очистки кобальта из руд. Это неорганический пигмент и предшественник катализаторов . [5] Карбонат кобальта(II) также встречается в виде редкого красно-розового минерала сферокобальтита . [6]
Подготовка и структура
[ редактировать ]Его готовят соединением растворов сернокислого кобальта и бикарбоната натрия :
- CoSO 4 + 2 NaHCO 3 → CoCO 3 + Na 2 SO 4 + H 2 O + CO 2
Эта реакция используется при осаждении кобальта из экстракта его обожженных руд. [5]
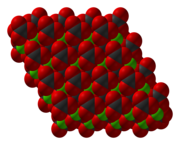
CoCO 3 имеет структуру, подобную кальциту , состоящую из кобальта с октаэдрической координационной геометрией . [7]
Реакции
[ редактировать ]Как и большинство карбонатов переходных металлов, карбонат кобальта нерастворим в воде, но легко подвергается воздействию минеральных кислот:
- CoCO 3 + 2 HCl + 5 H 2 O → [Co(H 2 O) 6 ]Cl 2 + CO 2
Его используют для приготовления многих координационных комплексов. Реакция карбоната кобальта(II) и ацетилацетона в присутствии перекиси водорода дает трис(ацетилацетонато)кобальт(III) . [8]
Нагревание карбоната происходит обычным для прокаливания способом , за исключением того, что продукт частично окисляется:
- 6CoCO3 3 + O2 → 2Co3O4 3O4 + CO6CO2
Образующийся Co 3 O 4 обратимо превращается в CoO при высоких температурах. [9]
Использование
[ редактировать ]Карбонат кобальта является предшественником карбонила кобальта и различных солей кобальта. Он входит в состав пищевых добавок, поскольку кобальт является важным элементом . Это предшественник синей керамической глазури, известной в случае с фаянсовой посудой .
Родственные соединения
[ редактировать ]Известны как минимум два карбонат-гидроксида кобальта(II): Co 2 (CO 3 )(OH) 2 и Co 6 (CO 3 ) 2 (OH) 8 ·H 2 O. [10]
Умеренно редкий сферокобальтит представляет собой природную форму карбоната кобальта, хорошие образцы которого доставляются, в частности, из Республики Конго . «Кобальтокальцит» представляет собой кобальтоносную разновидность кальцита очень похожую , по своим свойствам на сферокобальтит. [6]
Безопасность
[ редактировать ]Токсичность наблюдалась редко. Животные, включая человека, нуждаются в следовых количествах кобальта, компонента витамина B12 . [5]
Ссылки
[ редактировать ]- ^ Хейнс, WM, изд. (2017). Справочник CRC по химии и физике (97-е изд.). CRC Press, Taylor & Francisco Group. стр. 4–58. ISBN 978-1-4987-5429-3 .
- ^ «Константы произведения растворимости» . Архивировано из оригинала 15 июня 2012 г. Проверено 17 мая 2012 г.
- ^ Jump up to: а б с д «Карбонат кобальта(II)» .
- ^ Jump up to: а б с Sigma-Aldrich Co. , Карбонат кобальта(II) . Проверено 6 мая 2014 г.
- ^ Jump up to: а б с Дональдсон, Джон Даллас; Байерсманн, Детмар (2005). «Кобальт и соединения кобальта». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a07_281.pub2 . ISBN 3527306730 .
- ^ Jump up to: а б «Сферокобальтит: информация и данные о минерале сферокобальтита» . www.mindat.org . Проверено 7 августа 2018 г.
- ^ Пертлик, Ф. (1986). «Структура гидротермально синтезированного карбоната кобальта (II) и карбоната никеля (II)». Acta Crystallographica Раздел C. 42 : 4–5. дои : 10.1107/S0108270186097524 .
- ^ Брайант, Берл Э.; Фернелиус, В. Конард (1957). «Ацетилацетонат кобальта (III)». Неорганические синтезы . стр. 188–189. дои : 10.1002/9780470132364.ch53 . ISBN 9780470132364 .
- ^ Г. А. Эль-Шобаки, А. С. Ахмад, А. Н. Аль-Ноаими и Х. Г. Эль-Шобаки Журнал термического анализа и калориметрии, 1996, том 46, номер 6, стр. 1801-1808. онлайн аннотация
- ^ Бходжане, Пратик; Ле Бэйль, Армель; Шираге, Парашарам М. (2019). «Через четверть века после его синтеза и с более чем 200 статьями, основанными на его использовании, Co(CO 3 ) 0,5 (OH) 0,11 H 2 O' оказывается Co 6 (CO 3 ) 2 (OH) 8 ·H. 2 O по данным порошковой синхротронной дифракции» . Acta Crystallographica Раздел C: Структурная химия . 75 (Часть 1): 61–64. дои : 10.1107/S2053229618017734 . ПМИД 30601132 . S2CID 58657483 .
Внешние ссылки
[ редактировать ] СМИ, связанные с карбонатом кобальта (II), на Викискладе?
СМИ, связанные с карбонатом кобальта (II), на Викискладе?
