Оксид лития-кобальта
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК оксид лития-кобальта(III) | |
| Другие имена литий-кобальтит | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.032.135 |
| Номер ЕС |
|
ПабХим CID | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| ЛиКоО 2 | |
| Молярная масса | 97.87 g mol −1 |
| Появление | кристаллическое вещество темно-синего или голубовато-серого цвета |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | вредный |
| СГС Маркировка : | |
  | |
| Опасность | |
| Х317 , Х350 , Х360 | |
| P201 , P202 , P261 , P272 , P280 , P281 , P302+P352 , P308+P313 , P321 , P333+P313 , P363 , P405 , P501 | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Оксид лития-кобальта , иногда называемый кобальтатом лития. [2] или литий-кобальтит , [3] химическое соединение формулы LiCoO
2 . Атомы кобальта формально находятся в степени окисления +3, отсюда ИЮПАК называет оксид лития-кобальта (III) .
Оксид лития-кобальта представляет собой темно-синее или голубовато-серое кристаллическое вещество. [4] и обычно используется в положительных электродах литий -ионных батарей .
Структура
[ редактировать ]Строение LiCoO
2 был изучен с помощью многочисленных методов, включая дифракцию рентгеновских лучей , электронную микроскопию нейтронов , дифракцию на порошке и EXAFS . [5]
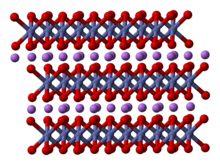
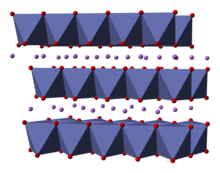
Твердое тело состоит из слоев одновалентных катионов лития ( Li +
), которые лежат между протяженными анионными листами атомов кобальта и кислорода, расположенными в виде октаэдров с общими ребрами , с двумя гранями, параллельными плоскости листа. [6] Атомы кобальта формально находятся в трехвалентной степени окисления ( Co 3+
) и зажаты между двумя слоями атомов кислорода ( O 2−
).
В каждом слое (кобальта, кислорода или лития) атомы расположены в правильной треугольной решетке. Решетки смещены так, что атомы лития находятся дальше всего от атомов кобальта, а структура повторяется в направлении, перпендикулярном плоскостям, через каждые три слоя кобальта (или лития). Симметрия точечной группы в обозначениях Германа-Могена , что означает элементарную ячейку с тройной неправильной вращательной симметрией и зеркальной плоскостью. Тройная ось вращения (которая нормальна к слоям) называется несобственной, потому что треугольники кислорода (находящиеся на противоположных сторонах каждого октаэдра) противонаправлены. [7]
Подготовка
[ редактировать ]Полностью восстановленный оксид лития-кобальта можно получить нагреванием стехиометрической смеси карбоната лития Li.
2 СО
3 и оксид кобальта(II,III) Co
33О
4 или металлический кобальт при 600–800 °C, а затем отжиг продукта при 900 °C в атмосфере кислорода. многочасовой [6] [3] [7]

Частицы нанометрового размера, более подходящие для использования в качестве катода, также можно получить путем прокаливания гидрата оксалата кобальта β- CoC.
22О
4 · 2ч
2 O , в виде стержнеобразных кристаллов длиной около 8 мкм и шириной 0,4 мкм, с гидроксидом лития LiOH , до 750–900 °С. [9]
Третий метод использует ацетат лития , ацетат кобальта и лимонную кислоту в равных молярных количествах в водном растворе. Нагревание при 80°С превращает смесь в вязкий прозрачный гель. Затем высушенный гель измельчают и постепенно нагревают до 550°С. [10]
Использование в аккумуляторных батареях
[ редактировать ]Полезность оксида лития-кобальта в качестве интеркаляционного электрода была открыта в 1980 году исследовательской группой Оксфордского университета под руководством Джона Б. Гуденаф и Токийского университета из Коичи Мидзусима . [11]
В настоящее время это соединение используется в качестве катода в некоторых перезаряжаемых литий-ионных батареях с размерами частиц от нанометров до микрометров . [10] [9] Во время зарядки кобальт частично окисляется до состояния +4, при этом часть ионов лития переходит в электролит, в результате чего образуется ряд соединений Li.
х СоО
2 с 0 < x <1. [3]
Батареи, изготовленные с использованием LiCoO
2 имеют очень стабильную емкость, но имеют меньшую емкость и мощность, чем катоды с катодами на основе (особенно богатых никелем) никель-кобальт-алюминиевых (NCA) или никель-кобальт-марганцевых (NCM) оксидов. [12] Проблемы с термической стабильностью лучше для LiCoO.
2 катода, чем другие химические продукты с высоким содержанием никеля, хотя и незначительно. Это делает LiCoO
2 аккумулятора подвержены тепловому выходу из строя в случаях неправильного обращения, например, при работе при высоких температурах (>130 °C) или при перезарядке . При повышенных температурах LiCoO
2 при разложении образуется кислород , который затем вступает в реакцию с органическим электролитом элемента. Эту реакцию часто можно наблюдать в литий-ионных батареях , где батарея становится очень летучей и должна быть переработана безопасным способом. Разложение LiCoO 2 является проблемой безопасности из-за масштабов этой сильно экзотермической реакции , которая может распространиться на соседние элементы или воспламенить близлежащий горючий материал. [13] В целом это наблюдается для катодов многих литий-ионных аккумуляторов.
Процесс делитирования обычно осуществляется химическими средствами. [14] хотя был разработан новый физический процесс, основанный на циклах ионного распыления и отжига, [15] оставляя свойства материала неизменными.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ 442704 - Оксид лития-кобальта(III) (14.09.2012). «Страница продукта Sigma-Aldrich» . Sigmaaldrich.com . Проверено 21 января 2013 г.
{{cite web}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ А. Л. Емелина, М. А. Быков, М. Л. Ковба, Б. М. Сенявин, Е. В. Голубина (2011), «Термохимические свойства кобальтата лития». Российский физический химический журнал , том 85, выпуск 3, страницы 357–363; два : 10.1134/S0036024411030071
- ^ Jump up to: а б с Ондржей Янковский, Ян Коваржик, Йиндржих Лейтнер, Светослав Ружичка, Давид Седмидубский (2016) «Термодинамические свойства стехиометрического кобальтита лития LiCoO2». Термохимика Акта , том 634, страницы 26-30. дои : 10.1016/j.tca.2016.04.018
- ^ LinYi Gelon New Battery Materials Co., Ltd, «Оксид лития-кобальта (LiCoO2) для литий-ионных аккумуляторов» . Запись в каталоге, доступ осуществлен 10 апреля 2018 г.,
- ^ И. Накаи; К. Такахаши; Ю. Сираиси; Т. Накагоме; Ф. Идзуми; Ю. Исии; Ф. Нисикава; Т. Кониши (1997). «Тонкая структура рентгеновского поглощения и нейтронографический анализ поведения деинтеркаляции в системах LiCoO2 и LiNiO2». Журнал источников энергии . 68 (2): 536–539. Бибкод : 1997JPS....68..536N . дои : 10.1016/S0378-7753(97)02598-6 .
- ^ Jump up to: а б Шао-Хорн, Ян ; Крогенек, Лоуренс; Дельмас, Клод; Нельсон, Э. Крис; О'Киф, Майкл А. (июль 2003 г.). «Атомное разрешение ионов лития в LiCoO
2 " . Nature Materials . 2 (7): 464–467. : 10.1038 /nmat922 . PMID 12806387. S2CID doi 34357573 . - ^ Jump up to: а б Х. Дж. Орман и П. Дж. Уайзман (январь 1984 г.). «Оксид лития кобальта(III), CoLiO
2 : уточнение структуры методом порошковой нейтронной дифракции». Acta Crystallographica Раздел C. 40 ( 1): 12–14. doi : 10.1107/S0108270184002833 . - ^ Ци, Чжаосян; Кениг, Гэри М. (16 августа 2016 г.). «Высокоэффективные субмикрометровые материалы LiCoO2, полученные в результате масштабируемой обработки шаблонов микрочастиц». ХимияВыбрать . 1 (13): 3992–3999. дои : 10.1002/slct.201600872 . ISSN 2365-6549 .
- ^ Jump up to: а б Ци, Чжаосян (август 2016 г.). «Высокоэффективные субмикрометровые материалы LiCoO2, полученные в результате масштабируемой обработки шаблонов микрочастиц». ХимияВыбрать . 1 (13): 3992–3999. дои : 10.1002/slct.201600872 .
- ^ Jump up to: а б Тан, В.; Лю, LL; Тиан, С.; Ли, Л.; Юэ, Ю.Б.; Ву, Ю.П.; Гуань, Ю.Ю.; Чжу, К. (01 ноября 2010 г.). «Нано-LiCoO2 как катодный материал большой емкости и высокой емкости для водных перезаряжаемых литиевых батарей». Электрохимические коммуникации . 12 (11): 1524–1526. дои : 10.1016/j.elecom.2010.08.024 .
- ^ К. Мидзушима, ПК Джонс, П. Дж. Уайзман, Дж. Б. Гуденаф (1980), « Ли
х СоО
2 (0 < x <1): новый катодный материал для батарей с высокой плотностью энергии». Бюллетень исследований материалов , том 15, страницы 783–789. дои : 10.1016/0025-5408(80)90012-4 - ^ Освальд, Стефан; Гастайгер, Хуберт А. (01 марта 2023 г.). «Предел структурной устойчивости слоистых оксидов переходных металлов лития вследствие выделения кислорода при высоком заряде и его зависимость от содержания никеля» . Журнал Электрохимического общества . 170 (3): 030506. doi : 10.1149/1945-7111/acbf80 . ISSN 0013-4651 . S2CID 258406065 .
- ^ Даути, Дэниел; Песаран, Ахмад. «Руководство по дорожной карте безопасности автомобильных аккумуляторов» (PDF) . Национальная лаборатория возобновляемых источников энергии . Проверено 19 января 2013 г.
- ^ Аурбах, Д. (2 июня 2002 г.). «Краткий обзор механизмов разрушения металлических литиевых и литий-графитовых анодов в растворах жидких электролитов» . Ионика твердого тела . 148 (3–4): 405–416. дои : 10.1016/S0167-2738(02)00080-2 .
- ^ Салагре, Елена; Сеговия, Пилар; Гонсалес-Баррио, Мигель Анхель; Юговац, Маттео; Морас, Паоло; Пис, Игорь; Бондино, Федерика; Пирсон, Джастин; Ван, Ричмонд Шивэй; Такеучи, Ичиро; Фуллер, Эллиот Дж.; Талин, Алек А.; Маскарак, Арантсасу; Мишель, Энрике Г. (2 августа 2023 г.). «Физическое делитирование эпитаксиальных катодов аккумуляторов LiCoO 2 как платформа для исследования электронной структуры поверхности» . Прикладные материалы и интерфейсы ACS . 15 (30): 36224–36232. дои : 10.1021/acsami.3c06147 . hdl : 10486/708446 . ISSN 1944-8244 .
Внешние ссылки
[ редактировать ]- Изображение структуры оксида лития-кобальта на атомном уровне. Архивировано 13 января 2008 г. на Wayback Machine Национальной лаборатории Лоуренса в Беркли.
