Бис(триметилсилил)амид лития
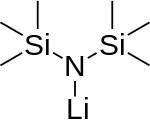 Мономер (не существует)
| |
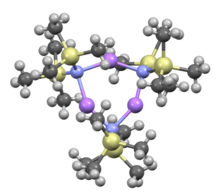
 Циклический тример
| |
| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
1,1,1-триметил -N- (триметилсилил)силанаминид лития | |
| Другие имена
Лития гексаметилдисилазид
Литиевая соль гексаметилдисилазана | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.021.569 |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| LiN(Si(CH 3 ) 3 ) 2 | |
| Молярная масса | 167.33 g·mol −1 |
| Появление | Белый твердый |
| Плотность | 0,86 г/см 3 и 25 °С |
| Температура плавления | От 71 до 72 ° C (от 160 до 162 ° F; от 344 до 345 К) |
| Точка кипения | От 80 до 84 ° C (от 176 до 183 ° F; от 353 до 357 К) (0,001 мм рт. ст.) |
| разлагается | |
| Растворимость | Большинство апротонных растворителей ТГФ , гексан , толуол |
| Кислотность ( pKa ) | 26 |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
легковоспламеняющийся, коррозионный |
| Родственные соединения | |
Родственные соединения
|
Бис(триметилсилил)амид натрия Бис(триметилсилил)амид калия |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Бис(триметилсилил)амид лития представляет собой литированное кремнийорганическое соединение формулы LiN(Si(CH 3 ) 3 ) 2 . Его обычно называют LiHMDS или (HMDS) ( литий - гексаметилдисилазид HMDS основном . в и ненуклеофильного - ссылка на сопряженную с ним ) Li используется в качестве сильного основания и лиганда кислоту Как и многие литиевые реагенты, он имеет тенденцию к агрегации и образует циклический тример в отсутствие координирующих частиц.
Подготовка
[ редактировать ]LiHMDS коммерчески доступен, но его также можно получить депротонированием бис (триметилсилил)амина н - бутиллитием . [ 1 ] Эту реакцию можно провести in situ . [ 2 ]
- HN(Si(CH 3 ) 3 ) 2 + C 4 H 9 Li → LiN(Si(CH 3 ) 3 ) 2 + C 4 H 10
После образования соединение можно очистить сублимацией или перегонкой .
Реакции и применение
[ редактировать ]В качестве основы
[ редактировать ]LiHMDS часто используется в органической химии как сильное ненуклеофильное основание . [ 3 ] Сопряженная с ним кислота имеет ~ pKa , 26 [ 4 ] что делает его менее основным, чем другие литиевые основания, такие как LDA (p K a сопряженной кислоты ~ 36). Он относительно более стерически затруднен и, следовательно, менее нуклеофильен , чем другие литиевые основания. Его можно использовать для образования различных литийорганических соединений, в том числе ацетилидов. [ 3 ] или еноляты лития . [ 2 ]

где Я = Ч 3 . По существу, он находит применение в ряде реакций сочетания, особенно в реакциях образования углерод-углеродных связей, таких как алкилирование Фратера-Зеебаха и смешанная конденсация Кляйзена .
Альтернативный синтез тетранитрида тетрасеры предполагает использование S(N(Si(CH 3 ) 3 ) 2 ) 2 в качестве предшественника с заранее образованными связями S–N. S(N(Si(CH 3 ) 3 ) 2 ) 2 получают реакцией бис(триметилсилил)амида лития и дихлорида серы ( SCl 2 ).
- 2 LiN(Si(CH 3 ) 3 ) 2 + SCl 2 → S(N(Si(CH 3 ) 3 ) 2 ) 2 + 2 LiCl
The S(N(Si(CH 3 ) 3 ) 2 ) 2 реагирует с комбинацией SCl 2 и сульфурилхлорид ( SO 2 Cl 2 ) с образованием S 4 N 4 , триметилсилилхлорид и диоксид серы : [ 5 ]
- 2 S(N(Si(CH 3 ) 3 ) 2 ) 2 + 2 SCl 2 + 2 SO 2 Cl 2 → S 4 N 4 + 8 (CH 3 ) 3 SiCl + 2 SO 2
В качестве лиганда
[ редактировать ]Li(HMDS) может реагировать с широким спектром галогенидов металлов посредством реакции метатезиса солей с образованием бис(триметилсилил)амидов металлов .
- MX n + n Li(HMDS) → M(HMDS) n + n LiX
где X = Cl, Br, I и иногда F
Комплексы бис(триметилсилил)амида металлов являются липофильными из-за лиганда и, следовательно, растворимы в ряде неполярных органических растворителей , что часто делает их более реакционноспособными, чем соответствующие галогениды металлов, которые может быть трудно солюбилизировать. Стерическая ; масса лигандов делает их комплексы дискретными и мономерными дальнейшее повышение их реакционной способности. Имея встроенное основание, эти соединения легко реагируют с предшественниками протонных лигандов с образованием других комплексов металлов и, следовательно, являются важными предшественниками более сложных координационных соединений . [ 6 ]
Нишевое использование
[ редактировать ]LiHMDS летуч, и его использование обсуждалось для атомно-слоевого осаждения соединений лития. [ 7 ]
Структура
[ редактировать ]Как и многие литийорганические реагенты, бис(триметилсилил)амид лития может образовывать агрегаты в растворе. Степень агрегации зависит от растворителя. В координационных растворителях, таких как эфиры [ 8 ] и амины , [ 9 ] мономер . и димер преобладают В мономерном и димерном состоянии одна или две молекулы растворителя связываются с литиевыми центрами. С аммиаком в качестве донорного основания бис(триметилсилил)амид лития образует трисольватированный мономер, стабилизированный межмолекулярными водородными связями. [ 10 ] [ 11 ] В некоординирующих растворителях, таких как ароматические соединения или пентан , преобладают сложные олигомеры , включая тример. [ 9 ] В твердом состоянии структура тримерная. [ 12 ]

| ||||
 Аддукт LiHMDS с TMEDA |
 ТГФ : Сольватированный димер [(LiHMDS) 2 (THF) 2 ] |
 Тример, не содержит растворителей: [(ЛиГМДС) 3 ] | ||
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Амоноо-Нейзер, Э.Х.; Шоу, РА; Сковлин, ДО; Смит, Британская Колумбия (1966). «Бис(триметилсилил)амид лития и трис(триметилсилил)амин». Неорганические синтезы . Том. 8. стр. 19–22. дои : 10.1002/9780470132395.ch6 . ISBN 978-0-470-13239-5 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Jump up to: а б Данхайзер, РЛ; Миллер, РФ; Брисбуа, Р.Г. (1990). «Детрифторацетилирующий перенос диазогруппы: ( E )-1-диазо-4-фенил-3-бутен-2-он» . Органические синтезы . 73 :134 ; Сборник томов , т. 9, с. 197 .
- ^ Jump up to: а б Ву, Джордж; Хуан, Миншэн (июль 2006 г.). «Литийорганические реагенты в фармацевтических асимметричных процессах». Химические обзоры . 106 (7): 2596–2616. дои : 10.1021/cr040694k . ПМИД 16836294 .
- ^ Фрейзер, Роберт Р.; Мансур, Тарек С.; Савард, Сильвен (август 1985 г.). «Измерения кислотности пиридинов в тетрагидрофуране с использованием литированных силиламинов». Журнал органической химии . 50 (17): 3232–3234. дои : 10.1021/jo00217a050 .
- ^ Маанинен, А.; Швари, Дж.; Лайтинен, Р.С.; Чиверс, Т. (2002). «Соединения общего интереса». В Кукуванисе, Дмитрий (ред.). Неорганические синтезы . Том. 33. Нью-Йорк: John Wiley & Sons, Inc., стр. 196–199. дои : 10.1002/0471224502.ch4 . ISBN 9780471208259 .
- ^ Майкл Лапперт , Андрей Протченко, Филип Пауэр , Александра Сибер (2009). Химия амидов металлов . Вайнхайм: Wiley-VCH. дои : 10.1002/9780470740385 . ISBN 978-0-470-72184-1 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Хямяляйнен, Яни; Холопайнен, Яни; Мунник, Франс; Хатанпяя, Тимо; Хейккиля, Микко; Ритала, Микко; Лескеля, Маркку (2012). «Тонкие пленки фосфата лития, выращенные методом атомно-слоевого осаждения». Журнал Электрохимического общества . 159 (3): А259–А263. дои : 10.1149/2.052203jes .
- ^ Лухт, Бретт Л.; Коллум, Дэвид Б. (1995). «Эфирная сольватация гексаметилдисилазида лития: неожиданные взаимосвязи числа сольватации, энергии сольватации и агрегатного состояния». Журнал Американского химического общества . 117 (39): 9863–9874. дои : 10.1021/ja00144a012 .
- ^ Jump up to: а б Лухт, Бретт Л.; Коллум, Дэвид Б. (1996). «Сольватация ионов лития: аминные и ненасыщенные углеводородные сольваты гексаметилдисилазида лития (LiHMDS)». Журнал Американского химического общества . 118 (9): 2217–2225. дои : 10.1021/ja953029p .
- ^ Нойфельд, Р.; Мишель, Р.; Хербст-Ирмер, Р.; Шёне, Р.; Сталке, Д. (2016). «Введение донора водородной связи в слабонуклеофильное основание Бренстеда: гексаметилдисилазиды щелочных металлов (MHMDS, M = Li, Na, K, Rb и Cs) с аммиаком». хим. Евро. Дж. 22 (35): 12340–12346. дои : 10.1002/chem.201600833 . ПМИД 27457218 .
- ^ Нойфельд, Р.: Определение молекулярной массы внешней калибровочной кривой DOSY как ценная методология характеристики реакционноспособных промежуточных продуктов в растворе. В: eDiss, Университет Георга Августа, Геттинген. 2016.
- ^ Роджерс, Робин Д.; Этвуд, Джерри Л.; Грюнинг, Райнер (1978). «Кристаллическая структура N -литиогексаметилдисилазана, [LiN(SiMe 3 ) 2 ] 3 ». Дж. Органомет. хим. 157 (2): 229–237. дои : 10.1016/S0022-328X(00)92291-5 .