Хлорат лития
 | |
| Имена | |
|---|---|
| Другие имена Хлорная кислота, литиевая соль | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.033.288 |
ПабХим CID | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| LiClO 3 | |
| Молярная масса | 90.39 g/mol |
| Температура плавления | От 127,6 до 129 ° C (от 261,7 до 264,2 ° F; от 400,8 до 402,1 К) [2] [3] [4] |
| 241 г/100 мл (0 °С) 459 г/100 мл (25 °С) 777 г/100 мл (60 °С) 2226 г/100 мл (100 °С) [1] | |
| −28.8·10 −6 см 3 /моль | |
| Родственные соединения | |
Другие анионы | Хлорид лития Гипохлорит лития Перхлорат лития |
Другие катионы | Хлорат натрия Хлорат калия Хлорат цезия |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
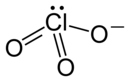
Хлорат лития – неорганическое химическое соединение формулы LiClO 3 .Как и все хлораты , он является окислителем и может стать нестабильным и, возможно, взрывоопасным при смешивании с органическими материалами, порошками химически активных металлов или серой.
Его можно получить реакцией горячего концентрированного гидроксида лития с хлором:
- 3 Cl 2 + 6 LiOH → 5 LiCl + LiClO 3 + 3 H 2 O
Хлорат лития имеет одну из самых высоких растворимостей в воде среди химических соединений. Это также шестиэлектронный окислитель. Его электрохимическому восстановлению способствуют кислоты, электрокатализаторы и окислительно-восстановительные медиаторы. Эти свойства делают хлорат лития полезным окислителем для с высокой плотностью энергии проточных батарей . [5] Хлорат лития имеет очень низкую температуру плавления для неорганической ионной соли.
Ссылки
[ редактировать ]- ^ Джон Рамбл (18 июня 2018 г.). Справочник CRC по химии и физике (99 изд.). ЦРК Пресс. стр. 4–47. ISBN 978-1138561632 .
- ^ Ван, Су-Чи Саймон (1983). «Электрохимия расплавленного хлората лития и его возможное использование с литием в батарее». Журнал Электрохимического общества . 130 (4): 741–747. Бибкод : 1983JElS..130..741W . дои : 10.1149/1.2119796 .
- ^ А. Н. Кэмпбелл, Э. М. Карцмарк, В. Б. Мэрик (1966). «Системы хлорат натрия — вода — диоксан и хлорат лития — вода — диоксан при 25°». Может. Дж. Чем . 44 (8): 935–937. дои : 10.1139/v66-136 . S2CID 97413079 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ http://scitation.aip.org/getabs/servlet/GetabsServlet?prog=normal&id=JESOAN000130000004000741000001&idtype=cvips&gifs=yes&ref=no [ мертвая ссылка ]
- ^ США 20140170511