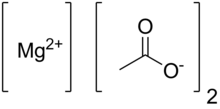
Ацетат магния
| |

| |
| Имена | |
|---|---|
| Название ИЮПАК
Ацетат магния
| |
| Идентификаторы | |
| |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.005.050 |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| Мг(СН 3 СОО) 2 | |
| Молярная масса | 142,394 (безводный) 214,455 (тетрагидрат) |
| Появление | Белые гигроскопичные кристаллы |
| Плотность | 1,45 г/см 3 (тетрагидрат) |
| Температура плавления | 80 ° C (176 ° F, 353 К) (тетрагидрат) |
| Растворимый | |
| −116.0·10 −6 см 3 /моль (+4 H 2 O | |
| Родственные соединения | |
Другие катионы
|
Ацетат кальция |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Безводный ацетат магния имеет химическую формулу Mg(C 2 H 3 O 2 ) 2 , а в его гидратированной форме - тетрагидрат ацетата магния - химическую формулу Mg(CH 3 COO) 2 • 4H 2 O. В этом соединении магний имеет степень окисления 2 + . Ацетат магния – это магниевая соль уксусной кислоты . [ 1 ] Он расплывается и при нагревании разлагается с образованием оксида магния . [ 2 ] Ацетат магния обычно используется в качестве источника магния в биологических реакциях. [ 3 ]
Физические свойства
[ редактировать ]Ацетат магния выглядит как белые гигроскопичные кристаллы. Он пахнет уксусной кислотой и растворим в воде. Когда он находится в водном растворе, его pH будет находиться на щелочной стороне нейтрального. [ 4 ] [ 5 ]
Хранилище
[ редактировать ]В связи с тем, что он очень гигроскопичен, его необходимо хранить вдали от воды. Он также несовместим с сильными окислителями и не должен смешиваться с ними. [ 6 ]
Синтез
[ редактировать ]Синтез ацетата магния реакцией гидроксида магния с уксусной кислотой. [ 7 ]
- 2 CH 3 COOH + Mg(OH) 2 → (CH 3 COO) 2 Mg + 2 H 2 O
Карбонат магния суспендируют в дистиллированной воде с 20% раствором уксусной кислоты. [ 8 ]
- 2 CH 3 COOH + MgCO 3 → Mg(CH 3 COO) 2 + CO 2 + H 2 O
Реакция металлического магния с уксусной кислотой, растворенной в сухом бензоле, приводит к образованию ацетата магния с выделением газообразного водорода. [ 9 ]
- Mg + 2CH 3 COOH → Mg(CH 3 COO) 2 + H 2
Использование и применение
[ редактировать ]В 1881 году Чарльз Кламонд изобрел корзину Кламонда , одну из первых эффективных газовых мантий . Реагенты, использованные в этом изобретении, включали ацетат магния, гидроксид магния и воду.
Ацетат магния обычно используется в качестве источника магния или ацетат-иона в химических экспериментах. Одним из примеров этого является использование ацетата магния и нитрата магния для моделирования молекулярной динамики и измерения поверхностного натяжения. В эксперименте авторы обнаружили, что ацетат обладает более сильным сродством к поверхности по сравнению с ионом нитрата и что ион Mg 2+ сильно отталкивается от взаимодействия воздуха и жидкости. Они также обнаружили, что Mg 2+ имел более сильную тенденцию связываться с ацетат-ионом по сравнению с нитратом. [ 10 ]
Одним из наиболее распространенных применений ацетата магния является смесь под названием ацетат кальция-магния (CMA). Это смесь ацетата кальция и ацетата магния. CMA считается экологически чистой альтернативой NaCl и CaCl 2 . CMA также действует как мощный агент контроля выбросов SO 2 , NO x и токсичных частиц в процессах сжигания угля, уменьшая кислотные дожди, а также как эффективный катализатор, способствующий сжиганию угля. [ 11 ]
Было обнаружено, что ацетат магния вызывает конформационные изменения Escherichia coli фермента примазы . Mg(OAc) 2 , MnCl 2 , CaCl 2 , NaOAc, LiCl, MgSO 4 и MgCl 2 В этом эксперименте сравнивали , чтобы увидеть, какое влияние они оказывают на фермент примазу Escherichia coli . Экспериментаторы обнаружили, что Mg(OAc) 2 вызывает наилучшие конформационные изменения. MgSO 4 и MgCl 2 слегка вызывали эффект, а остальные - нет. [ 12 ]
Когда ацетат магния смешивается с перекисью водорода, он действует как бактерицидное средство. [ 13 ]
Было показано, что ацетат магния эффективен при озолении органических соединений при подготовке к анализу на фтор, когда присутствуют высокие или низкие концентрации фтора. [ 14 ]
Безопасность
[ редактировать ]Ацетат магния является относительно безопасным соединением, и ему присвоен нулевой рейтинг опасности для здоровья. Однако всегда следует обращаться с ним в перчатках и защитных очках. При попадании в глаза, на кожу, при проглатывании или вдыхании он вызывает раздражение соответствующих участков: глаз, кожи, желудочно-кишечного тракта и легких. [ 15 ]
Ссылки
[ редактировать ]- ^ Ацетат магния . Опасность.com. Проверено 12 апреля 2012 г.
- ^ Поставщик ацетата магния и техническая информация American Elements, получено 12 апреля 2012 г.
- ^ «Информационный бюллетень Sigma-Aldrich об ацетате магния» (PDF) . Проверено 26 апреля 2012 г.
- ^ «Информационный бюллетень об ацетате магния Unisenchem» . Проверено 27 апреля 2012 г.
- ^ «Информационный бюллетень об ацетате магния Unisenchem» (PDF) . Архивировано из оригинала (PDF) 8 июля 2010 г. Проверено 16 декабря 2013 г.
- ^ «Информационный бюллетень об ацетате магния Unisenchem» . Проверено 27 апреля 2012 г.
- ^ Стоуффер, М.Р. «Адсорбенты для удаления H 2 , других соединений, вызывающих запах, и кислых газов из газовых потоков и способы производства и использования этих адсорбентов» . Проверено 25 апреля 2012 г.
- ^ Стащук П.; Пекальска, Дж. (2003). «Методы получения магниевых органических соединений из природного доломита». Физиохимические проблемы переработки полезных ископаемых . 37 : 149–158.
- ^ Энциклопедия химических реакций . 1957. с. 399.
- ^ Минофар, Бабак; Вача, Роберт; Вахаб, Абдул; Махиуддин, Сех; Кунц Вернер; Юнгвирт, Павел (2006). «Склонность к границе раздела воздух/вода и спариванию ионов в растворах ацетата магния и нитрата магния: моделирование молекулярной динамики и измерения поверхностного натяжения». Дж. Физ. Хим . 110 (32): 15939–15944. дои : 10.1021/jp060627p . ПМИД 16898748 .
- ^ Дионисий, Дионисий; Цианоу, Марина; Боцарис, Грегори (2000). «Экстракционная кристаллизация для производства ацетата кальция и ацетата магния из карбонатных источников». Индийский англ. хим. Рез . 39 (11): 4192–4202. дои : 10.1021/ie9906823 .
- ^ Урлахер, Тереза М.; Грип, Марк А. (1995). «Ацетат магния вызывает конформационные изменения примазы Escherichia coli». Биохимия . 34 (51): 16708–16714. дои : 10.1021/bi00051a020 . ПМИД 8527445 .
- ^ Виго, Т.Л., Данна, Г.Ф. «Продукты реакции ацетата магния и перекиси водорода для придания антибактериальной активности волокнистым субстратам» . Патент . Проверено 26 апреля 2012 г.
{{cite web}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Кратчфилд, В. младший (1942). «Ацетат магния как озолитель при анализе фтора». Индийский англ. хим. Анальный. Эд . 14 : 57–58. дои : 10.1021/i560101a023 .
- ^ «Паспорт безопасности материала Sigma-Aldrich» (PDF) . www.lakeland.edu . 07.02.2009.