Основной ацетат бериллия

| |
| Имена | |
|---|---|
| Систематическое название ИЮПАК
Гекса-мк-ацетат(О,О')-мк4-оксотетрабериллий(II) | |
| Другие имена
оксиацетат бериллия
Ацетат оксида бериллия Основной ацетат бериллия | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.038.881 |
| Номер ЕС |
|
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 12 ч. 18 быть 4 Ох 13 | |
| Молярная масса | 406.3122 g/mol |
| Появление | бесцветный |
| Температура плавления | 285 ° С (545 ° F; 558 К) |
| Точка кипения | 330 ° С (626 ° F; 603 К) |
| Растворимость в хлороформе | растворимый |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
высокотоксичный |
| NIOSH (пределы воздействия на здоровье в США): | |
ПЭЛ (допустимо)
|
СВВ 0,002 мг/м 3 С 0,005 мг/м 3 (30 минут), с максимальным пиком 0,025 мг/м. 3 (как Бэ) [ 1 ] |
РЕЛ (рекомендуется)
|
Са С 0,0005 мг/м 3 (как Бэ) [ 1 ] |
IDLH (Непосредственная опасность)
|
Са [4 мг/м 3 (как Бэ)] [ 1 ] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Основной ацетат бериллия представляет собой химическое соединение формулы Be 4 O(O 2 CCH 3 ) 6 . Это соединение имеет своеобразную структуру, но не имеет применения и изучено лишь незначительно. Это бесцветное твердое вещество, растворимое в органических растворителях.
Подготовка
[ редактировать ]Его можно получить обработкой основного карбоната бериллия горячей уксусной кислотой .
- 2 Be 2 CO 3 (OH) 2 + 6 AcOH → Be 4 O(AcO) 6 + 5 H 2 O + 2 CO 2
Основной ацетат бериллия нерастворим в воде, но растворим в хлороформе , что соответствует его неполярности. Плавится и сублимируется в вакууме без разложения. [ 2 ]
Структура
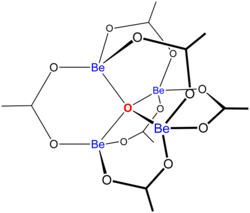
[ редактировать ]«Основные ацетаты » состоят из ансамбля металлических центров, связанных с центральным оксидным ионом, и набора ацетатных лигандов . Основной ацетат бериллия имеет тетраэдрический Be 4 O. 6+ ядро с ацетатами (CH 3 CO 2 − ), охватывающий каждую из пар Be 2+ центры. [ 3 ] [ 4 ] Он состоит из переплетенных шестичленных колец Be 2 O 3 C. Структура обусловлена его значительной стабильностью (соединение перегоняется при 330 ° C).
Использование
[ редактировать ]Растворимость соли в органических растворителях (хлороформе) полезна для извлечения и очистки фракций, богатых бериллием, для многих целей. Монокристаллы основного ацетата бериллия можно легко вырастить, и они полезны для юстировки рентгеновских дифрактометров, а также в качестве эталона в кристаллографии белков.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с Карманный справочник NIOSH по химическим опасностям. «#0054» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Мёллер, Т. (1950). «Основные бериллиевые производные органических кислот». В Одриет, LF (ред.). Неорганические синтезы, Том 3 . Том. 3. Джон Уайли и сыновья . стр. 4–9. дои : 10.1002/9780470132340.ch2 . ISBN 978-0-470-13234-0 .
- ^ Брэгг, штат Вашингтон (1923). «Кристаллическая структура основного ацетата бериллия» . Природа . 111 (2790): 532. Бибкод : 1923Natur.111..532B . дои : 10.1038/111532a0 .
- ^ Полинг, Л .; Шерман, Дж. (1934). «Структура карбоксильной группы. II. Кристаллическая структура основного ацетата бериллия» (PDF) . Труды Национальной академии наук . 20 (6): 340–5. Бибкод : 1934PNAS...20..340P . дои : 10.1073/pnas.20.6.340 . ПМК 1076415 . ПМИД 16587899 .