Ацетат ртути(II)

| |
| |
| Имена | |
|---|---|
| Другие имена
ацетат ртути
ацетат ртути | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.014.993 |
| Номер ЕС |
|
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 1629 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 4 Н 6 О 4 Ртуть | |
| Молярная масса | 318.678 g/mol |
| Появление | белое твердое вещество |
| Запах | легкий уксуса запах |
| Плотность | 3,28 г/см 3 , твердый |
| Температура плавления | 179 ° C (354 ° F, 452 К) (разлагается) |
| 25 г/100 мл (10 °С) 100 г/100 мл (100 °С) | |
| Растворимость | растворим в спирте , диэтиловом эфире |
| −100·10 −6 см 3 /моль | |
| Опасности | |
| СГС Маркировка : | |
  
| |
| Опасность | |
| Х300 , Х310 , Х330 , Х373 , Х410 | |
| P260 , P262 , P264 , P270 , P271 , P273 , P280 , P284 , P301+P310 , P302+P350 , P304+P340 , P310 , P314 , P320 , P321 , P322 , P330 , P361 , П363 , П391 , П403+П233 , П405 , П501 | |
| NFPA 704 (огненный алмаз) | |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза )
|
40,9 мг/кг (крыса, перорально) 23,9 мг/кг (мыши, перорально) [1] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
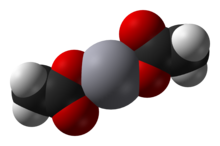
Ацетат ртути(II) , также известный как ацетат ртути, собой химическое соединение , соль ртути(II) уксусной кислоты с формулой Hg ( O 2 C CH 2 3 ) представляет . Обычно сокращенно Hg(OAc) 2 , это соединение используется в качестве реагента для получения ртутьорганических соединений из ненасыщенных органических предшественников. Это белое водорастворимое твердое вещество, но некоторые образцы со временем могут становиться желтоватыми из-за разложения.
Структура
[ редактировать ]Ацетат ртути(II) представляет собой кристаллическое твердое вещество, состоящее из изолированных молекул Hg(OAc) 2 с расстоянием Hg-O 2,07 Å . Также присутствуют три длинные и слабые межмолекулярные связи Hg···O размером около 2,75 Å, что приводит к слегка искаженной квадратно-пирамидальной координационной геометрии Hg. [2]
Синтез и реакции
[ редактировать ]Ацетат ртути(II) можно получить реакцией оксида ртути с уксусной кислотой . [3]
HgO + 2 CH 3 COOH → Hg(CH 3 COO) 2 + H 2 O
Неорганические реакции
[ редактировать ]Ацетат ртути(II) в растворе уксусной кислоты реагирует с H 2 S , вызывая быстрое осаждение черной (β) полиморфной модификации HgS . При осторожном нагревании суспензии черное твердое вещество превращается в красную форму. [4] Минерал киновари — красный HgS. Осаждение HgS, а также некоторых других сульфидов с использованием сероводорода является этапом качественного неорганического анализа .
Органическая химия
[ редактировать ]Богатые электронами арены подвергаются «меркурации» при обработке Hg(OAc) 2 . Такое поведение иллюстрируется фенолом :
- C 6 H 5 OH + Hg(OAc) 2 → C 6 H 4 (OH)-2-HgOAc + HOAc
Оставшаяся у ртути ацетатная группа (ОАс) может быть заменена хлоридом: [5]
- C 6 H 4 (OH)-2-HgOAc + NaCl → C 6 H 4 (OH)-2-HgCl + NaOAc
ртуть 2+ Центр связывается с алкенами , индуцируя присоединение гидроксида и алкоксида . Например, обработка метилакрилата ацетатом ртути в метаноле дает сложный эфир α-ртути: [6]
- Hg(OAc) 2 + CH 2 =CHCO 2 CH 3 + CH 3 OH → CH 3 OCH 2 CH(HgOAc)CO 2 CH 3 + HOAc
Используя высокое сродство ртути(II) к серным лигандам, Hg(OAc) 2 можно использовать в качестве реагента для снятия защиты с тиоловых групп в органическом синтезе . Аналогичным образом Hg(OAc) 2 использовалась для превращения тиокарбоната эфиров в дитиокарбонаты:
- (RS) 2 C=S + H 2 O + Hg(OAc) 2 → (RS) 2 C=O + HgS + 2 HOAc
Ацетат ртути (II) используется в реакциях оксимеркурации .
Известным применением Hg(OAc) 2 был синтез идоксуридина .
Токсичность
[ редактировать ]Ацетат ртути является высокотоксичным соединением, поскольку он водорастворим и содержит ионы ртути. Симптомы отравления ртутью включают периферическую невропатию , изменение цвета и шелушение кожи (шелушение и/или шелушение кожи). [7] Хроническое воздействие может вызвать снижение интеллекта и почечную недостаточность . [8]
Ссылки
[ редактировать ]- ^ «Ртуть (органо)алкильные соединения (в виде Hg)» . Непосредственно опасные для жизни и здоровья концентрации (IDLH) . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Оллманн, Р. (1973). «Строение ацетата ртути(II)» . Журнал кристаллографии - Кристаллические материалы . 138 (1–6): 366–373. дои : 10.1524/zkri.1973.138.jg.366 . S2CID 96160619 .
- ^ Ф. Вагенкнехт; Р. Джуза (1963). «Ацетат ртути(II)». В Г. Брауэре (ред.). Справочник по препаративной неорганической химии, 2-е изд . Том. 2. Нью-Йорк, Нью-Йорк: Академик Пресс. п. 1120.
- ^ Ньюэлл, Лайман К.; Мэксон, Р.Н.; Филсон, Миннесота (1939). «Красный сульфид ртути». Неорганические синтезы . Том. 1. С. 19–20. дои : 10.1002/9780470132326.ch7 . ISBN 9780470132326 .
- ^ Уитмор, ФК; Хэнсон, ER (1925). « О -Хлормеркурифенол». Органические синтезы . 4 : 13. дои : 10.15227/orgsyn.004.0013 .
- ^ Картер, Герберт Э.; Уэст, Гарольд Д. (1940). «ДЛ-Серин». Органические синтезы . 20:81 . дои : 10.15227/orgsyn.020.0081 .
- ^ Бернхофт, Робин А. (2012). «Токсичность ртути и ее лечение: обзор литературы» . Журнал окружающей среды и общественного здравоохранения . 2012 : 1–10. дои : 10.1155/2012/460508 . ISSN 1687-9805 . ПМЦ 3253456 . ПМИД 22235210 .
- ^ Бозе-О'Рейли, Стефан; Маккарти, Кэтлин М.; Стеклинг, Надин; Леттмайер, Беате (сентябрь 2010 г.). «Воздействие ртути и здоровье детей» . Современные проблемы детского и подросткового здравоохранения . 40 (8): 186–215. дои : 10.1016/j.cppeds.2010.07.002 . ПМК 3096006 . ПМИД 20816346 .
