Амальгама натрия
Амальгама натрия с общей формулой Na(Hg) представляет сплав ртути натрия и собой . Термин «амальгама» используется для обозначения сплавов, интерметаллических соединений и растворов (как твердых, так и жидких), содержащих ртуть в качестве основного компонента. Амальгамы натрия часто используются в реакциях как сильные восстановители с лучшими эксплуатационными характеристиками по сравнению с твердым натрием. Они менее опасно реагируют с водой и фактически часто используются в виде водной суспензии.
Амальгама натрия использовалась в качестве реагента еще в 1862 году. [1] Метод синтеза был описан Дж. Альфредом Ванклином в 1866 году. [2]
Структура и составы
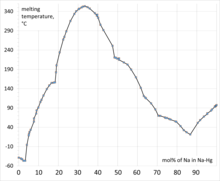
[ редактировать ]Никакой конкретной формулы «амальгаме натрия» не присвоено. Na 5 Hg 8 и Na 3 Hg являются четко определенными соединениями. В амальгамах натрия расстояния Hg-Hg увеличиваются примерно до 5 Å по сравнению с примерно 3 Å для самой ртути. [3] Обычно амальгамы классифицируют по весовому проценту натрия. Амальгамы с 2% Na при комнатной температуре являются твердыми веществами, тогда как некоторые более разбавленные амальгамы остаются жидкими. [4]
Подготовка
[ редактировать ]| Внешние видео | |
|---|---|
| Демонстрация и комментарий к приготовлению амальгамы натрия. | |
через YouTube | |
Металлический натрий растворяется в ртути экзотермически , т. е. с выделением тепла, поэтому образование амальгамы натрия опасно искрообразованием. [5] Этот процесс вызывает локальное кипение ртути, и по этой причине образование обычно проводится в вытяжном шкафу и часто выполняется безвоздушными методами , такими как синтез в безводном жидком парафине. Амальгаму натрия можно получить в лаборатории растворением металлического натрия в ртути или наоборот. [6] [7] [8] Амальгамы натрия можно приобрести в магазинах химической продукции.
Использование
[ редактировать ]Амальгама натрия использовалась в органической химии как мощный восстановитель , обращаться с которым безопаснее, чем с самим натрием. Он используется при деградации Эмде , а также для восстановления ароматических кетонов до гидролов. [9]
В конструкции натриевой лампы высокого давления используется амальгама натрия, обеспечивающая натрий для получения нужного цвета и ртуть для настройки электрических характеристик лампы.
Электролиз на ртутной ячейке
[ редактировать ]Амальгама натрия — побочный продукт хлора , получаемый электролизом в ртутных элементах . В этой ячейке рассол (концентрированный хлорида натрия раствор ) подвергается электролизу между жидким ртутным катодом и титановым или графитовым анодом . Хлор образуется на аноде, а натрий, образующийся на катоде, растворяется в ртути, образуя амальгаму натрия. Обычно эта амальгама натрия отводится и подвергается реакции с водой в «ячейке разложения» с образованием газообразного водорода , концентрированного раствора гидроксида натрия и ртути, которые подлежат вторичной переработке в процессе. В принципе, вся ртуть должна быть полностью переработана, но небольшая ее часть неизбежно теряется. Из-за опасений по поводу утечки этой ртути в окружающую среду процесс ртутных элементов обычно заменяется установками, в которых используется менее токсичный катод.
Ссылки
[ редактировать ]- ^ Аткинсон, Э. (1862). «XLI. Химические заметки из зарубежных журналов». Лондонский, Эдинбургский и Дублинский философский журнал и научный журнал . 24 (161): 305–311. дои : 10.1080/14786446208643359 .
- ^ Ванклин, Дж. Альфред (1866). «XII. — О новом способе формирования металлоорганических тел» . Дж. Хим. Соц . 19 : 128–130. дои : 10.1039/JS8661900128 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Кейт Р. Бушек «Амальгама натрия» в Энциклопедии реагентов для органического синтеза, 2001, Джон Уайли. дои : 10.1002/047084289X.rs040
- ^ W.4r Б. Ренфроу-младший и Ч.Р. Хаузер (1993). «Трифенилметил натрия» . Органические синтезы
{{cite journal}}: CS1 maint: numeric names: authors list (link); Сборник томов , т. 2, с. 607 . - ^ 3% Na в ртути: Бэбкок, Ш.; Ланкельма, HP; Вопичка, Э. (2007). «Амальгама натрия». Неорганические синтезы . Том. 1. С. 10–11. дои : 10.1002/9780470132326.ch4 . ISBN 978-0-470-13232-6 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ см. примечания в Ричард Н. Макдональд и Чарльз Э. Рейнеке (1988). «Транс-3,5-Циклогексадиен-1,2-дикарбоновая кислота» . Органические синтезы ; Сборник томов , т. 6, с. 461 .
- ^ Процедура получения Na(Hg) добавлением Na к Hg: Тони К. Т. Чанг, Майрон Розенблюм и Нэнси Симмс (1993). «Винилирование енолятов эквивалентом винилкатиона» . Органические синтезы
{{cite journal}}: CS1 maint: multiple names: authors list (link); Сборник томов , т. 8, с. 479 . - ^ Бахманн, МЫ (февраль 1933 г.). «Механизм восстановления амальгамой натрия и спиртом. I. Восстановление ароматических кетонов до гидролов». Журнал Американского химического общества . 55 (2): 770–774. дои : 10.1021/ja01329a051 . ISSN 0002-7863 .
Внешние ссылки
[ редактировать ]- Оксфордский паспорт безопасности материалов, заархивировано 17 декабря 2011 г. в Wayback Machine.
