Метабисульфит натрия

| |
| |
| Имена | |
|---|---|
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| Информационная карта ECHA | 100.028.794 |
| Номер ЕС |
|
| номер Е | Е223 (консерванты) |
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| Na2S2ONa2S2O5 | |
| Молярная масса | 190,107 г/моль |
| Появление | Порошок от белого до желтого цвета |
| Запах | Слабый SO 2 |
| Плотность | 1,48 г/см 3 |
| Температура плавления | 170 ° C (338 ° F; 443 К) разложение начинается при 150 ° C. |
| |
| Растворимость | Хорошо растворим в глицерине Мало растворим в этаноле |
| Опасности | |
| СГС Маркировка : | |
 
| |
| Опасность | |
| Х302 , Х318 | |
| P264 , P270 , P280 , P301+P312 , P305+P351+P338 , P310 , P330 , P501 | |
| NFPA 704 (огненный алмаз) | |
| NIOSH (пределы воздействия на здоровье в США): | |
ПЭЛ (допустимо)
|
Никто [ 1 ] |
РЕЛ (рекомендуется)
|
СВВ 5 мг/м 3 [ 1 ] |
IDLH (Непосредственная опасность)
|
без даты [ 1 ] |
| Паспорт безопасности (SDS) | Паспорт безопасности Маллинкродта |
| Родственные соединения | |
Другие анионы
|
Сульфит натрия Бисульфит натрия |
Другие катионы
|
Метабисульфит калия |
Родственные соединения
|
Дитионит натрия Тиосульфат натрия Сульфат натрия |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Метабисульфит натрия или пиросульфит натрия (написание IUPAC; Br. E. метабисульфит натрия или пиросульфит натрия ) — неорганическое соединение химической формулы Na 2 S 2 O 5 . Вещество иногда называют метабисульфитом динатрия. Используется как дезинфицирующее , антиоксидантное и консервирующее средство. [ 2 ] При растворении в воде образует бисульфит натрия .
Подготовка
[ редактировать ]Метабисульфит натрия можно получить обработкой раствора гидроксида натрия диоксидом серы . [ 3 ] При проведении в теплой воде Na 2 SO 3 сначала выпадает в осадок в виде желтого твердого вещества. При большем количестве SO 2 твердое вещество растворяется с образованием дисульфита, который кристаллизуется при охлаждении. [ 4 ]
- SO 2 + 2 NaOH → Na 2 SO 3 + H 2 O
- SO 2 + Na 2 SO 3 → Na 2 S 2 O 5
что дает остаток бесцветного твердого вещества Na 2 S 2 O 5 .
Химическая структура
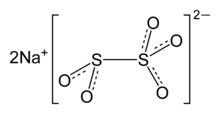
[ редактировать ]Анионный метабисульфит состоит из группы SO 2 , связанной с группой SO 3 , причем отрицательный заряд более локализован на конце SO 3 . Длина связи S–S составляет 2,22 Å, а «тионатные» и «тионитовые» расстояния S–O составляют 1,46 и 1,50 Å соответственно. [ 5 ]
Реактивность
[ редактировать ]При растворении в воде образуется бисульфит:
- Na 2 S 2 O 5 + H 2 O → 2 Na + + 2HSO3 −
Использование
[ редактировать ]Метабисульфит натрия и калия имеет множество основных и нишевых применений. Его широко используют для консервирования продуктов питания и напитков .
- Метабисульфит натрия добавляют в качестве вспомогательного вещества к лекарствам, содержащим адреналин ( адреналин ), чтобы предотвратить окисление адреналина. [ 6 ] Например, его добавляют в комбинированные лекарственные препараты, содержащие местный анестетик и адреналин. [ 6 ] и к составу автоинъекторов адреналина , таких как EpiPen. [ 7 ] Это продлевает срок годности препарата. [ 6 ] хотя метабисульфит натрия вступает в реакцию с адреналином, вызывая его разложение и образование сульфоната адреналина. [ 8 ]
- В сочетании с гидросульфитом натрия используется как средство для удаления пятен ржавчины. [ 9 ]
- Его используют в фотографии. [ 10 ]
- Концентрированный метабисульфит натрия можно использовать для удаления пней . Некоторые марки содержат 98% метабисульфита натрия и вызывают разложение лигнина в пнях, что облегчает удаление. [ 11 ]
- Он также используется в качестве вспомогательного вещества в некоторых таблетках , таких как парацетамол .
- Очень важным аспектом этого вещества, связанным со здоровьем, является то, что его можно добавлять в мазок крови при тестировании на серповидно-клеточную анемию (и другие подобные формы гемоглобина мутации ). Вещество вызывает серповидное расслоение несуществующих клеток (путем сложной полимеризации ), тем самым подтверждая заболевание.
- Используется в качестве отбеливателя при производстве кокосовых сливок.
- Он (или жидкий SO 2 ) обычно используется в виноделии как антимикробное и антиоксидантное средство; Бутилированное вино указывает на его использование с этикеткой «Содержит сульфиты» в США.
- Он используется в качестве восстановителя для разрыва сульфидных связей в севших предметах одежды из натуральных волокон, что позволяет одежде вернуться к своей первоначальной форме после стирки.
- Он используется в качестве источника SO 2 (в смеси с воздухом или кислородом) для разрушения цианида в коммерческих цианирования золота . процессах
- Его используют в качестве источника SO 2 (в смеси с воздухом или кислородом) для осаждения элементарного золота в золотохлористоводородных (царской водке) растворах.
- Он используется в водоочистной промышленности для гашения остаточного хлора.
- Его используют при тоновом травлении образцов металлов на основе железа для микроструктурного анализа. [ 12 ] [ 13 ]
- Он используется в качестве фунгицида для борьбы с микробами и плесенью при транспортировке потребительских товаров, таких как обувь и одежда. Перед отправкой добавляются пластиковые наклейки и упаковка (например, Micro-Pak ™ ), содержащие безводный твердый активный ингредиент метабисульфита натрия. Устройства поглощают влагу из атмосферы во время транспортировки и выделяют небольшое количество диоксида серы. [ 14 ]
- Используется для консервирования фруктов во время транспортировки. [ 15 ]
- Используется в качестве растворителя при экстракции крахмала из клубней. [ 16 ] фрукты, [ 17 ] и зерновые культуры. [ 18 ] [ 19 ]
- Он используется в качестве травильного агента для обработки мембран обратного осмоса под высоким давлением и нанофильтрации для опреснения воды для длительных периодов хранения между использованиями.
- Он используется для создания бисульфитного аддукта из кетонов, чтобы помочь в отделении кетонового продукта. Использование метабисульфита по сравнению с сульфитом также более энтропийно выгодно.
Безопасность
[ редактировать ]Метабисульфит натрия, несмотря на то, что он не горюч, разлагается при температуре 150 °C с выделением токсичных газов при разложении. Он коррозионно-активен при растворении в воде.
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с Карманный справочник NIOSH по химическим опасностям. «#0566» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Барбера, Хосе Хименес; Мецгер, Адольф; Вольф, Манфред (2000). «Химия сульфитов, тиосульфатов и дитионитов». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a25_477 . ISBN 3527306730 .
- ^ Кэтрин Э. Хаускрофт; Алан Дж. Шарп (2008). «Глава 16: Группа 16 элементов». Неорганическая химия, 3-е издание . Пирсон. п. 520. ИСБН 978-0-13-175553-6 .
- ^ Джонстон, Х.Ф. (1946). «Сульфиты и пиросульфиты щелочных металлов». Неорганические синтезы . Том. 2. С. 162–167. дои : 10.1002/9780470132333.ch49 . ISBN 9780470132333 .
- ^ К.Л. Картер, Т.А. Сиддики, К.Л. Мерфи, Д.В. Беннетт «Удивительно неуловимая кристаллическая структура метабисульфита натрия» Acta Crystallogr. (2004). Б60, 155–162. дои : 10.1107/S0108768104003325
- ^ Перейти обратно: а б с МакГи, Дуглас Л. (2013). «Местная и местная анестезия» . В Робертсе, Джеймс Р.; Джеррис, Р. Хеджес (ред.). Клинические процедуры Робертса и Хеджеса в неотложной медицине (6-е изд.). Эльзевир/Сондерс. п. 519. ИСБН 9781455748594 .
- ^ Ниязи, Сафараз К. (2009). Справочник по рецептурам для фармацевтического производства. Том 6, Стерильные продукты (2-е изд.). Нью-Йорк: Информа Здравоохранение. п. 410. ИСБН 9781420081312 .
- ^ Барнс, Эндрю Р. (2013). «Глава 48. Химическая стабильность лекарственных форм» . В Олтоне, Майкл Э.; Тейлор, Кевин М.Г. (ред.). Фармацевтика Олтона: разработка и производство лекарств (4-е изд.). Черчилль Ливингстон/Эльзевир. п. 833. ИСБН 9780702053931 .
- ^ «Ингредиенты» . Саммит брендов . 31 октября 2019 года . Проверено 25 апреля 2021 г.
- ^ Анчелл, Стив (2008). Поваренная книга в темной комнате (3-е изд.). Амстердам: Focal Press. стр. 193 . ISBN 978-0240810553 .
- ^ [1] [ мертвая ссылка ]
- ^ «Цветная металлография» . 04 мая 2011 г.
- ^ Джордж Ф. Вандер Воорт. «ТРАВЛЕНИЕ ИЗОТЕРМИЧЕСКИ ОБРАБОТАННЫХ СТАЛЕЙ» . Asminternational.org . Архивировано из оригинала (PDF) 16 октября 2022 года . Проверено 24 января 2022 г.
- ^ «Наклейки для улучшенной упаковки Micro-Pak» (PDF) . 05.05.2020.
- ^ Сивакумар, Д.; Корстен, Л. (05 мая 2020 г.). «15 — Личи (Litchi chinensis Sonn.)» . Послеуборочная биология и технология тропических и субтропических фруктов . Серия публикаций Woodhead по пищевой науке, технологиям и питанию. Вудхед. стр. 361–409д. дои : 10.1533/9780857092885.361 . ISBN 9781845697358 .
- ^ Манек, Рахул В.; Строители, Филип Ф.; Коллинг, Уильям М.; Эмехе, Мартинс; Кунле, Олобайо О. (июнь 2012 г.). «Физико-химические и связующие свойства крахмала, полученного из Cyperus esculentus» . AAPS PharmSciTech . 13 (2): 379–388. дои : 10.1208/s12249-012-9761-z . ISSN 1530-9932 . ПМЦ 3364391 . ПМИД 22350737 .
- ^ Наваб, Анджум; Алам, Фероз; Хак, Мухаммад Абдул; Хаснайн, Абид (2016). «Биоразлагаемая пленка из крахмала косточек манго: Влияние пластификаторов на физические, барьерные и механические свойства» . Крахмал - Штерке . 68 (9–10): 919–928. дои : 10.1002/star.201500349 . ISSN 1521-379X .
- ^ Ньякабау, Татенда; Вокадала, Обиро Катберт; Эммамбукс, Мохаммад Наушад (2013). «Влияние замачивающих добавок на извлечение теф-крахмала и его качество» . Крахмал - Штерке . 65 (9–10): 738–746. дои : 10.1002/star.201200241 . hdl : 2263/41924 . ISSN 1521-379X .
- ^ Парк, Ш.; Бин, СР; Уилсон, доктор медицинских наук; Шобер, Ти Джей (2006). «Быстрое выделение сорго и других зерновых крахмалов с использованием обработки ультразвуком» . Зерновая химия . 83 (6): 611–616. дои : 10.1094/CC-83-0611 . ISSN 1943-3638 .
