Нитрид натрия
| |
| Имена | |
|---|---|
| Название ИЮПАК
Нитрид натрия
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Информационная карта ECHA | 100.032.017 |
| Номер ЕС |
|
| Характеристики | |
| NaNa3N N | |
| Молярная масса | 82.976 g/mol |
| Появление | красновато-коричневое или темно-синее твердое вещество |
| Температура плавления | 87 ° C (189 ° F; 360 К) [1] (разлагается) |
| реагирует | |
| Структура | |
| Кубический, cP4 [2] | |
| вечера 3 м [2] | |
| Термохимия | |
Стандартная энтальпия
образование (Δ f H ⦵ 298 ) |
-151 Дж/моль [2] |
| Родственные соединения | |
Другие анионы
|
Амид натрия Имид натрия |
Другие катионы
|
Нитрид лития Нитрид калия |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Нитрид натрия — неорганическое соединение с химической формулой Na 3 N. В отличие от нитрида лития и некоторых других нитридов , нитрид натрия — крайне нестабильный щелочного металла нитрид . Его можно создать путем объединения атомных пучков натрия и азота , нанесенных на низкотемпературную сапфировую подложку. [1] Он легко разлагается на элементы:
Синтез
[ редактировать ]Нитрид натрия можно синтезировать двумя разными способами: разложением NaNH термическим 2 или прямой реакцией элементов. [2] Самый распространенный способ успешного синтеза нитрида натрия был использован Дитером Фишером, Мартином Янсеном и Григорием Важенином с использованием последнего метода. Первый способ заключается в раздельном введении Na и N 2 в газовой фазе в желаемых соотношениях и нанесении их в вакуумной камере на охлаждаемую подложку, которую затем нагревают до комнатной температуры (298 К) для кристаллизации. [1] Второй метод заключается во взаимодействии элементарного натрия с активированным плазмой азотом на поверхности металла. Этот синтез можно дополнительно облегчить, вводя в соединение жидкий сплав Na-K, удаляя излишки жидкости и промывая свежим сплавом. Затем твердое вещество отделяют от жидкости с помощью центрифуги. Однако метод Важенина очень чувствителен к воздуху и может быстро разлагаться и воспламеняться, если не подвергаться воздействию среды с чистым кислородом (O 2 ). [3]
Характеристики
[ редактировать ]Нитрид натрия может иметь красновато-коричневый или темно-синий цвет в зависимости от синтеза соединения из-за собственных свойств. [1] [3] Через несколько недель хранения при комнатной температуре он не проявляет признаков разложения. [3] Соединение не имеет точки плавления, поскольку оно разлагается обратно на свои элементарные формы, как показано с помощью масс-спектрометрии при температуре около 360 К. [1] [2] Расчетная энтальпия образования соединения составляет +64 кДж/моль. [3]
Структура
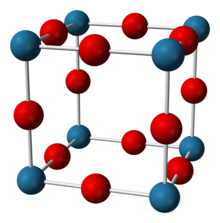
[ редактировать ]Нитрид натрия кажется примерно на 90% ионным при комнатной температуре, но имеет ширину запрещенной зоны, типичную для полупроводника. [2] [3] Он имеет структуру анти-ReO 3 с простой решеткой, состоящей из октаэдров NNa 6 . [1] [2] [3] [4] Соединение имеет длину связи N-Na 236,6 пм. [1] [3] Эта структура была подтверждена с помощью рентгеновской дифракции, а позже и нейтронной дифракции на порошке и монокристаллах. [1] [2] [3] [4]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час Фишер Д., Янсен М. (2002). «Синтез и строение Na 3 N». Энджью Чем . 41 (10): 1755–1756. doi : 10.1002/1521-3773(20020517)41:10<1755::AID-ANIE1755>3.0.CO;2-C . ПМИД 19750706 .
{{cite journal}}: CS1 maint: multiple names: authors list (link) Фишер, Д.; Канкаревич, З.; Шён, Дж. К.; Янсен, МЗ (2004). «Синтез и строение К 3 Н». З. Анорг. Аллг. Хим . 630 (1): 156. doi : 10.1002/zaac.200300280 . . «Приготовлено неуловимое бинарное соединение» Новости химии и техники 80, № 20 (20 мая 2002 г.) - ^ Перейти обратно: а б с д и ж г час Сангстер, Дж. (2004). «Система N-Na (азот-натрий)». Журнал фазового равновесия и диффузии . 25 (6): 560–563. дои : 10.1007/s11669-004-0082-0 . S2CID 97905377 .
- ^ Перейти обратно: а б с д и ж г час Важенин, Г.В. (2007). «Плазменный синтез и свойства Na 3 N». Неорганическая химия . 46 (13): 5146–5148. дои : 10.1021/ic700406q . ПМИД 17530752 .
- ^ Перейти обратно: а б Важенин Г.В., Хох К., Диннебье Р.Е., Сенишин А., Ньева Р. (2009). «Температурно-зависимое структурное исследование анти -ReO 3 -типа Na 3 N: искажать или не искажать?». Журнал неорганической и общей химии . 636 (1): 94–99. дои : 10.1002/zaac.200900488 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )
