Гидроксид алюминия
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Гидроксид алюминия | |
| Систематическое название ИЮПАК Тригидроксидоалюминий | |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.040.433 |
| КЕГГ | |
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики [1] [2] | |
| Ал(ОН) 3 | |
| Молярная масса | 78.003 g·mol −1 |
| Появление | Белый аморфный порошок |
| Плотность | 2,42 г/см 3 , твердый |
| Температура плавления | 300 ° С (572 ° F; 573 К) |
| 0,0001 г/(100 мл) | |
Произведение растворимости ( K sp ) | 3×10 −34 |
| Растворимость | растворим в кислотах и щелочах |
| Кислотность ( pKa ) | >7 |
| Изоэлектрическая точка | 7.7 |
| Термохимия [3] | |
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | −1277 кДж·моль −1 |
| Фармакология [4] | |
| A02AB01 ( ВОЗ ) | |
| Опасности | |
| СГС Маркировка : | |
| нет пиктограмм СГС | |
| нет заявлений об опасности | |
| P261 , P264 , P271 , P280 , P304+P340 , P305+P351+P338 , P312 , P337+P313 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Невоспламеняющийся |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза ) | >5000 мг/кг (крыса, перорально) |
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов |
| Родственные соединения | |
Другие анионы | Никто |
Родственные соединения | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
гидроксид алюминия , Al ( OH ) 3 встречается в природе как минерал гиббсит (также известный как гидраргиллит) и его три гораздо более редкие полиморфные модификации : байерит , дойлеит и нордстрандит. Гидроксид алюминия амфотерен , т. е. обладает как основными , так и кислотными свойствами. Близкими родственниками являются гидроксид оксида алюминия , AlO(OH) и оксид алюминия или оксид алюминия ( Al 2 O 3 ), последний из которых также амфотерен. Эти соединения вместе являются основными компонентами алюминиевой руды бокситов . Гидроксид алюминия также образует студенистый осадок в воде.
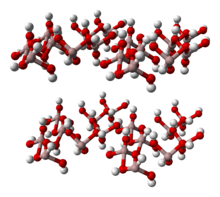
Структура
[ редактировать ]Al(OH) 3 состоит из двойных слоев гидроксильных групп, причем ионы алюминия занимают две трети октаэдрических отверстий между двумя слоями. [5] [6] четыре полиморфа . Выявлены [7] Все они состоят из слоев октаэдрических звеньев гидроксида алюминия с водородными связями между слоями. Полиморфы различаются расположением слоев. Все формы Al(OH) 3 имеют шестиугольную форму. Кристаллы [ оспаривается – обсуждаем ] :
- гиббсит также известен как γ- Ал(ОН) 3 [8] или α- Ал(ОН) 3 [ нужна ссылка ]
- Байерит также известен как α- Ал(ОН) 3 [8] или тригидрат β-оксида алюминия [ нужна ссылка ]
- Нордстрандит также известен как Ал(ОН) 3 [8]
- дойлит
Гидраргиллит , который когда-то считался гидроксидом алюминия, представляет собой фосфат алюминия . Тем не менее, и гиббсит , и гидраргиллит относятся к одному и тому же полиморфизму гидроксида алюминия: гиббсит чаще всего используется в Соединенных Штатах, а гидраргиллит чаще всего используется в Европе. Гидраргиллит назван в честь греческих слов, обозначающих воду ( гидра ) и глину ( аргиллес ). [ нужна ссылка ]
Характеристики
[ редактировать ]Гидроксид алюминия амфотерен . В кислоте он действует как основание Бренстеда-Лоури . Он нейтрализует кислоту с образованием соли: [9]
- 3 HCl + Al(OH) 3 → AlCl 3 + 3 H 2 O
В основаниях он действует как кислота Льюиса, связывая ионы гидроксида: [9]
- Аl(ОН) 3 + ОН − → [Ал(ОН) 4 ] −
Производство
[ редактировать ]
Практически весь гидроксид алюминия, используемый в коммерческих целях, производится по процессу Байера. [10] который включает растворение боксита в гидроксиде натрия при температуре до 270 ° C (518 ° F). Твердые отходы, бокситовые хвосты , удаляют, а гидроксид алюминия осаждают из оставшегося раствора алюмината натрия . Этот гидроксид алюминия можно превратить в оксид алюминия или оксид алюминия путем прокаливания . [ нужна ссылка ]
Остаток или хвосты бокситов , которые в основном состоят из оксида железа, очень едкие из-за остаточного гидроксида натрия. Исторически его хранили в лагунах; это привело к аварии на глиноземном заводе Айка в 2010 году в Венгрии, где прорыв дамбы привел к утоплению девяти человек. Еще 122 человека обратились за лечением от химических ожогов. Грязь загрязнила 40 квадратных километров (15 квадратных миль) земли и достигла Дуная . Хотя грязь считалась нетоксичной из-за низкого уровня содержания тяжелых металлов, pH суспензии составлял 13. [11]
Использование
[ редактировать ]Наполнитель и антипирен
[ редактировать ]Гидроксид алюминия находит применение в качестве огнезащитного наполнителя для полимеров. Он выбран для этих целей, поскольку он бесцветен (как и большинство полимеров), недорогой и обладает хорошими огнезащитными свойствами. [12] гидроксид магния и смеси хунтита и гидромагнезита . Аналогично применяют [13] [14] [15] [16] [17] Он разлагается при температуре около 180 ° C (356 ° F), поглощая при этом значительное количество тепла и выделяя водяной пар.
Помимо огнезащитных свойств, он очень эффективен в качестве средства подавления дыма для широкого спектра полимеров, особенно для полиэфиров , акрила , этиленвинилацетата , эпоксидных смол , поливинилхлорида (ПВХ) и каучука . [18]
Гидроксид алюминия используется в качестве наполнителя в некоторых искусственного камня материалах из , часто в акриловой смоле . [ нужна ссылка ]
Прекурсор соединений Al
[ редактировать ]Гидроксид алюминия является сырьем для производства других соединений алюминия: прокаленных оксидов алюминия, сульфата алюминия , хлорида полиалюминия, хлорида алюминия , цеолитов , алюмината натрия , активированного оксида алюминия и нитрата алюминия . [6]
Свежеосажденный гидроксид алюминия образует гели , которые являются основой для применения солей алюминия в качестве флокулянтов при очистке воды. Этот гель со временем кристаллизуется. Гели гидроксида алюминия можно дегидратировать (например, с помощью смешивающихся с водой неводных растворителей, таких как этанол ) с образованием аморфного порошка гидроксида алюминия, который легко растворяется в кислотах. Нагревание превращает его в активированные оксиды алюминия, которые используются в качестве осушителей , адсорбентов при очистке газов и носителей катализаторов . [12]
Фармацевтический
[ редактировать ]Под общим названием «альгелдрат» гидроксид алюминия используется в качестве антацида у людей и животных (в основном кошек и собак). Он предпочтительнее других альтернатив, таких как бикарбонат натрия, потому что Al(OH) 3 , будучи нерастворимым, не повышает pH желудка выше 7 и, следовательно, не вызывает секрецию избыточной кислоты желудком. Торговые марки включают Alu-Cap, Aludrox, Gaviscon или Pepsamar. Вступает в реакцию с избытком кислоты в желудке, снижая кислотность содержимого желудка. [19] [20] которые могут облегчить симптомы язвы , изжоги или диспепсии . Такие продукты могут вызвать запор , поскольку ионы алюминия подавляют сокращения гладкомышечных клеток желудочно-кишечного тракта, замедляя перистальтику и удлиняя время, необходимое для прохождения стула через толстую кишку . [21] Некоторые такие продукты созданы для минимизации таких эффектов за счет включения равных концентраций гидроксида или карбоната магния , которые оказывают уравновешивающее слабительное действие. [22]
Это соединение также используется для контроля гиперфосфатемии (повышенного уровня фосфата или фосфора в крови) у людей и животных, страдающих почечной недостаточностью. Обычно почки фильтруют излишки фосфатов из крови, но почечная недостаточность может привести к накоплению фосфатов. Соль алюминия при попадании в организм связывается с фосфатом в кишечнике и снижает количество усваиваемого фосфора. [23] [24]
Осажденный гидроксид алюминия включается в качестве адъюванта в некоторые вакцины (например, в вакцину против сибирской язвы ). Одной из известных марок адъюванта гидроксида алюминия является Альгидрогель производства Brenntag Biosector. [25] [ нужна полная цитата ] [ мертвая ссылка ] Поскольку он хорошо поглощает белок, он также выполняет функцию стабилизации вакцин, предотвращая осаждение или прилипание белков в вакцине к стенкам контейнера во время хранения. Гидроксид алюминия иногда называют « квасцами » — термин, обычно обозначающий один из нескольких сульфатов. [ нужна ссылка ]
Составы вакцин, содержащие гидроксид алюминия, стимулируют иммунную систему , вызывая выделение мочевой кислоты , что является иммунологическим сигналом опасности . Это сильно привлекает определенные типы моноцитов , которые дифференцируются в дендритные клетки . Дендритные клетки захватывают антиген, переносят его в лимфатические узлы и стимулируют Т- и В-клетки . [26] По-видимому, он способствует индукции хорошего ответа Th2 , поэтому полезен для иммунизации против патогенов, блокируемых антителами. Однако он обладает небольшой способностью стимулировать клеточный (Th1) иммунный ответ, что важно для защиты от многих патогенов. [27] он также бесполезен, когда антиген основан на пептидах . [28]
Безопасность
[ редактировать ]В 1960-х и 1970-х годах предполагалось, что алюминий связан с различными неврологическими расстройствами , включая болезнь Альцгеймера . [29] [30] С тех пор многочисленные эпидемиологические исследования не обнаружили связи между воздействием алюминия из окружающей среды или проглоченного алюминия и неврологическими расстройствами, хотя инъекционный алюминий в этих исследованиях не рассматривался. [31] [32] [33]
Нервные расстройства были обнаружены в экспериментах на мышах, мотивированных болезнью войны в Персидском заливе (GWI). Гидроксид алюминия, введенный в дозах, эквивалентных тем, которые вводились военным США, показал увеличение реактивных астроцитов, усиление апоптоза мотонейронов и пролиферацию микроглии в спинном мозге и коре головного мозга. [34]
Ссылки
[ редактировать ]- ^ Для произведения растворимости: «Константы произведения растворимости» . Архивировано из оригинала 15 июня 2012 года . Проверено 17 мая 2012 г.
- ^ Для изоэлектрической точки: Гейер, К.Х.; Томпсон, округ Колумбия; Заичек, ОТ (сентябрь 1958 г.). «Растворимость гидроксида алюминия в кислых и основных средах при 25 °С» . Канадский химический журнал . 36 (9): 1268–1271. дои : 10.1139/v58-184 . ISSN 0008-4042 .
- ^ Зумдал, Стивен С. (2009). Химические принципы (6-е изд.). Компания Хоутон Миффлин. ISBN 978-0-618-94690-7 .
- ^ Блэк, Рональд А.; Хилл, Д. Эшли (15 июня 2003 г.). «Лекарства, отпускаемые без рецепта при беременности» . Американский семейный врач . 67 (12): 2517–2524. ISSN 0002-838X . ПМИД 12825840 . Проверено 1 июля 2017 года .
- ^ Уэллс, А.Ф. (1975), Структурная неорганическая химия (4-е изд.), Оксфорд: Clarendon Press
- ^ Jump up to: а б Эванс, Калифорния (1993). «Свойства и применение оксидов и гидроксидов алюминия». В Эй Джей Даунсе (ред.). Химия алюминия, галлия, индия и таллия (1-е изд.). Лондон; Нью-Йорк: Blackie Academic & Professional. ISBN 9780751401035 .
- ^ Карамалидис, АК; Джомбак Д.А. (2010). Моделирование поверхностного комплексообразования: гиббсит . Джон Уайли и сыновья . стр. 15–17. ISBN 978-0-470-58768-3 .
- ^ Jump up to: а б с Веферс, Карл; Мисра, Чанакья (1987). Оксиды и гидроксиды алюминия . Исследовательские лаборатории Алкоа. п. 2. ОКЛК 894928306 .
- ^ Jump up to: а б Безграничный (26 июля 2016 г.). «Основные и амфотерные гидроксиды» . Безграничная химия . Архивировано из оригинала 22 августа 2017 года . Проверено 2 июля 2017 г.
- ^ Хинд, Арканзас; Бхаргава СК; Грокотт СК (1999). «Химия поверхности твердых тел процесса Байера: обзор». Коллоиды Surf Physiochem Eng Аспекты . 146 (1–3): 359–74. дои : 10.1016/S0927-7757(98)00798-5 .
- ^ «Венгрия борется за то, чтобы остановить поток токсичного осадка» . Новостной сайт BBC . 5 октября 2010 г.
- ^ Jump up to: а б Хадсон, Л. Кейт; Мишра, Чанакья; Перротта, Энтони Дж.; Веферс, Карл; Уильямс, Ф.С. (2000). «оксид алюминия». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a01_557 . ISBN 3527306730 .
- ^ Холлингбери, Луизиана; Халл ТР (2010). «Огнезащитные свойства хунтита и гидромагнезита — обзор» (PDF) . Деградация и стабильность полимеров . 95 (12): 2213–2225. doi : 10.1016/j.polymdegradstab.2010.08.019 .
- ^ Холлингбери, Луизиана; Халл ТР (2010). «Термическое разложение хунтита и гидромагнезита - обзор» (PDF) . Термохимика Акта . 509 (1–2): 1–11. дои : 10.1016/j.tca.2010.06.012 .
- ^ Холлингбери, Луизиана; Халл ТР (2012). «Огнезащитное действие хунтита в природных смесях с гидромагнезитом» (PDF) . Деградация и стабильность полимеров . 97 (4): 504–512. doi : 10.1016/j.polymdegradstab.2012.01.024 .
- ^ Холлингбери, Луизиана; Халл ТР (2012). «Термическое разложение природных смесей хунтита и гидромагнезита» (PDF) . Термохимика Акта . 528 : 45–52. дои : 10.1016/j.tca.2011.11.002 .
- ^ Халл, ТР; Витковский А; Холлингбери, Лос-Анджелес (2011). «Огнезащитное действие минеральных наполнителей» (PDF) . Деградация и стабильность полимеров . 96 (8): 1462–1469. doi : 10.1016/j.polymdegradstab.2011.05.006 . S2CID 96208830 .
- ^ Инженерные материалы Huber. «Безгалогенные огнезащитные добавки Huber» (PDF) . Проверено 3 июля 2017 г.
- ^ Гэлбрейт, А; Буллок, С; Маниас, Э; Хант, Б; Ричардс, А. (1999). Основы фармакологии: учебник для медсестер и медицинских работников . Харлоу: Пирсон. п. 482.
- ^ Папич, Марк Г. (2007). «Гидроксид алюминия и карбонат алюминия». Справочник Сондерса по ветеринарным препаратам (2-е изд.). Сент-Луис, Миссури: Сондерс/Эльзевир. стр. 15–16. ISBN 9781416028888 .
- ^ Вашингтон, Нина (2 августа 1991 г.). Антациды и антирефлюксные средства . Бока-Ратон, Флорида: CRC Press. п. 10. ISBN 978-0-8493-5444-1 .
- ^ Билл, Роберт Л. (1 сентября 2016 г.). Клиническая фармакология и терапия для ветеринарных врачей — Электронная книга . Elsevier Науки о здоровье. п. 105. ИСБН 9780323444026 .
- ^ Пламб, Дональд К. (2011). «Гидроксид алюминия». Справочник ветеринарных препаратов Пламба (7-е изд.). Стокгольм, Висконсин; Эймс, Айова: Уайли. стр. 36–37. ISBN 9780470959640 .
- ^ Lifelearn Inc. (1 ноября 2010 г.). «Гидроксид алюминия» . Знай своего питомца . Проверено 30 июня 2017 г.
- ^ «О биосекторе Бреннтаг - Бреннтаг» . brenntag.com . Проверено 19 апреля 2018 г.
- ^ Кул, М; Сулье Т; ван Нимвеген М; Уилларт М.А.; Маскенс Ф; Юнг С; Хогстеден ХК; Хаммад Х; Ламбрехт Б.Н. (24 марта 2008 г.). «Алюминиевый адъювант повышает адаптивный иммунитет, индуцируя образование мочевой кислоты и активируя воспалительные дендритные клетки» . Джей Эксп Мед . 205 (4): 869–82. дои : 10.1084/jem.20071087 . ПМК 2807488 . ПМИД 18362170 .
- ^ Петровский Н., Агилар Дж.К. (2004). «Вакцинные адъюванты: современное состояние и будущие тенденции». Иммунология и клеточная биология . 82 (5): 488–96. дои : 10.1111/j.0818-9641.2004.01272.x . ПМИД 15479434 . S2CID 154670 .
- ^ Кранаж, депутат парламента; Робинсон А. (2003). Робинсон А; Хадсон М.Дж.; Кранаж МП (ред.). Протоколы вакцинации - Том 87 «Методов биомедицинских протоколов молекулярной медицины» (2-е изд.). Спрингер . п. 176. ИСБН 978-1-59259-399-6 .
- ^ «Миф о болезни Альцгеймера» . Ассоциация Альцгеймера . Проверено 29 июля 2012 г.
- ^ Хан, А. (1 сентября 2008 г.). «Алюминий и болезнь Альцгеймера» . Общество Альцгеймера . Архивировано из оригинала 11 марта 2012 года . Проверено 8 марта 2012 г.
- ^ Рондо V (2002). «Обзор эпидемиологических исследований алюминия и кремнезема в отношении болезни Альцгеймера и связанных с ней расстройств» . Преподобный Environ Health . 17 (2): 107–21. дои : 10.1515/REVEH.2002.17.2.107 . ПМЦ 4764671 . ПМИД 12222737 .
- ^ Мартин К.Н., Коггон Д.Н., Инскип Х., Лейси Р.Ф., Янг В.Ф. (май 1997 г.). «Концентрация алюминия в питьевой воде и риск болезни Альцгеймера» . Эпидемиология . 8 (3): 281–6. дои : 10.1097/00001648-199705000-00009 . JSTOR 3702254 . ПМИД 9115023 . S2CID 32190038 .
- ^ Грейвс А.Б., Рознер Д., Эчеверрия Д., Мортимер Дж.А., Ларсон Э.Б. (сентябрь 1998 г.). «Профессиональное воздействие растворителей и алюминия и предполагаемый риск болезни Альцгеймера» . Оккуп Энвирон Мед . 55 (9): 627–33. дои : 10.1136/oem.55.9.627 . ПМЦ 1757634 . ПМИД 9861186 .
- ^ Шоу, Кристофер А.; Петрик, Майкл С. (ноябрь 2009 г.). «Инъекции гидроксида алюминия приводят к двигательному дефициту и дегенерации двигательных нейронов» . Журнал неорганической биохимии . 103 (11): 1555–1562. дои : 10.1016/j.jinorgbio.2009.05.019 . ISSN 1873-3344 . ПМЦ 2819810 . ПМИД 19740540 .
Внешние ссылки
[ редактировать ]- Международная карта химической безопасности 0373
- «Некоторые свойства гидроксида алюминия, осаждаемого в присутствии глины», Институт почвенных исследований, Р. К. Тернер, Министерство сельского хозяйства, Оттава.
- Влияние старения на свойства полиядерных катионов гидроксиалюминия
- Второй вид полиядерного катиона гидроксиалюминия, его образование и некоторые свойства.

