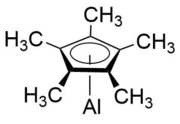
(Пентаметилциклопентадиенил)алюминий(I)
| |
| Имена | |
|---|---|
| Другие имена
AlCp*, Cp*Al
| |
| Идентификаторы | |
| |
| Характеристики | |
| С 10 Н 15 Ал | |
| Молярная масса | 162.212 g·mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
(Пентаметилциклопентадиенил)алюминий(I) представляет собой металлоорганическое соединение формулы Al(C 5 Me 5 ) («Me» — метильная группа ; CH 3 ). Соединение часто обозначают AlCp* или Cp*Al, где Cp* — пентаметилциклопентадиенид-анион (C 5 Me 5 − ). Обнаружен в 1991 году Домейером и др. , [1] AlCp* служит первым задокументированным примером стабильного при комнатной температуре соединения одновалентного алюминия . В изолированной форме Cp*Al существует в виде тетрамера [ Cp*Al] 4 и представляет собой желтый кристалл, который разлагается при температуре выше 100 °C, но также сублимируется при температуре выше 140 °C. [1] [2]
Синтез
[ редактировать ]Самый ранний документально подтвержденный синтез и характеристика Cp*Al были проведены Dohmeier et al. в 1991 году, [1] где четыре эквивалента AlCl в толуоле / диэтиловом эфире взаимодействуют с двумя эквивалентами 2[Mg(Cp*) 2 ] с образованием [Cp*Al] 4 в виде желтых кристаллов:
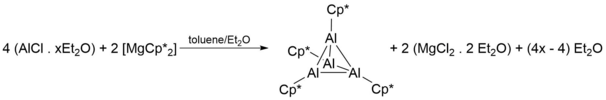
Несмотря на то, что описанная выше схема синтеза успешно дает тетраметры [Cp*Al] 4 с разумными выходами (44%), использование AlCl оказалось проблематичным, поскольку синтез AlCl требует жестких условий, а его реакционная природа затрудняет хранение. Таким образом, были открыты более простые способы синтеза тетрамера [Cp*Al] 4 и потребовалось восстановление Cp*AlX 2 (X = Cl , Br , I ) металлом ( K, когда X = Cl ) или металлом. сплав ( сплавы Na /K, когда X = Br, I): [3] [4] [5] [6] [7]

Более экзотические способы синтеза [Cp*Al] 4 включают контролируемое диспропорционирование диалана Al(II) на составляющие продукты Al(I) и Al(III). Например, взаимодействие диалана [Cp*AlBr] 2 с основанием Льюиса, таким как пиридин, основание Льюиса стабилизирует [Cp*AlBr 2 ] и [Cp*Al] 4 . [8]
Мономерный Cp*Al также был выделен в твердой матрице Ar путем нагревания [Cp*Al] 4 в толуоле до 133 °C и распыления полученных паров с Ar на медный блок, выдержанный при 12 K. [9]
Структура и связь
[ редактировать ]Рентгеновские кристаллографические данные показали, что Cp*Al существует исключительно в виде тетрамера в твердом состоянии. Этот тетрамер, [Cp*Al] 4 , состоит из тетраэдра Al 4 , а кольца Cp* имеют форму ŋ 5 -координирован с катионом алюминия(I) так, что плоскости C 5 Me 5 - кольца примерно параллельны противоположному основанию тетраэдра Al 4 . [1] Перпендикулярное расстояние между Al и кольцом Cp*, определенное с помощью кристаллографии, находится в диапазоне от 199,7 до 203,2 пм со средним значением 201,5 пм. [1] Связь Al-Al в [Cp*Al] 4 составляет 276,9 пм, что немного короче, чем у металлического алюминия, длина связи Al-Al которого составляет 286 пм. [1] Кроме того, связь Al-Al в [Cp*Al] 4 значительно короче, чем в других олигомерных и полимерных материалах III группы M(I)-ŋ. 5 -Cp*-соединения, такие как октаэдрические [InCp*] 6 (394, 336 пм), димерные [InCp*] 2 (363,1 пм) и полимерные [TlCp*] (641 пм), что указывает на значительно большее взаимодействие между атомами алюминия в [Cp*Al] 4, чем одновалентные соединения Cp* In(I) и Tl(I). [3] Дополнительные характеристики, которые были выполнены, включают рамановскую спектроскопию , которая обнаружила рамановскую активную дыхательную вибрацию (A 1 , 377 см-1) тетраэдра Al 4 в [Cp*Al] 4 . [1]
орбитали естественной связи Анализ (NBO) [Cp*Al] и [Cp*Al] 4 с использованием B3LYP/6-31G(d,p) показал, что средний перенос заряда на фрагмент Cp* на атом Al составляет 0,657 и 0,641 соответственно. . Это немного превышает значения переноса заряда, рассчитанные для [CpAl] и [Cp*Al] 4 (0,630 и 0,591 соответственно). Расчет NBO разрыва ВЗМО-НСМО в [Cp*Al] также выявил значительное уменьшение в тетрамерном комплексе [Cp*Al] 4 по сравнению с мономерным [Cp*Al] (4,36 по сравнению с 5,49), что согласуется с плотностью Функциональная теория расчетов аналогичных систем, включая суператомов комплексы золота , алюминия и галлия . [10] Расчеты атомов в молекулах (AIM) показывают, что связь Al-Al является металлической. [11] стабилизация [Cp*Al] 4 относительно [CpAl] 4 возникает за счет добавления взаимодействий HH на метильных группах, присоединенных к лиганду Cp*, в отличие от увеличения связывающих взаимодействий Al-Al. Считается, что [11]
Несмотря на свою типично тетрамерную форму, мономер Cp*Al был выделен и изучен в газовой фазе с помощью газофазной дифракции электронов . В газообразной мономерной форме перпендикулярное расстояние между кольцом Al и кольцом Cp* было рассчитано равным 206,3(8) пм, что немного больше, чем у тетрамерного [Cp*Al] 4 . [2]
Реактивность
[ редактировать ]Было показано, что при выделении в твердой матрице Ar, легированной H 2 , мономерный Cp*Al образует гидридные разновидности H 2 Cp*Al при воздействии H 2 и фотолизе с помощью ртутной лампы: [9]
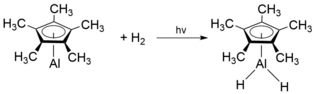
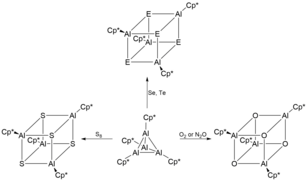
При температуре выше 100 °С [Cp*Al] 4 разлагается с образованием пентаметилциклопентандиена (Cp*H), металлического алюминия (Al(0)) и других нелетучих соединений Al(III). [2] Общая стабильность [Cp*Al] 4 уникальна, поскольку существует термодинамическое сродство к тетрамерным соединениям алюминия(I) ([RAl] 4 ) к диспропорционированию на элементарный алюминий и R 3 Al. можно синтезировать ряд различных новых олигомерных структур . Таким образом, при использовании тетрамерного [Cp*Al] 4 в качестве предшественника [6] Например, обработка [Cp*Al] 4 избытком селена и теллура в мягких условиях дает уникальные гетерокубановые структуры [Cp*AlSe] 4 и [Cp*AlTe] 4 соответственно. [4] Эти гетерокубановые структуры чрезвычайно чувствительны к воздуху и влаге, что приводит к их разложению и выделению H 2 Se и H 2 Te соответственно. Аналогично, реакция [Cp*Al] 4 с более легкими халькогенами , такими как O 2 , N 2 O и сера, дает [Cp*AlX] 4 (X = O, S). [12]
[Cp*Al] 4 также использовался в качестве предшественника для синтеза первого в мире стабильного димерного иминоалана, содержащего гетероцикл Al 2 N 2 , путем обработки [Cp*Al] 4 Me 3 SiN 3 в молярном соотношении 1:4. . [13] Полученные иминоаланы характеризовались тем, что они содержали идеально плоское ядро Al 2 N 2 с тремя координационными атомами алюминия и азота. Другие димерные иминоаланы, включая [Cp*AlNSi( i -Pr) 3 ] 2 , [Cp*AlNSiPh 3 ] 2 и [Cp*AlNSi( t -Bu) 3 ] 2, с тех пор были синтезированы с использованием [Cp*Al] 4 в качестве предшественник путем окислительного присоединения органического азида. [3]

Функция лиганда
[ редактировать ]
[Cp*Al] способен выступать в качестве атипичного экзотического лиганда в связях донорно-акцепторного типа. Например, смешивание [Cp*Al] 4 с кислотой Льюиса B(C 6 F 6 ) 3 образует связь донорно-акцепторного типа Al-B и приводит к синтезу аддукта [Cp*Al-B(C 6 Ф 6 ) 3 ]. [14] Аналогичные комплексы основной группы, которые были синтезированы и охарактеризованы, включают диалановые комплексы [Cp*Al-Al(C 6 F 5 ) 3 ] [15] и [Cp*Al-Al( t -Bu) 3 ], [16] и комплексы группа 13-группа 13 [Cp*Al-Ga( t -Bu) 3 ]. [16]
[Cp*Al] также способен действовать как мощный лиганд для переходных металлов . Например, обработка [Cp*Al] [(dcpe)Pt(H)(CH 2 t -Bu)] (dcpe = бис(дициклогексилфосфино)этан) дает [(dcpe)Pt(Cp*Al) 2 ]. [17] Другие переходные металлы, которые используют [Cp*Al] в качестве лиганда, включают, помимо прочего, d 10 металлоцентровые комплексы, такие как [Pd(Cp*Al) 4 ] и [Ni(Cp*Al) 4 ], [18] и лантаноидов / актинидов металлоцентрические комплексы , такие как (CpSiMe 3 ) 3 U-AlCp*, (CpSiMe 3 )3Nd-AlCp* и (CpSiMe 3 ) 3 Ce-AlCp*. [3] [19]

Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г Домейер, Карстен; Робл, Кристиан; Таке, Матиас; Шнёкель, Хансгеорг (1991). «Тетрамерное соединение алюминия (I) [{Al (η 5 -C 5 Me 5 } 4 ] . ) (5): 564–565. doi:10.1002/anie.199105641. ISSN 0570-0833.
- ^ Jump up to: а б с Хааланд, Арне; Мартинсен, Чель-Гуннар; Шлыков Сергей А.; Вольден, Ханс Видар; Домейер, Карстен; Шнёкель, Хансгеорг (1995). «Молекулярная структура мономерного (пентаметилциклопентадиенил) алюминия (I) методом газофазной электронной дифракции». Металлоорганические соединения . 14 (6): 3116–3119. дои : 10.1021/om00006a065 . ISSN 0276-7333 .
- ^ Jump up to: а б с д Лю, Яшуай; Ли, Цзя; Ма, Сяоли; Ян, Чжи; Роски, Герберт В. (2018). «Химия алюминия (I) с β-дикетиминатными лигандами и пентаметилциклопентадиенильными заместителями: синтез, реакционная способность и применение». Обзоры координационной химии . 374 : 387–415. дои : 10.1016/j.ccr.2018.07.004 . ISSN 0010-8545 . S2CID 105749253 .
- ^ Jump up to: а б Шульц, Стефан; Роски, Герберт В.; Кох, Ханс Иоахим; Шелдрик, Джордж М.; Сталке, Дитмар; Кун, Аня (1993). «Простой синтез [(Cp*Al) 4 ] и его преобразование в гетерокубаны [(Cp*AlSe) 4 ] и [(Cp*AlTe) 4 ](Cp*=η 5 -C5 CH3 ( ) 5 ) Angewandte Chemie International Edition in English. 32 (12): 1729–1731. doi:10.1002/anie.199317291. ISSN 0570-0833.
- ^ Шорманн, Марк; Климек, Клаус С.; Хатоп, Хаген; Варки, Саджи П.; Роски, Герберт В.; Леманн, Кристофер; Ропкен, Корд; Хербст-Ирмер, Регина; Нольтемейер, Матиас (2001). «Натрий-калиевый сплав для восстановления моноалкильных соединений алюминия (III)». Журнал химии твердого тела . 162 (2): 225–236. Бибкод : 2001JSSCh.162..225S . дои : 10.1006/jssc.2001.9278 . ISSN 0022-4596 .
- ^ Jump up to: а б Нагендран, Сельвараджан; Роски, Герберт В. (февраль 2008 г.). «Химия алюминия (I), кремния (II) и германия (II)». Металлоорганические соединения . 27 (4): 457–492. дои : 10.1021/om7007869 . ISSN 0276-7333 .
- ^ Минасян, Стефан Г.; Арнольд, Джон (2008). «Синтез и реакционная способность бис-пентаметилциклопентадиенилдииоддиалана (Cp*AlI) 2 : предшественника алюминия (ii) для (Cp*Al) 4 ». Химические коммуникации (34): 4043–5. дои : 10.1039/b806804f . ISSN 1359-7345 . ПМИД 18758620 .
- ^ Хофманн, Александр; Лампрехт, Анна; Хименес-Халла, Дж. Оскар К.; Утешитель, Тобиас; Дьюхерст, Райан Д.; Ленчик, Карстен; Брауншвейг, Хольгер (9 августа 2018 г.). «Диспропорционирование диалана, вызванное основанием Льюиса». Химия: Европейский журнал . 24 (45): 11795–11802. дои : 10.1002/chem.201802300 . ISSN 1521-3765 . ПМИД 29920807 . S2CID 49308900 .
- ^ Jump up to: а б Химмель, Ханс-Йорг; Волле, Жан (декабрь 2002 г.). «Исследование реакционной способности соединений алюминия (I): реакция пентаметилциклопентадиенилалюминия, Al[C 5 (CH 3 ) 5 ], мономеров с диводородом в твердой матрице Ar с образованием новой молекулы гидрида алюминия H 2 Al[C 5 ] (СН 3 ) 5 ]». Металлоорганические соединения . 21 (26): 5972–5977. дои : 10.1021/om020787x . ISSN 0276-7333 .
- ^ Уильямс, Кристен С.; Хупер, Джозеф П. (08 декабря 2011 г.). «Структура, термодинамика и энергетическое содержание алюминиево-циклопентадиенильных кластеров». Журнал физической химии А. 115 (48): 14100–14109. Бибкод : 2011JPCA..11514100W . дои : 10.1021/jp207292t . hdl : 10945/48676 . ISSN 1089-5639 . ПМИД 22007955 . S2CID 2992445 .
- ^ Jump up to: а б Мэн, Линпэн; Цзэн, Яньли; Сунь, Чжэн; Ли, Сяоянь; Лу, Фейфей (28 июля 2015 г.). «Влияние заместителей на связь М–М в Cp4Al4 и Cp2M2X2 (M = B, Al, Ga; Cp = C5H5, X = галоген)». Транзакции Далтона . 44 (31): 14092–14100. дои : 10.1039/C5DT01901J . ISSN 1477-9234 . ПМИД 26171664 .
- ^ Стельцер, Адриан К.; Хробарик, Питер; Браун, Томас; Каупп, Мартин; Браун-Кула, Беатрис (29 апреля 2016 г.). «Завершение семейства гетерокубанов [Cp*AlE] 4 (E = O, S, Se и Te) путем селективного оксигенирования и сульфирования [Cp*Al] 4 по теории функциональной плотности : расчеты [Cp*AlE] 4 и реакционная способность [Cp*AlO] 4 в сторону гидролиза». Неорганическая химия . 55 (10): 4915–4923. doi : 10.1021/acs.inorgchem.6b00462 . ISSN 0020-1669 . ПМИД 27129027 .
- ^ Шульц, Стефан; Хеминг, Людгер; Хербст-Ирмер, Регина; Роски, Герберт В.; Шелдрик, Джордж М. (18 мая 1994 г.). «Синтез и структура первого димерного иминоалана, содержащего гетероцикл Al 2 N 2 ». Angewandte Chemie International Edition на английском языке . 33 (9): 969–970. дои : 10.1002/anie.199409691 . ISSN 0570-0833 .
- ^ Горден, Джон Д.; Фойгт, Андреас; Макдональд, Чарльз Л.Б.; Сильверман, Джоэл С.; Коули, Алан Х. (2000). «Аддукт кислоты Льюиса аландиила: связь алюминий (I)-донор бора-акцептор». Журнал Американского химического общества . 122 (5): 950–951. дои : 10.1021/ja993537p . ISSN 0002-7863 .
- ^ Горден, Джон Д.; Макдональд, Чарльз Л.Б.; Коули, Алан Х. (2001). «Валентный изомер диалана» . Химические коммуникации (1): 75–76. дои : 10.1039/B007341P . ISSN 1359-7345 .
- ^ Jump up to: а б Шульц, Стефан; Кучковски, Андреас; Шухманн, Даниэлла; Флёрке, Ульрих; Нигер, Мартин (2006). «Группа 13-Группа 13 Донорно-акцепторные комплексы». Металлоорганические соединения . 25 (22): 5487–5491. дои : 10.1021/om0606946 . ISSN 0276-7333 .
- ^ Вайс, Дана; Стейнке, Тобиас; Зима, Мануэла; Фишер, Роланд А.; Фрелих, Николаус; Уддин, Джамал; Френкинг, Гернот (2000). «[(dcpe)Pt(ECp*) 2 ] (E = Al, Ga): Синтез, структура и ситуация связывания первых комплексов алюминия (I) и галлия (I) с фосфинзамещенными центрами переходных металлов». Металлоорганические соединения . 19 (22): 4583–4588. дои : 10.1021/om000310q . ISSN 0276-7333 .
- ^ Бучин, Беатрис; Стейнке, Тобиас; Гемель, Кристиан; Каденбах, Томас; Фишер, Роланд А. (2005). «Синтез и характеристика романа Эл. я Соединение Al(C 5 Me 4 Ph): сравнение координационной химии Al(C 5 Me 5 ) и Al(C 5 Me 4 Ph) при d. 10 Металлические центры». Журнал неорганической и общей химии . 631 (13–14): 2756–2762. doi : 10.1002/zaac.200500129 . ISSN 0044-2313 .
- ^ Минасян, Стефан Г.; Кринский, Джамин Л.; Райнхарт, Джеффри Д.; Коппинг, Рой; Тылищак, Толек; Януш, Маркус; Шух, Дэвид К.; Арнольд, Джон (30 сентября 2009 г.). «Сравнение связей 4 f и 5 f металл-металл в (CpSiMe 3 ) 3 M-ECp * (M = Nd, U; E = Al, Ga; Cp * = C 5 Me 5 ): синтез, термодинамика, магнетизм. и электронная структура». Журнал Американского химического общества . 131 (38): 13767–13783. дои : 10.1021/ja904565j . ISSN 0002-7863 . ПМИД 19725526 .